Clear Sky Science · de
PRMT6 ist erforderlich, um makrophageninduzierte Entzündungen bei heterotoper Ossifikation zu initiieren und zu verstärken, indem CCL2‑Expression erhöht wird
Wenn Heilung zu weit geht
Manchmal versucht der Körper nach einer schweren Verletzung oder Operation so intensiv zu heilen, dass er tatsächlich neuen Knochen an Stellen bildet, an denen keiner sein sollte. Diese schmerzhafte Erkrankung, bei der unerwünschtes Knochenwachstum in Weichteilen entsteht, kann Gelenke versteifen, Amputationen verkomplizieren und die alltägliche Bewegung erschweren. Die verfügbaren Behandlungen sind begrenzt und verhindern oft nicht, dass das Problem wiederkehrt. Diese Studie legt einen frühen Schalter im Immunsystem offen, der Trauma mit dieser abnormen Knochenbildung verknüpft — und weist auf ein kurzes, kritisches Zeitfenster hin, in dem gezielte Behandlung den Prozess stoppen könnte, bevor er beginnt. 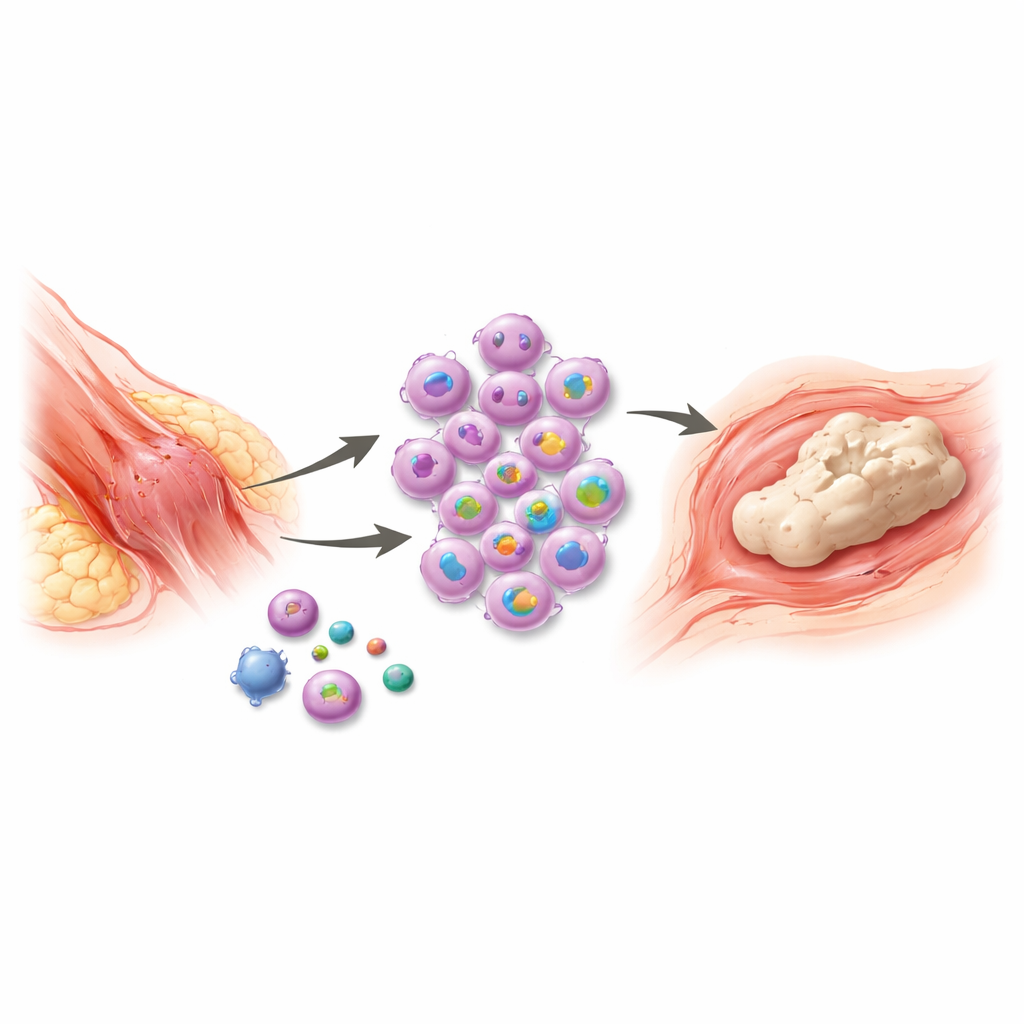
Das Problem: Knochen am falschen Ort
Nach schweren Traumata wie Verbrennungen, Frakturen oder orthopädischen Eingriffen entwickeln manche Patienten Inseln von Knochen innerhalb von Muskeln, Sehnen und anderen Weichteilen. Der neue Knochen entsteht durch einen Prozess, der der normalen Knochenentwicklung ähnelt, beginnend mit Entzündung und endend mit ausgereiftem, mineralisiertem Gewebe. Zwar ist bekannt, dass Immunzellen, sogenannte Makrophagen, zentral für diese Reaktion sind, doch die schrittweise Steuerung, wie sie Entzündungen auslösen und aufrechterhalten, war unklar. Ohne dieses Wissen behandeln Therapien wie Entzündungshemmer, Strahlentherapie oder späte operative Entfernung meist die Folgen und nicht die Ursache — Rückfälle sind deshalb häufig.
Der zentrale Vermittler der Entzündung
Mit einem Mausmodell, das Sehnenverletzung mit Verbrennung kombiniert und damit schwere Traumata beim Menschen gut nachahmt, verfolgten die Forschenden den Verlauf am Verletzungsort über die Zeit. Sie beobachteten einen raschen Anstieg von Makrophagen in den ersten Tagen nach der Verletzung, der dann bestehen blieb, während sich abnormer Knochen bildete. Wurden diese Zellen entfernt, verschwand der zusätzliche Knochen nahezu vollständig, und das umliegende Gewebe zeigte deutlich weniger Störungen von Blutgefäßen und Stützzellen. Eine tiefere Genanalyse des verletzten Gewebes hob ein Molekül in diesen Makrophagen besonders hervor: PRMT6, ein Enzym, das Proteine modifiziert und hilft zu steuern, welche Gene aktiviert werden.
Ein molekularer Lautstärkeregler für Entzündung
Das Team fand heraus, dass die PRMT6‑Spiegel in Makrophagen nach Verletzung und als Antwort auf Gefahren‑ oder bakterielle Signale im Labor schnell anstiegen. Mäuse ohne PRMT6 oder Tiere, bei denen PRMT6 selektiv nur in Makrophagen vermindert war, zeigten deutlich weniger Makrophagen an der Verletzungsstelle und entwickelten erheblich weniger abnormen Knochen. Wichtig ist: Die verletzten Sehnen dieser Tiere heilten tatsächlich besser, mit geordneterem Gewebe und weniger Narbenbildung. Das deutet darauf hin, dass PRMT6 für die gesunde Reparatur nicht erforderlich ist, sondern vielmehr als Lautstärkeregler wirkt, der schädliche Entzündungen verstärkt. Als die Forscher PRMT6 mit einem Medikament blockierten, wirkte dies nur, wenn es früh verabreicht wurde — in den ersten Wochen nach der Verletzung. Ein späterer Behandlungsbeginn zeigte kaum Wirkung und machte so ein schmales, aber wirkungsvolles therapeutisches Zeitfenster sichtbar. 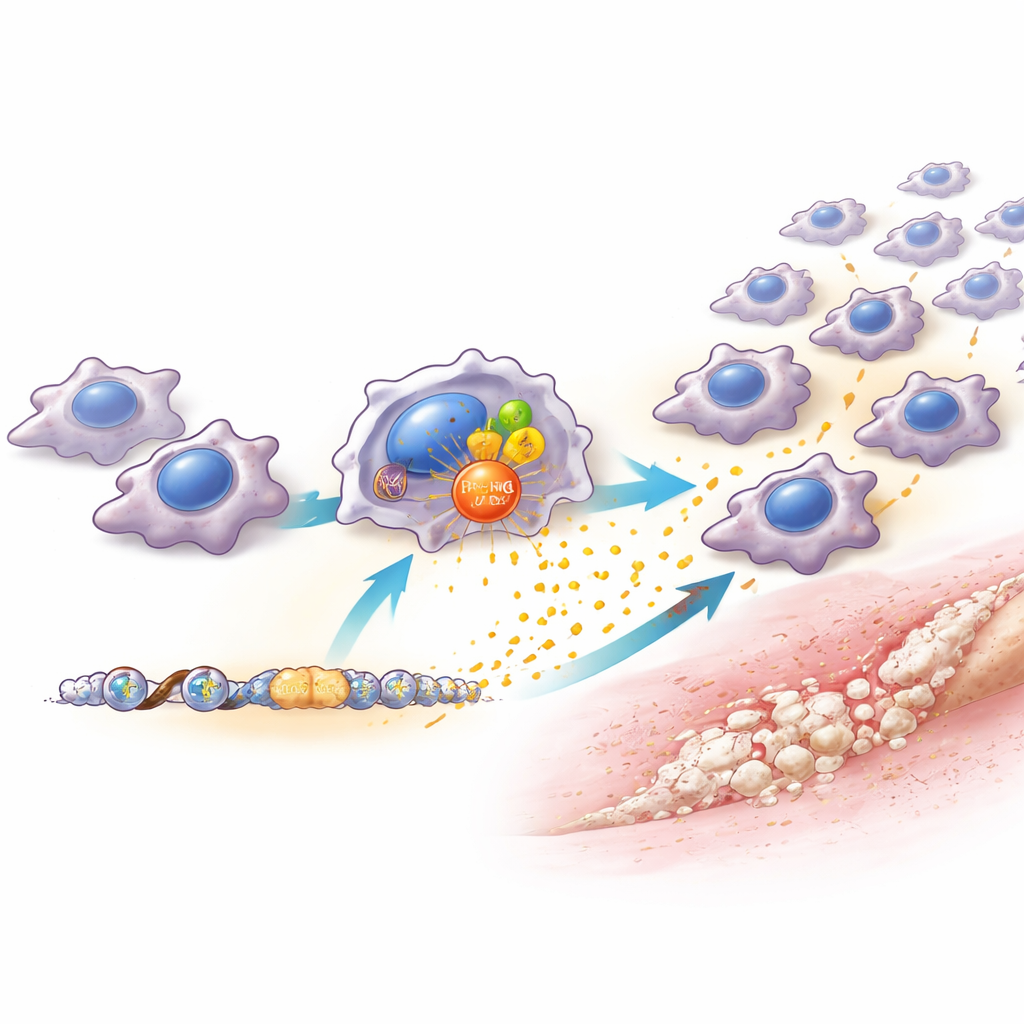
Wie ein Signal viele Immunzellen anzieht
Um zu verstehen, wie PRMT6 diese Wirkung ausübt, untersuchten die Wissenschaftler Makrophagen im Detail. Ohne PRMT6 produzierten diese Zellen deutlich geringere Mengen mehrerer chemischer Lockstoffe, besonders eines namens CCL2, das normalerweise mehr Monozyten und Makrophagen aus dem Blut in verletztes Gewebe zieht. PRMT6 hilft, das CCL2‑Gen auf zwei Wegen einzuschalten: Es arbeitet mit dem bekannten Entzündungsregler NF‑κB zusammen und markiert chemisch benachbarte DNA‑verpackende Proteine, sodass dieses Gen leichter abgelesen werden kann. In der Folge schütten Makrophagen mit hohem PRMT6 mehr CCL2 aus, ziehen zusätzliche Makrophagen an und bauen ein „Entzündungszentrum“ auf, das Blutgefäße und knochenbildende Vorläuferzellen fördert. Wurde CCL2 gezielt nur in Makrophagen reduziert, ähnelte das Ergebnis stark dem Verlust von PRMT6 — weniger Makrophagen, schwächere entzündliche Nischen und weniger zusätzlicher Knochen. Die Wiedergabe von CCL2 stellte den Makrophagen‑Zustrom und das abnorme Knochenwachstum teilweise wieder her.
Eine gezielte Chance, unerwünschten Knochen zu verhindern
Insgesamt zeigt die Studie, dass PRMT6 in Makrophagen als früher epigenetischer Verstärker wirkt: Es erhöht ein zentrales chemisches Signal, das mehr Immunzellen anzieht, die wiederum Knochenbildung an Orten vorantreiben, an denen sie nicht hingehört. Weil die Blockade von PRMT6 nur während der frühen Entzündungsphase das unerwünschte Knochenwachstum deutlich reduzierte und gleichzeitig die normale Sehnenheilung intakt ließ — ja sogar die Gewebeorganisation verbesserte — bietet dieser Signalweg eine vielversprechende neue Strategie. Grundsätzlich könnte ein kurzer, gut getimter Behandlungszyklus mit PRMT6‑gezielter Therapie nach schwerem Trauma oder Operation langfristige Behinderungen durch heterotope Ossifikation verhindern, ohne die natürliche Reparaturfähigkeit des Körpers zu beeinträchtigen.
Zitation: Chu, W., Peng, W., Wu, Z. et al. PRMT6 is required for initiating and amplifying macrophage-induced inflammation in heterotopic ossification by increasing CCL2 expression. Bone Res 14, 29 (2026). https://doi.org/10.1038/s41413-026-00512-w
Schlüsselwörter: heterotope Ossifikation, Makrophagen, Entzündung, epigenetische Regulation, CCL2‑Signalgebung