Clear Sky Science · de
C/EBPβ bestimmt die postmenopausale FSHβ-Transkription und die Blockade des AEP/C/EBPβ-Wegs lindert Osteoporose
Warum diese Forschung für das Leben nach der Menopause wichtig ist
Viele Frauen hören, dass der abfallende Östrogenspiegel der wichtigste Grund für brüchige Knochen nach der Menopause sei. Diese Studie fügt dem Bild ein neues Element hinzu: Ein anderes Hormon, das follikelstimulierende Hormon (FSH), und ein Proteinduo im Gehirn und Knochen—C/EBPβ und AEP—wirken zusammen und beschleunigen den Knochenverlust. Noch interessanter ist, dass die Forschenden an Mäusen zeigen, dass die Blockade dieses Wegs mit einer experimentellen Tablette die Knochen genauso wirksam schützen kann wie ein zugelassenes Osteoporosemedikament.
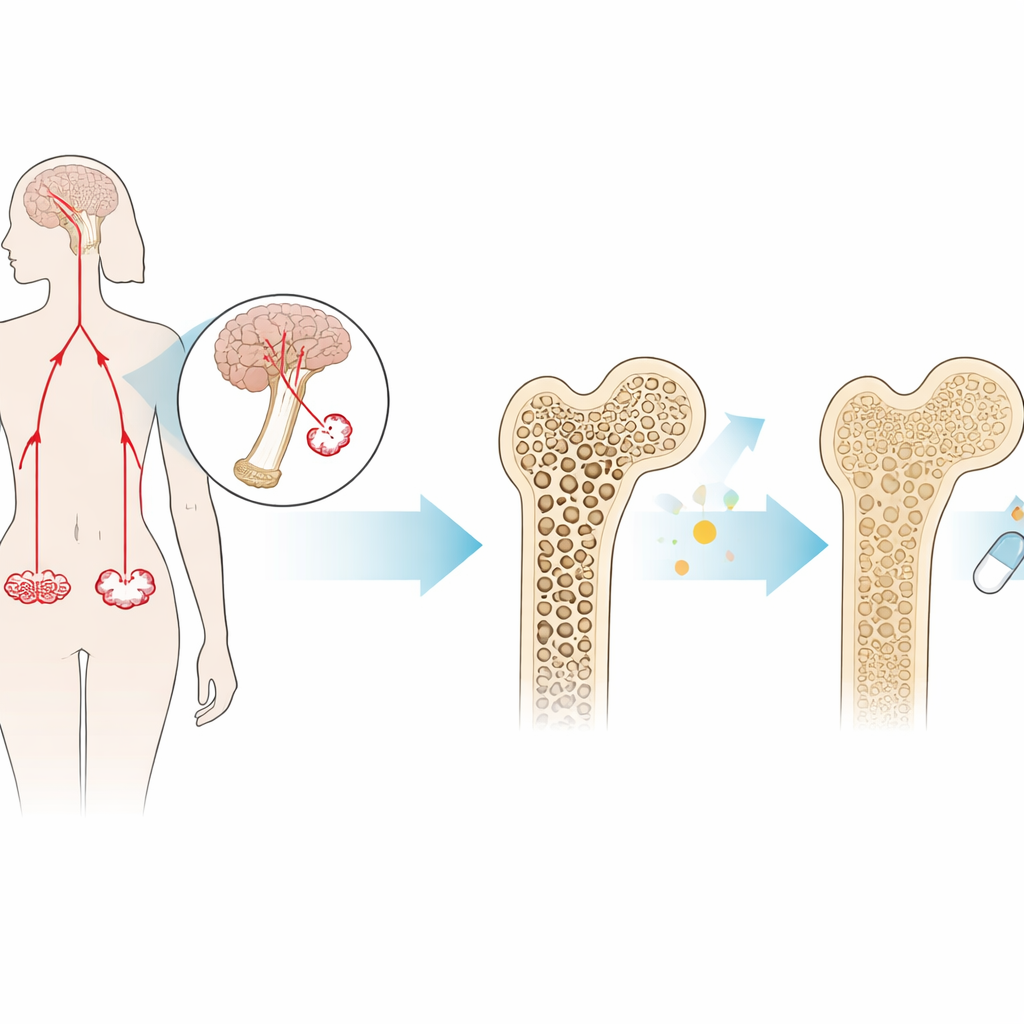
Ein weniger bekanntes Hormon mit großer Wirkung auf den Knochen
FSH wird in der Hypophyse gebildet und ist vor allem für seine Rolle bei der Fruchtbarkeit bekannt. Bei Frauen, die sich der Menopause nähern, steigt der FSH-Spiegel mehrere Jahre vor der letzten Menstruationsblutung stark an. Über seine reproduktive Funktion hinaus kann FSH direkt am Knochen wirken: Es bindet an Rezeptoren auf knochenabbauenden Zellen (Osteoklasten) und treibt diese dazu, Knochen schneller abzubauen, als er wieder aufgebaut wird. Frühere Arbeiten zeigten, dass Mäuse, denen FSH oder sein Rezeptor fehlen, vor Knochenverlust geschützt sind, selbst wenn ihr Östrogen niedrig ist. Das deutet darauf hin, dass FSH selbst und nicht nur Östrogenmangel die postmenopausale Osteoporose antreiben kann.
Der Steuerungsmechanismus in der Hypophyse
Die neue Studie konzentriert sich auf C/EBPβ, ein Protein, das an die DNA bindet und Gene an- oder ausschaltet. Die Autorinnen und Autoren entdeckten, dass C/EBPβ direkt an die Kontrollregion des Gens für die Beta-Untereinheit von FSH bindet—den Teil des Hormons, der seine Identität bestimmt—und dessen Produktion in der Hypophyse erhöht. In kultivierten Hypophysenzellen führte eine Erhöhung von C/EBPβ zu mehr FSH, während das Stilllegen von C/EBPβ FSH reduzierte, besonders wenn die Zellen durch das reproduktive Signal aus dem Gehirn, GnRH, stimuliert wurden. Bei ovariektomierten Mäusen, die durch Entfernen der östrogenproduzierenden Eierstöcke die Menopause nachahmen, produzierten Tiere mit reduziertem C/EBPβ deutlich weniger FSH in Hypophyse und Blut. Diese Experimente zeigen C/EBPβ als zentralen Schalter, der bestimmt, wie stark FSH nach dem Östrogenabfall ansteigt.
Eine sich selbst verstärkende Schleife und ein neues Wirkstoffziel
C/EBPβ steuert außerdem ein anderes Protein namens AEP, eine schneidende Enzymaktivität, die andere Moleküle aktivieren oder deaktivieren kann. Im Gehirn wurde eine C/EBPβ–AEP-Kette mit Alzheimer-ähnlichen Schäden in Verbindung gebracht. Die Forschenden fragten hier, ob dieselbe Kette rückkoppelt auf FSH und Knochen. Bei Mäusen ohne AEP fielen die Spiegel sowohl von C/EBPβ als auch von FSH in der Hypophyse, und der Knochenverlust nach Eierstockentfernung war reduziert. Die Blockade von AEP mit einem niedermolekularen Wirkstoff, genannt #11a, zeigte einen ähnlichen Effekt: Nach monatelanger Behandlung hatten ovariektomierte Mäuse niedrigere FSH-Werte, stärkere Knochen in hochauflösenden Scans und weniger überaktive knochenabbauende Zellen. Eine andere Wirkstoffklasse—TrkB-Aktivatoren, die AEP indirekt dämpfen—half zwar Knochenzellen in Kultur, konnte aber bei Tieren das FSH nicht senken, vor allem weil ihr Zielrezeptor in der Hypophyse kaum vorhanden ist. Dieser Gegensatz untermauerte die Schlussfolgerung, dass eine direkte Hemmung von AEP ein wirkungsvollerer Weg ist, die C/EBPβ–FSH-Achse an ihrer Quelle auszuschalten.
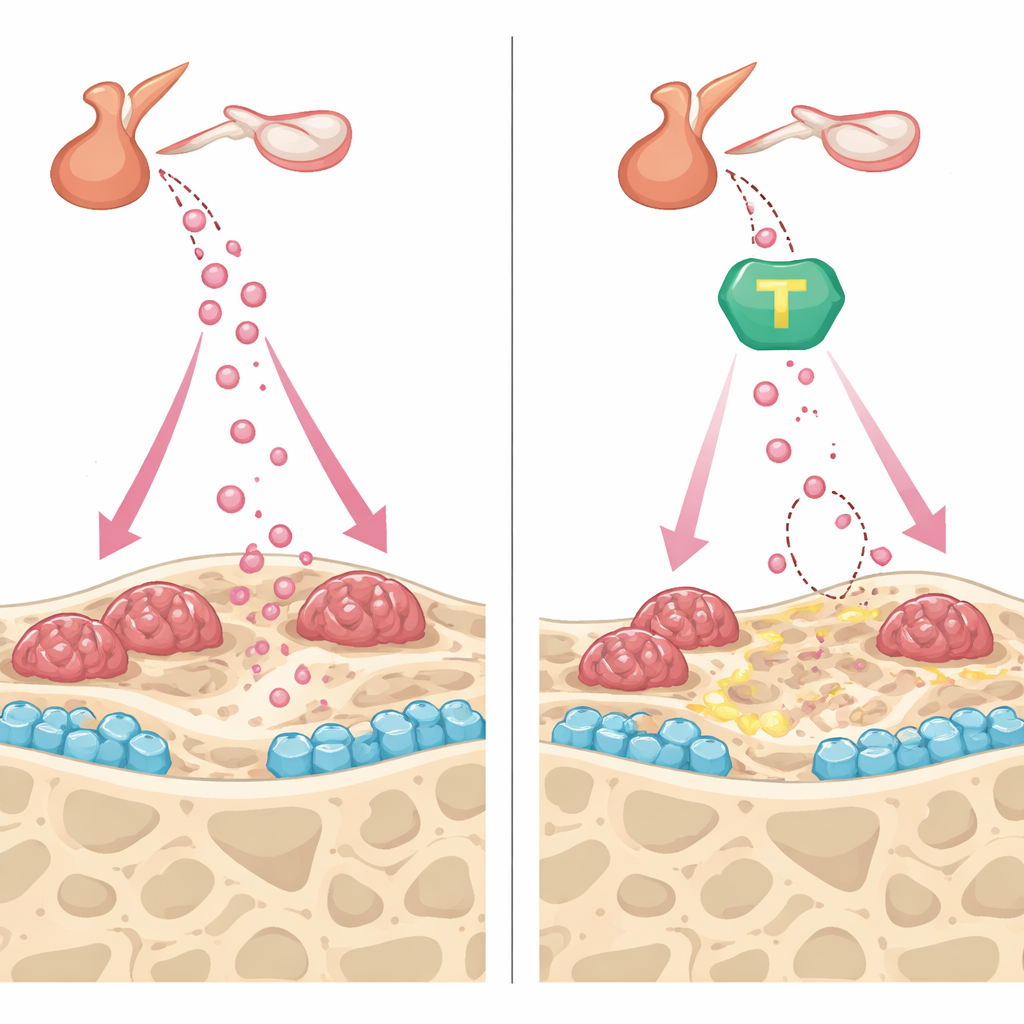
Den Knochen aus zwei Richtungen schützen
Über die Senkung von FSH hinaus zeigten #11a und der TrkB-Aktivator CF3CN komplementäre Vorteile direkt im Knochen. In Kulturen von knochenbildenden Zellen beschleunigten beide Verbindungen die Reifung und die Mineralablagerung, teilweise indem sie Fibronectin bewahrten—ein Strukturprotein, das AEP normalerweise zerschneidet—und indem sie pro-knochenbildende Signale wie Osteoprotegerin erhöhten. In knochenabbauenden Zellen dämpften die Wirkstoffe die Wirkung eines wichtigen Resorptionssignals, reduzierten die Anzahl großer, mehrkerniger Zellen und deren Fähigkeit, Gruben in Knochenscheiben zu ätzen. In lebenden Mäusen bremsten sowohl #11a als auch CF3CN den raschen Knochenumbau aus, der durch Eierstockentfernung ausgelöst wird, und stabilisierten Knochendichte und Mikroarchitektur. Auffällig war, dass die experimentelle Pille #11a im direkten Vergleich mit Teriparatid, einem von der FDA zugelassenen injizierbaren Aufbaupräparat, im Modell die Fähigkeit zeigte, Knochenvolumen und -stärke wiederherzustellen.
Was das für die zukünftige Osteoporosebehandlung bedeuten könnte
Für Nicht-Fachleute lautet die Kernbotschaft: Diese Arbeit identifiziert einen doppelten Weg, der menopausebedingte Entzündungsprozesse mit steigendem FSH und Knochen-schädigung verknüpft, und zeigt, dass die Zielrichtung AEP diese Kette unterbrechen kann. Bei Mäusen senkt ein oraler AEP-Inhibitor nicht nur das überschüssige FSH, das den Knochenabbau antreibt, sondern verschiebt auch direkt das Gleichgewicht im Knochen hin zu Aufbau statt Abbau. Während diese Befunde noch am Menschen geprüft werden müssen, deuten sie darauf hin, dass künftige Osteoporosebehandlungen über die bloße Östrogenersatz- oder Aufbaustimulation hinausgehen und stattdessen diesen neu kartierten hormonellen und enzymatischen Kreislauf beruhigen könnten, der die postmenopausale Knochenbrüchigkeit antreibt.
Zitation: Xie, Z., Liao, J., Xiong, J. et al. C/EBPβ dictates postmenopausal FSHβ transcription and blockade of AEP/C/EBPβ pathway alleviates osteoporosis. Bone Res 14, 31 (2026). https://doi.org/10.1038/s41413-026-00510-y
Schlüsselwörter: postmenopausale Osteoporose, follikelstimulierendes Hormon, C/EBPβ AEP-Weg, Knochenumbau, hormonzielgerichtete Therapie