Clear Sky Science · de
TGF-β-induzierte Bildung fibröser Narben begrenzt die Erholung nach Rückenmarksverletzung
Warum Narben im Rückenmark wichtig sind
Wenn das Rückenmark schwer verletzt wird, bleiben viele Menschen mit bleibender Lähmung oder Gefühlsverlust zurück, weil beschädigte Nervenfasern nicht wieder nachwachsen. Diese Studie stellt eine einfache, aber entscheidende Frage: Was blockiert genau dieses Nachwachsen – und kann die Barriere sicher entfernt werden? Indem die Autoren aufdecken, wie eine bestimmte Art von Narbe im Inneren des verletzten Markes entsteht, weisen sie auf einen neuen Weg, das Nervensystem bei der Selbstreparatur zu unterstützen.
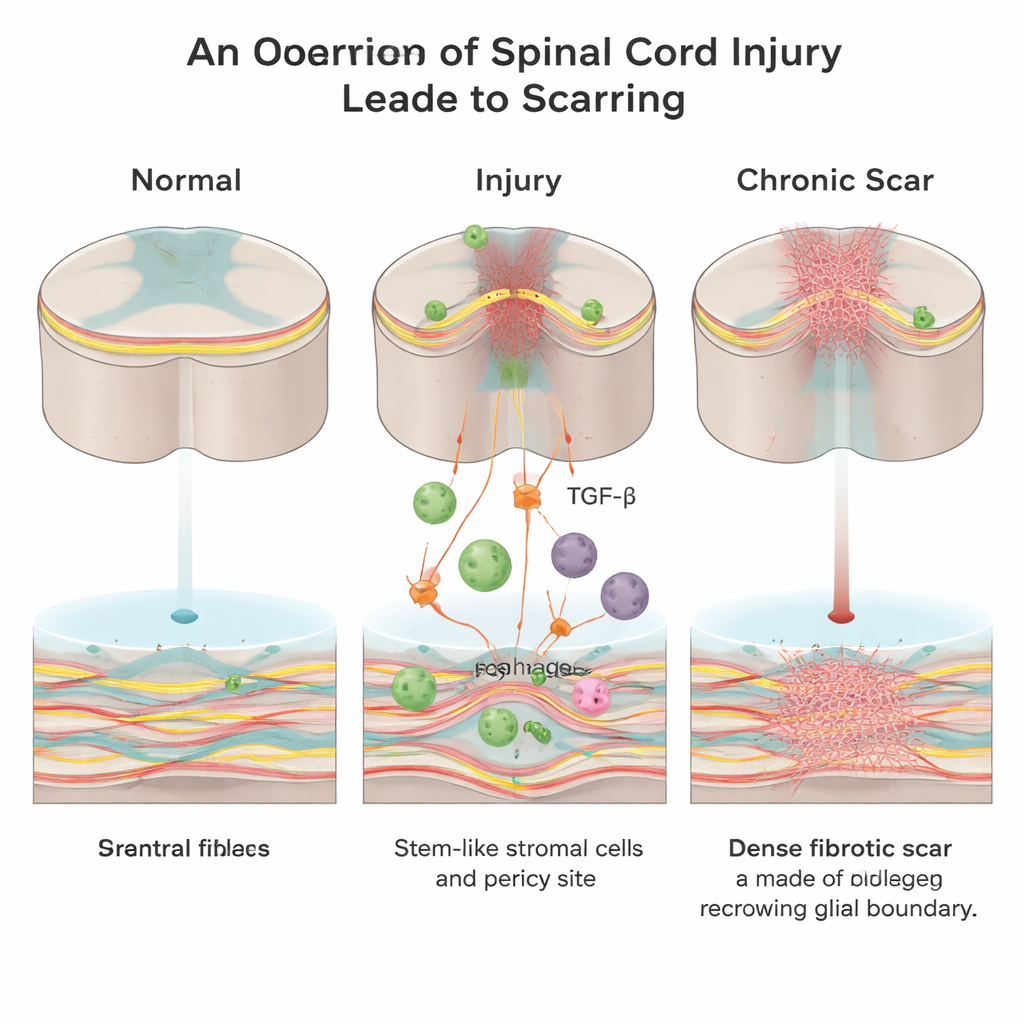
Eine verborgene Wand innerhalb der Verletzung
Nach einer Rückenmarksverletzung eilt der Körper herbei, um die Wunde zu verschließen. Es bilden sich zwei Haupttypen von Narbengewebe: eine „gliale“ Narbe, die von Stützzellen namens Astrozyten gebildet wird, und eine „fibröse“ Narbe, die reich an Kollagen, Fibronectin und Fibroblasten ist. Während die gliale Narbe schützende Funktionen haben kann, schafft die fibröse Narbe eine dichte physische und chemische Wand, die wachsende Nervenfasern nur schwer überwinden können. Bislang wussten Wissenschaftler deutlich weniger darüber, wie dieser fibröse Kern entsteht und welche Signale seine Bildung antreiben.
Die Rolle von Immunzellen und ein kraftvolles Signal
Die Forscher arbeiteten mit erwachsenen Mäusen und konzentrierten sich auf ein Signalmolekül namens Transforming Growth Factor‑beta (TGF‑β), das die Wundheilung im Körper koordiniert und bei fibrotischen Erkrankungen häufig überaktiv ist. Sie stellten fest, dass nach einer Rückenmarksverletzung eindringende Immunzellen, sogenannte Makrophagen, eine wichtige Quelle aktiven TGF‑β1 an der Läsionsstelle werden. Dieser Anstieg an TGF‑β1 rekrutiert lokale mesenchymale Stromal-/Stammzellen und gefäßassoziierte Zellen namens Perizyten und treibt sie dazu, sich in Fibroblasten zu verwandeln – genau die Zellen, die die kollagenreiche fibröse Narbe ablagern.
Das Signal dämpfen, um einen Weg zu öffnen
Um zu prüfen, ob dieser Weg tatsächlich schädliche Narbenbildung verursacht, nutzte das Team mehrere genetische Methoden in Mäusen. Wenn sie Makrophagen entfernten oder das TGF‑β1-Gen nur in Makrophagen‑Linienzellen löschten, nahm das Ausmaß des fibrösen Gewebes im verletzten Rückenmark deutlich ab, und mehr Nervenfasern sowie serotoninerge Bahnen konnten die Verletzungszone durchqueren. Ebenso führte die gezielte Deletion des TGF‑β-Rezeptors in Perizyten zu einer verminderten Reaktion auf TGF‑β, weniger Kollagenablagerung und verbesserten Bewegungs- und Empfindungsergebnissen in Verhaltenstests. Wichtig war, dass Perizyten und verwandte stammzellähnliche Zellen weiterhin vorhanden waren, aber weniger wahrscheinlich zu narbenbildenden Fibroblasten wurden.
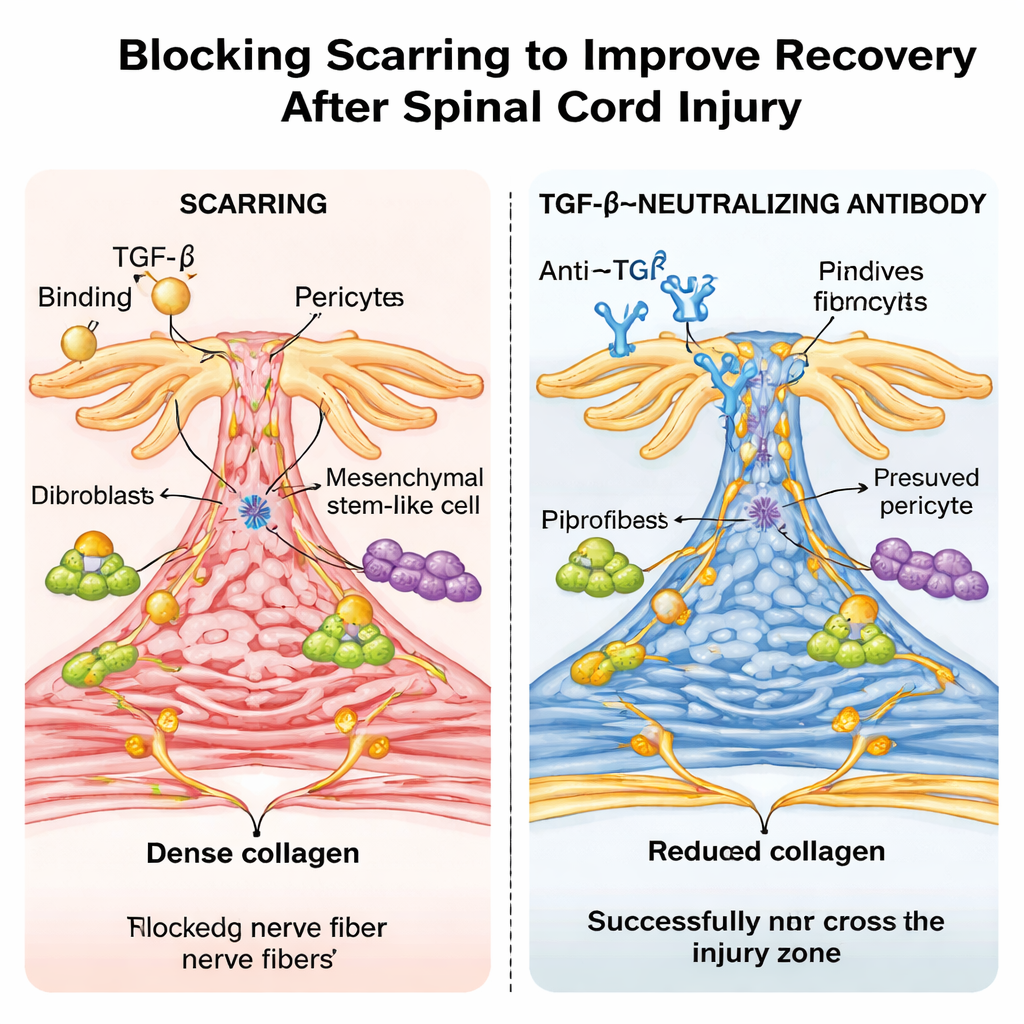
Ein medikamentartiger Antikörper und ein überraschender Alterseffekt
Die Forscher versuchten dann einen klinisch relevanteren Ansatz: normale Mäuse wurden mit einem Laborantikörper behandelt, der TGF‑β neutralisiert. Wiederholte Gaben nach der Verletzung senkten die aktiven TGF‑β-Werte im Blut und Rückenmark, verkleinerten die fibröse Narbe und ermöglichten es Nervenfasern, die Läsion effektiver zu überbrücken, mit deutlichen Verbesserungen bei Geh- und Sensorikfunktionen. Einzelzell-RNA-Sequenzierung bestätigte, dass TGF‑β-ansprechende Gene in narbenbildenden Zelltypen unbehandelter Mäuse sehr aktiv waren und durch den Antikörper gedämpft wurden. Auffällig war, dass bei gleicher Rückenmarksquetschung in neugeborenen Mäusen die Tiere nahezu ohne fibröse Narben heilten, keine nachweisbare TGF‑β-Aktivierung an der Verletzungsstelle zeigten und nahezu normale Bewegungsfähigkeiten wiedererlangten – ähnlich der narbenfreien Reparatur, die bei manchen nicht‑säugetierischen Tieren beobachtet wird.
Was das für zukünftige Behandlungen bedeuten könnte
Insgesamt deuten die Befunde darauf hin, dass eine übermäßige Aktivierung von TGF‑β nach einer Rückenmarksverletzung hilfreiche Reparaturzellen in den Bau einer starren fibrösen Wand umleitet, die das Nervenwachstum und die funktionelle Erholung blockiert. Indem man diese Überaktivierung verhindert – entweder durch gezielte Verringerung der TGF‑β-Produktion in Makrophagen, Blockade seines Rezeptors auf Perizyten und Stromazellen oder durch Einsatz eines neutralisierenden Antikörpers – könnte es möglich sein, die schädliche Narbe zu reduzieren und gleichzeitig günstigere Gewebereaktionen zu erhalten oder sogar zu fördern. Obwohl die Übertragung dieser Strategien auf den Menschen sorgfältige Studien erfordert, um Nebenwirkungen zu vermeiden, hebt diese Arbeit die TGF‑β-getriebene fibröse Narbenbildung als zentrale und potenziell medikamentös angreifbare Barriere für die Reparatur des Rückenmarks hervor.
Zitation: Pan, D., Wu, P., Noller, K. et al. TGF-β-induced fibrotic scar formation limits recovery of spinal cord injury. Bone Res 14, 27 (2026). https://doi.org/10.1038/s41413-026-00507-7
Schlüsselwörter: Rückenmarksverletzung, fibröse Narbe, TGF-beta, Makrophagen, Nervenerneuerung