Clear Sky Science · de
HIF-1α und BMAL1 in der Knochenregeneration: Wechselspiel zwischen Hypoxieantwort und circadianem Rhythmus
Warum gebrochene Knochen besser heilen, als Sie denken
Wenn wir einen Knochen brechen oder einen Zahn gezogen bekommen, startet unser Körper still und koordiniert ein überraschend gut organisiertes Reparaturprogramm. Tief in der verletzten Region sinkt der Sauerstoffgehalt und unsere innere Tages‑Nacht‑Uhr läuft weiter. Dieser Artikel untersucht, wie zwei Schaltzentralen – HIF‑1α, der Niedrigsauerstoff wahrnimmt, und BMAL1, ein zentrales Uhrprotein – zusammenarbeiten, um Knochenzellen durch Entzündung, Neubildung von Gewebe und die Wiederherstellung der finalen Festigkeit zu führen. Das Verständnis dieser Partnerschaft könnte Behandlungen von Frakturen, Osteoporose, Arthritis und sogar Zahnersatz verbessern.
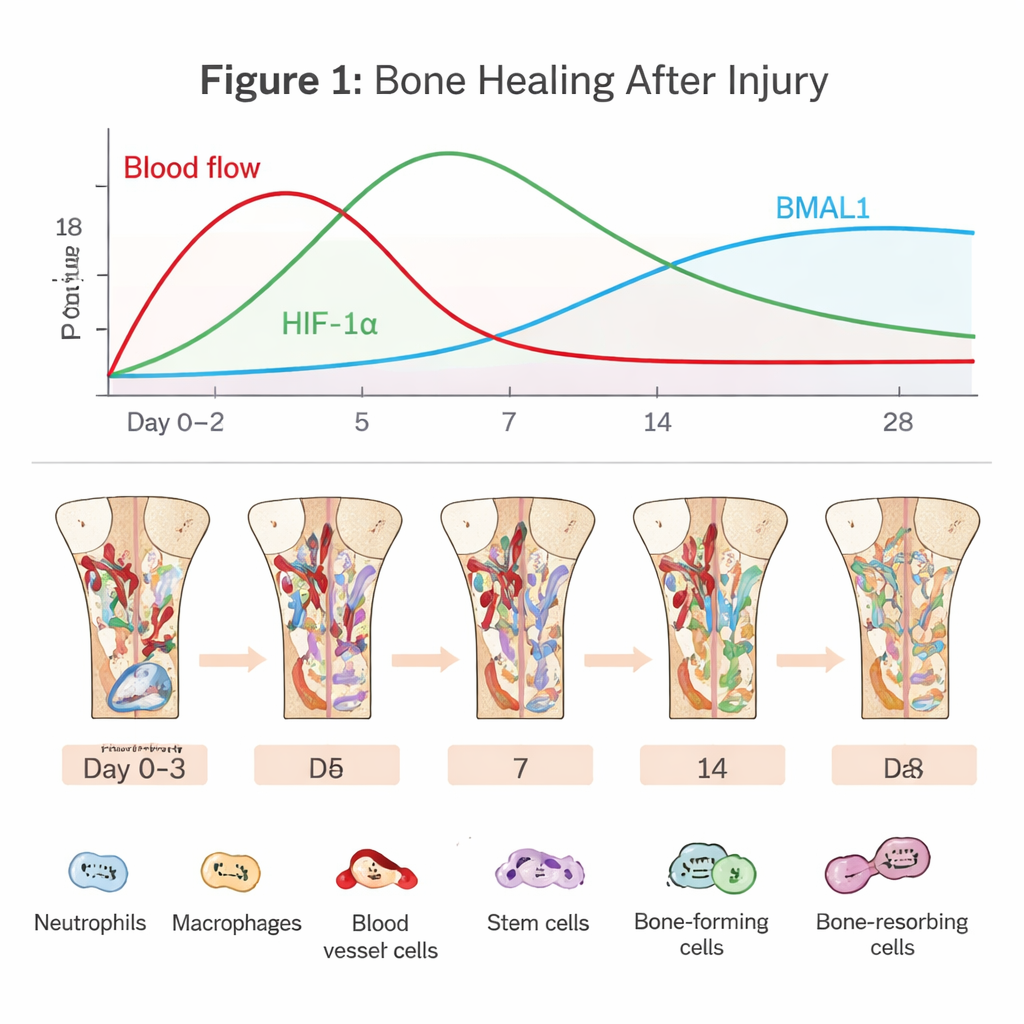
Das verborgene Drama in einem heilenden Knochen
Knochenregeneration beginnt in dem Moment, in dem Blutgefäße reißen. Ein Blutgerinnsel bildet sich, unterbricht die Sauerstoffversorgung weitgehend und schafft eine raue, sauerstoffarme Nische. Immunzellen wie Neutrophile und Makrophagen stürmen herbei, um Trümmer zu beseitigen und Mikroben abzuwehren. Gleichzeitig werden Knochenmarkstammzellen und Gefäßzellen rekrutiert, um die Stelle wieder aufzubauen. Diese frühe „entzündliche Phase“ ist ein zweischneidiges Schwert: Ein kurzer, gut getakteter Entzündungsschub startet die Reparatur, hält er jedoch zu lange oder ist zu heftig, kann die Heilung ins Stocken geraten oder scheitern. Der Artikel betont, dass das Navigieren dieses schmalen Pfades stark davon abhängt, wie Zellen Sauerstoff und Zeit wahrnehmen.
Wie Zellen Niedrigsauerstoff zu ihrem Vorteil nutzen
In der sauerstoffarmen Frakturzonen stabilisiert sich das Protein HIF‑1α und schaltet Gene an, die Zellen bei der Anpassung helfen. Es treibt Endothelzellen dazu, neue Blutgefäße auszutreiben, sodass frischer Sauerstoff und Nährstoffe die Defektzone erreichen. Zudem programmiert es den zellulären Stoffwechsel in Richtung Glykolyse um, eine Energiegewinnungsweise, die auch bei Sauerstoffmangel funktioniert. Für Stammzellen und knochenbildende Osteoblasten kann eine moderate Aktivierung von HIF‑1α Proliferation, Migration und Knochenwachstum fördern, unter anderem durch die Steigerung von Faktoren wie VEGF, die Gefäßneubildung mit Knochenbildung verknüpfen. Ist die Hypoxie jedoch zu stark oder zu langanhaltend, akkumulieren Stressmoleküle und reaktive Sauerstoffspezies, was Osteoblasten zugrunde richten und knochenabbauende Osteoklasten stimulieren kann. Dasselbe hypoxische Signal kann daher je nach Intensität und Dauer entweder die Heilung unterstützen oder sabotieren.
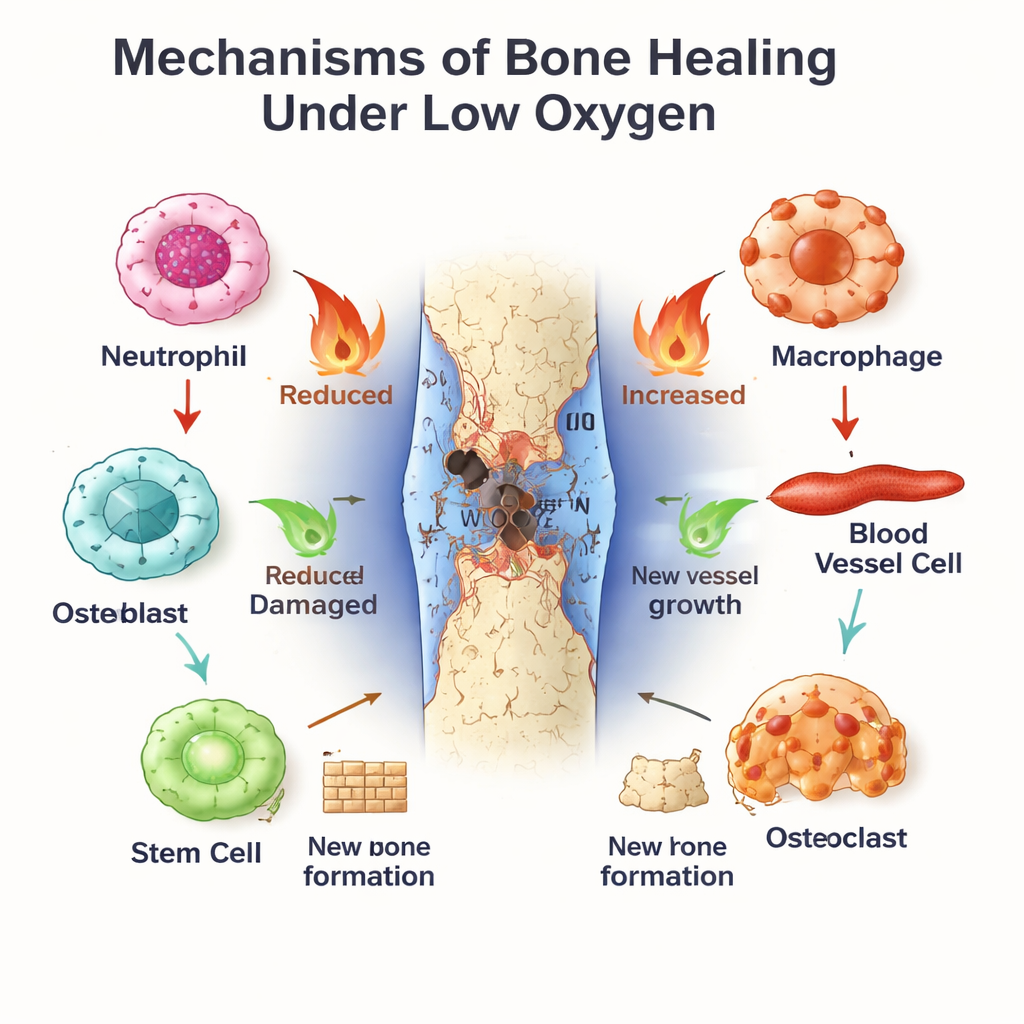
Die innere Uhr des Körpers als Manager der Knochenreparatur
Parallel dazu läuft die circadiane Uhr, ein molekularer Zeitgeber, der in nahezu jeder Zelle vorhanden ist. BMAL1, eines ihrer zentralen Komponenten, hilft dabei, tägliche Rhythmen in der Immunaktivität, dem Verhalten von Blutgefäßen und der Differenzierung von Stammzellen zu setzen. Neutrophile und Makrophagen zeigen tageszeitabhängige Unterschiede darin, wie stark sie auf Verletzungen reagieren und wie schnell sie altern oder vom entzündlichen (M1‑ähnlichen) in den heilenden (M2‑ähnlichen) Zustand wechseln. In Gefäßzellen und Knochenmarkstammzellen fördert BMAL1 gesunde Proliferation und geordnete Knochenbildung, unter anderem indem es Wachstumswege wie Wnt und TGF‑β/SMAD feinjustiert. Ist BMAL1 gestört – durch Gendefekte, Schichtarbeit oder Stoffwechselerkrankungen – neigen Knochen dazu, Masse zu verlieren, Stammzellen erschöpfen und das Gleichgewicht zwischen Knochenaufbau und -abbau verschiebt sich zugunsten des Verlusts.
Ein Dialog zwischen Sauerstoffwahrnehmung und Körperuhr
Im Zentrum des Reviews steht das entstehende „Crosstalk“ zwischen HIF‑1α und BMAL1. Diese beiden Proteine teilen ähnliche Strukturelemente und können physisch interagieren, sogar Mischpaare bilden, die an DNA binden und überlappende Gensätze kontrollieren. Jeder kann die Produktion und Stabilität des anderen beeinflussen und so Rückkopplungsschleifen schaffen, die die Tages‑Nacht‑Taktung mit der Hypoxieantwort der Zellen verknüpfen. Gemeinsam steuern sie auch das zelluläre Redoxgleichgewicht – wie viele schädliche reaktive Sauerstoffspezies produziert werden gegenüber der verfügbaren antioxidativen Kapazität – und sie ko‑regulieren Schlüsselenzyme, die entscheiden, ob Zellen mehr auf sauerstoffabhängige Atmung oder auf sauerstofffreie Glykolyse setzen. Diese gemeinsame Kontrolle trägt entscheidend dazu bei, ob die Frakturumgebung konstruktiven Wiederaufbau oder übermäßige Entzündung und Knochenabbau fördert.
Was das für Erkrankungen und Therapien bedeutet
Die gleiche HIF‑1α–BMAL1‑Partnerschaft zeigt sich in vielen knochenbezogenen Erkrankungen. Bei Schichtarbeitern verändern gestörter Schlaf und Lichtbelastung wahrscheinlich BMAL1, erhöhen oxidativen Stress und stören die HIF‑1α‑gesteuerte Reparatur, was zur Osteoporose beitragen kann. Bei Diabetes schwächt hoher Blutzucker sowohl die Uhrenfunktion als auch die Hypoxie‑Signalgebung, untergräbt die Gefäßneubildung und die stammzellgetriebene Knochenbildung. Bei Arthrose stört der Verlust von BMAL1 in Knorpelzellen deren Rhythmus und ihre schützende Beziehung zu HIF‑1α, was den Knorpelabbau beschleunigt. Rund um Titanimplantate scheinen kontrollierte Hypoxie und ein gesunder circadianer Rhythmus eine bessere Osseointegration zu unterstützen, was nahelegt, dass zukünftige Implantatbeschichtungen so gestaltet werden könnten, dass sie HIF‑1α und BMAL1 sanft aktivieren. Insgesamt kommt der Artikel zu dem Schluss, dass erfolgreiche Knochenregeneration nicht nur davon abhängt, welche Zellen vorhanden sind, sondern davon, wie sie Sauerstoff und Zeit lesen – und dass die gezielte Ansprache dieses Dialogs neue Wege zu schnellerer, stabilerer Heilung eröffnen könnte.
Zitation: Weng, Y., Xiong, J., Zhao, Q. et al. HIF-1α and BMAL1 in bone regeneration: crosstalk between hypoxia response and circadian rhythm. Bone Res 14, 25 (2026). https://doi.org/10.1038/s41413-026-00506-8
Schlüsselwörter: Knochenregeneration, circadianer Rhythmus, Hypoxie, Osteoporose, Frakturheilung