Clear Sky Science · de
Intelligente Biomaterialien zur Reparatur und Regeneration des altersbedingten Skeletts
Stärkere Knochen in einer alternden Welt
Viele Menschen erwarten mit dem Älterwerden schwächere Knochen und Gelenkschmerzen als unvermeidliche Begleiterscheinungen. Wissenschaftler entwickeln jedoch inzwischen „intelligente“ Materialien, die erkennen können, wann und wo Knochen versagen, und dann deren Selbstheilung unterstützen. Diese Materialien zielen darauf ab, Frakturen zuverlässiger zu reparieren, Osteoporose und Arthrose zu verlangsamen oder umzukehren und die Notwendigkeit wiederholter Operationen zu reduzieren – und älteren Menschen so bessere Chancen zu geben, aktiv und selbstständig zu bleiben.
Wie Knochen altern und warum sie leichter brechen
Knochen sind lebendes Gewebe, das sich ständig erneuert, doch mit dem Alter gerät dieses Gleichgewicht aus dem Takt. Stammzellen im Knochenmark verlagern sich von der Bildung knochenbildender Zellen hin zu Fettzellen; knochenaufbauende Zellen ermüden und knochenabbauende Zellen werden überaktiv. Die stützende Matrix aus Kollagen und Mineralien wird trockener und spröder, und das mikroskopische „Gerüst“ dünnt aus. Hormonelle Veränderungen, chronische niedriggradige Entzündungen, überschüssige reaktive Sauerstoffmoleküle und ein lokal saures Milieu setzen zusätzlich unter Druck. Außen sichtbar äußert sich das in dünnerem, poröserem Knochen, steiferen Gelenken, gekrümmter Wirbelsäule und einem erhöhten Risiko für Brüche sowie Erkrankungen wie Osteoporose und Arthrose.
Warum aktuelle Behandlungen nicht ausreichen
Die heutigen Hauptbehandlungen umfassen Medikamente, die Knochenverlust verlangsamen oder Knochenaufbau stimulieren, sowie Operationen und Metall- oder Keramikimplantate zur Stabilisierung von Frakturen oder zum Ersatz beschädigter Gelenke. Diese Ansätze haben vielen Menschen geholfen, tragen aber erhebliche Nachteile. Systemisch verabreichte Medikamente erreichen oft nur einen winzigen Bruchteil des Knochengewebes und können Nebenwirkungen wie Kieferprobleme, Blutgerinnsel oder bei langfristiger Anwendung sogar ein erhöhtes Krebsrisiko verursachen. Stammzelltherapien zeigen im Tierversuch Potenzial, stehen aber vor Herausforderungen wie Überleben der Zellen, unvorhersehbarem Verhalten und möglicher Tumorbildung. Konventionelle Implantate bieten zwar Stabilität, sind aber „dumm“: Sie nehmen ihre Umgebung nicht wahr, können die Wirkstofffreisetzung nicht anpassen und können in fragiler, alter Knochenstruktur versagen.
Intelligente Wirkstoffträger, die den Körper patrouillieren
Intelligente Biomaterialien bringen eine Art Intelligenz ins Spiel. Eine wichtige Strategie ist die systemische „smarte Abgabe“ von Medikamenten mittels Nanopartikeln oder weichen Gelen, die im Blutkreislauf zirkulieren und nur an Problemstellen aktiviert werden. Diese Träger lassen sich so konstruieren, dass sie auf interne Signale wie Säure, hohe Mengen schädlicher Sauerstoffspezies oder knochenabbauende Enzyme reagieren – oder auf externe Reize wie Licht, Ultraschall, Wärme oder magnetische Felder. Manche Partikel bleiben in normalem Gewebe intakt, öffnen sich aber und setzen ihre Arzneistofffracht in sauren, enzymreichen Bereichen frei, in denen überaktive Osteoklasten Knochen abbauen. Andere neutralisieren überschüssige reaktive Sauerstoffmoleküle und geben gleichzeitig langsam ein entzündungshemmendes Medikament frei oder tragen Kontrastfarbstoffe, damit Ärzte ihren Weg in Echtzeit verfolgen können. Durch die Kombination mehrerer Auslöser – etwa pH-Wert und Oxidantien – können Forschende die Zielgenauigkeit erhöhen und Nebenwirkungen reduzieren.
Lokale Gerüste, die wie temporäre intelligente Knochen wirken
Bei großen Defekten oder komplexen Frakturen älterer Knochen können lokale „intelligente Gerüste“ direkt in die Lücke implantiert werden. Diese 3D-Strukturen aus Metallen, Keramiken, Polymeren oder deren Kombinationen sind so konstruiert, dass sie Festigkeit, Porosität und Flexibilität des Knochens nachahmen. Ihre schwammartige Architektur ermöglicht das Einwachsen von Blutgefäßen und neuem Knochen, während das Material allmählich aufgelöst und durch das Gewebe des Patienten ersetzt wird. 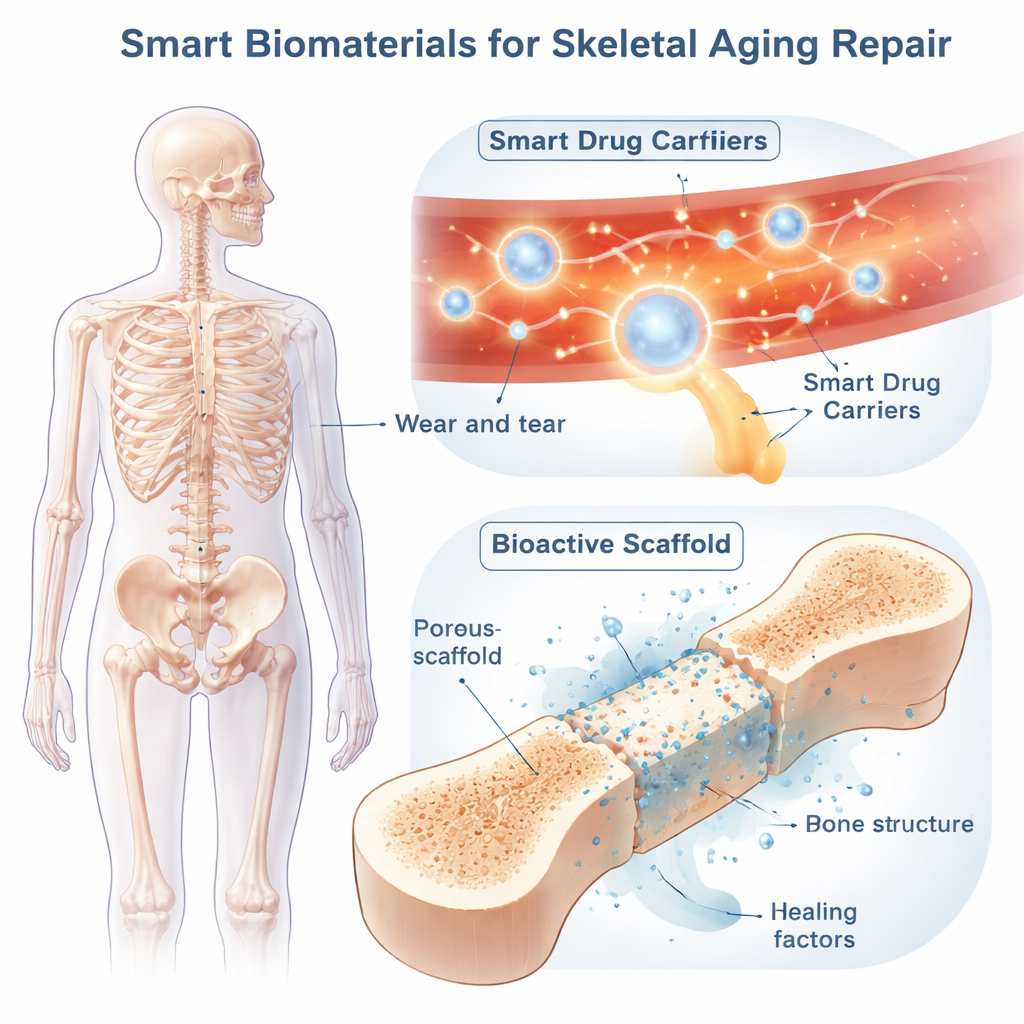
Aus dem Labor in die Klinik: Werkzeuge, Hürden und Zukunftsperspektiven
Zur Herstellung dieser komplexen Systeme nutzen Wissenschaftler fortschrittliche Fertigungsverfahren wie 3D-Druck und additive Fertigung, um Porengröße, Steifigkeit und Wirkstoffbeladung präzise einzustellen. Dennoch ist der Übergang intelligenter Biomaterialien in die Routinebehandlung anspruchsvoll. Die meisten injizierten Partikel reichern sich noch in Organen wie Leber und Milz an statt im Knochen, und viele Tiermodelle erfassen nicht die Komplexität altersbedingter Veränderungen beim Menschen. Großserienproduktion, Qualitätskontrolle, regulatorische Zulassung und Kosten bleiben große Hürden. Forscher sehen Hoffnung in der Kombination intelligenter Materialien mit künstlicher Intelligenz, um Gerüstdesign und Wirkstoffdosierung zu personalisieren, sowie in eingebauten Sensoren, die die Heilung verfolgen und Therapie in einem „Closed-Loop“-Verfahren automatisch anpassen können. 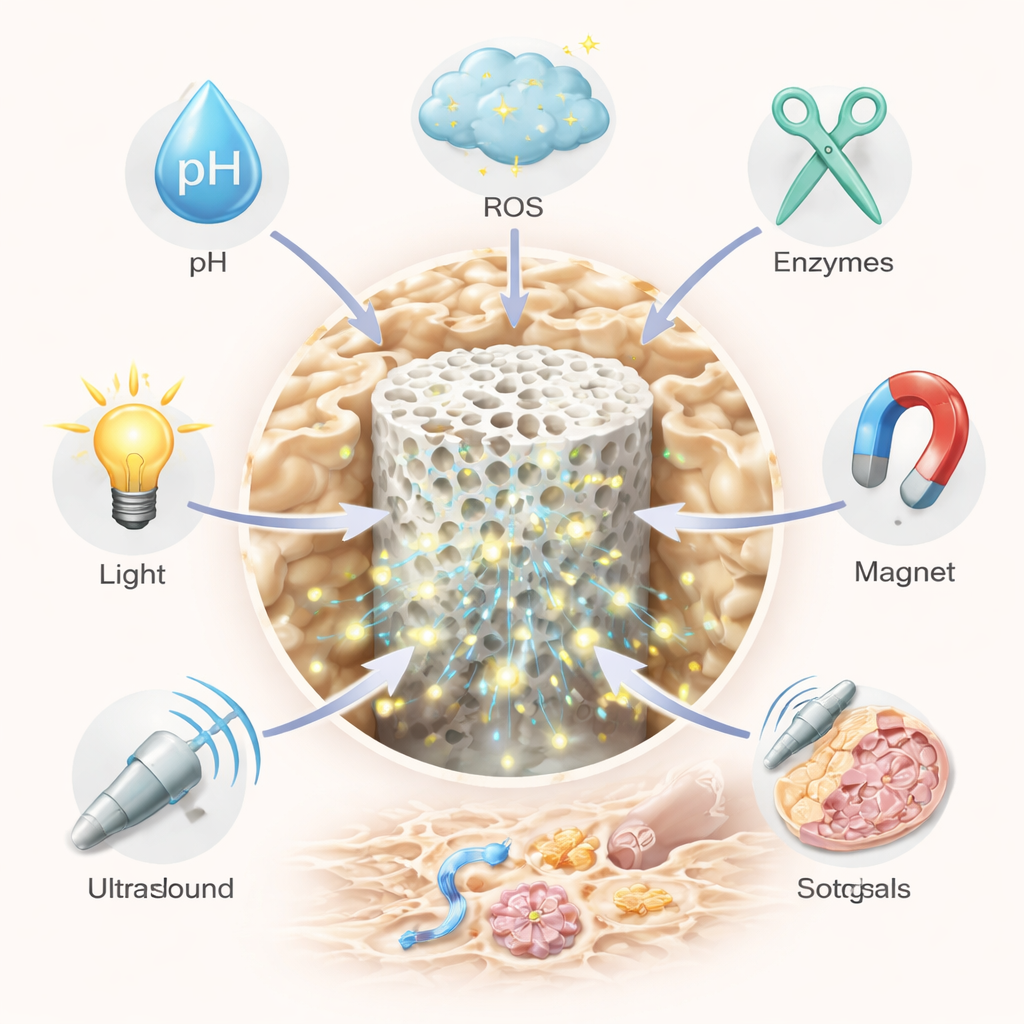
Was das für Patientinnen und Patienten bedeuten könnte
Im Kern zeigt diese Forschung, dass Knochenschwäche im Alter kein unvermeidlicher, einseitiger Abstieg sein muss, sondern ein komplexes ingenieurwissenschaftliches Problem, das lösbar erscheinen kann. Intelligente Biomaterialien wirken wie winzige, programmierbare Reparaturcrews: Sie patrouillieren im Blut, siedeln sich an geschädigten Stellen an und geben genau das frei, was nötig ist, genau dann, wenn es nötig ist, um Knochenstruktur und -funktion wiederherzustellen. Obwohl diese Technologien noch überwiegend in der Forschungsphase sind, deuten sie auf eine Zukunft hin, in der Frakturen schneller heilen, Implantate länger halten und Therapien auf die individuelle Knochenbiologie jeder Person zugeschnitten sind – sodass mehr Menschen bis ins hohe Alter mobil und selbstständig bleiben können.
Zitation: Liang, D., Wang, H., Jiang, Y. et al. Smart biomaterials for skeletal aging repair and regeneration. Bone Res 14, 24 (2026). https://doi.org/10.1038/s41413-026-00505-9
Schlüsselwörter: intelligente Biomaterialien, Skelettalterung, Knochenregeneration, Osteoporose, stimuli-responsive Gerüste