Clear Sky Science · de
Entzündungsfördernde synoviale Makrophagen‑abgeleitete extrazelluläre Vesikel verschlimmern Knorpelschäden auf FMRP‑selektive Weise bei Arthrose
Warum Gelenkentzündung bei schmerzenden Knien wichtig ist
Viele Menschen verstehen Arthrose als einfachen „Verschleiß“ alternder Gelenke, doch wachsende Evidenz zeigt, dass eine niedriggradige Entzündung im Gelenk die Erkrankung still vorantreiben kann. Diese Studie stellt eine gezielte Frage: Wie kommunizieren Immunzellen in der Gelenkinnenhaut mit Knorpelzellen, und lässt sich dieses Gespräch unterbrechen, um Gelenke zu schützen? Die Antworten enthüllen ein winziges molekulares Botenstoffsystem, das Schäden verschärft — aber auch neue Wege zur Diagnose und Behandlung der Arthrose eröffnet.
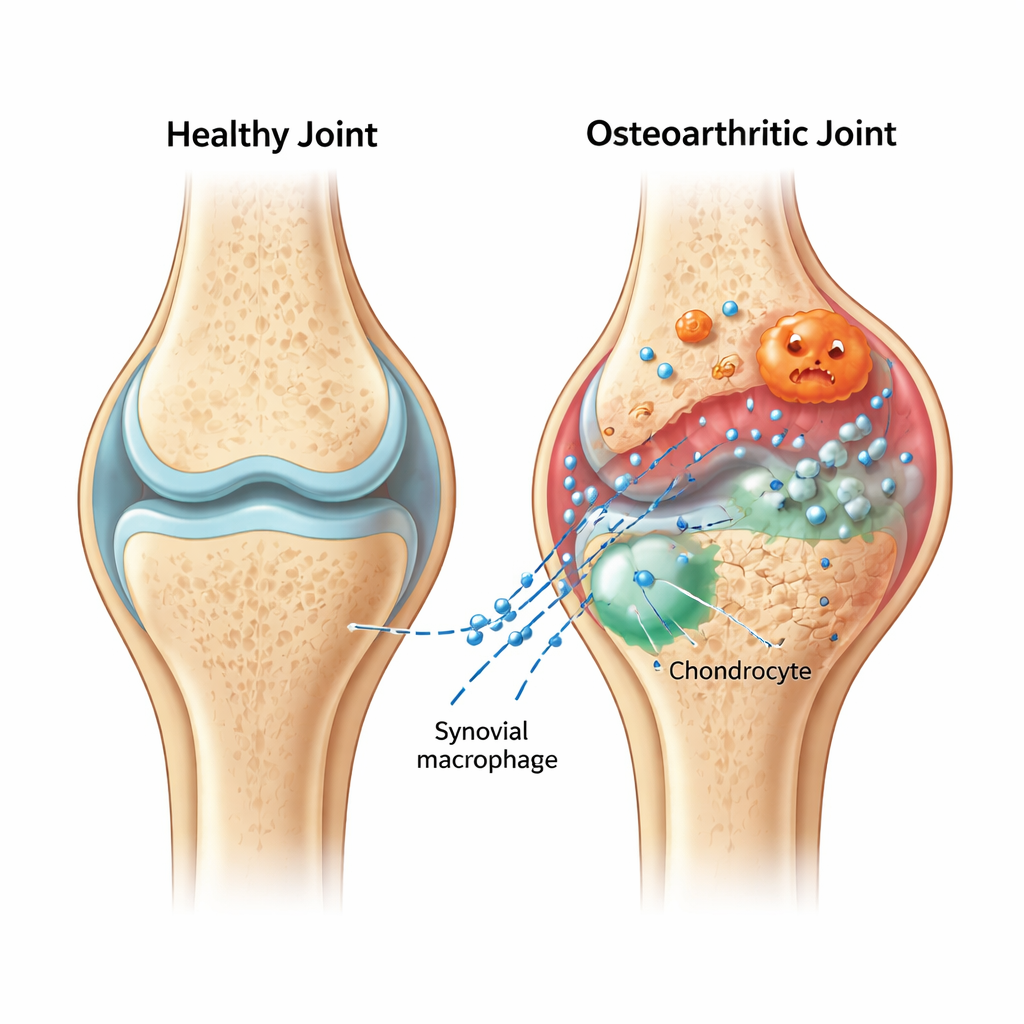
Kleine Pakete, die schlechte Nachrichten transportieren
Im arthritischen Knie entzündet sich die weiche Synovialmembran und füllt sich mit Immunzellen, den Makrophagen. Die Autorinnen und Autoren konzentrierten sich auf die „heißblütige“ Variante dieser Zellen — proinflammatorische Makrophagen — und auf die mikroskopischen Bläschen, die sie freisetzen, die sogenannten extrazellulären Vesikel. Diese Vesikel wirken wie versiegelte Pakete, die Moleküle zwischen Zellen transportieren. In Ratten mit chirurgisch induzierter Arthrose zeigten die Forschenden, dass Vesikel aus entzündeten Makrophagen zum Knorpel wandern und die Schäden verschlimmern: die normalerweise glatte, polsternde Oberfläche wurde rauer und dünner, wichtige Knorpelproteine nahmen ab, während Spaltungsenzyme zunahmen.
Wie Entzündung die Knorpel‑Selbstreinigung abschaltet
Knorpelzellen, oder Chondrozyten, sind auf einen Reinigungsprozess namens Autophagie angewiesen, um abgenutzte Komponenten zu recyceln und langfristig gesund zu bleiben. Als die Forschenden Gene verglichen, die in Knorpel nach Exposition gegenüber entzündlichen Vesikeln gegenüber einer harmlosen Kochsalzlösung aktiviert waren, zeigten sich deutliche Anzeichen für eine Unterdrückung der Autophagiewege. Unter dem Elektronenmikroskop enthielt Knorpel aus vesikelbehandelten Gelenken deutlich weniger der charakteristischen Recycling‑Vesikel. In Zellkulturen bildeten Chondrozyten, die Makrophagen‑Vesikeln ausgesetzt waren, ebenfalls weniger Autophagosomen und Autolysosomen, was bestätigt, dass ihre Selbstreinigungsmechanismen abgeschaltet wurden, während sich Schäden anhäuften.
Eine einzelne microRNA kippt einen kritischen Schalter
Tiefergehend untersuchte das Team die winzigen RNA‑Regulatoren, die in Makrophagen‑Vesikeln verpackt sind. Ein Molekül, miR‑155‑5p, stach heraus: Es war in Vesikeln aus arthrotischen Tieren und in humanen Arthrosegelenkgeweben, besonders in der Synovialmembran, angereichert. Experimente zeigten, dass vesikelvermitteltes miR‑155‑5p in Chondrozyten gelangt und direkt ein Protein namens GSK‑3β anvisiert, das normalerweise dabei hilft, einen wachstumssteuernden Signalweg namens mTORC1 zu dämpfen. Wird GSK‑3β unterdrückt, wird mTORC1 überaktiv und die Autophagie fällt, sodass Knorpelzellen weniger belastbar werden. Die Blockade von miR‑155‑5p mit einem synthetischen „AntagomiR“ bei Ratten stellte die Autophagie wieder her, bewahrte die Knorpelstruktur und verringerte Arthrosesymptome, während Mäuse, die genetisch kein miR‑155 in ihren Makrophagen hatten, eine mildere Erkrankung und weniger Synovitis entwickelten.
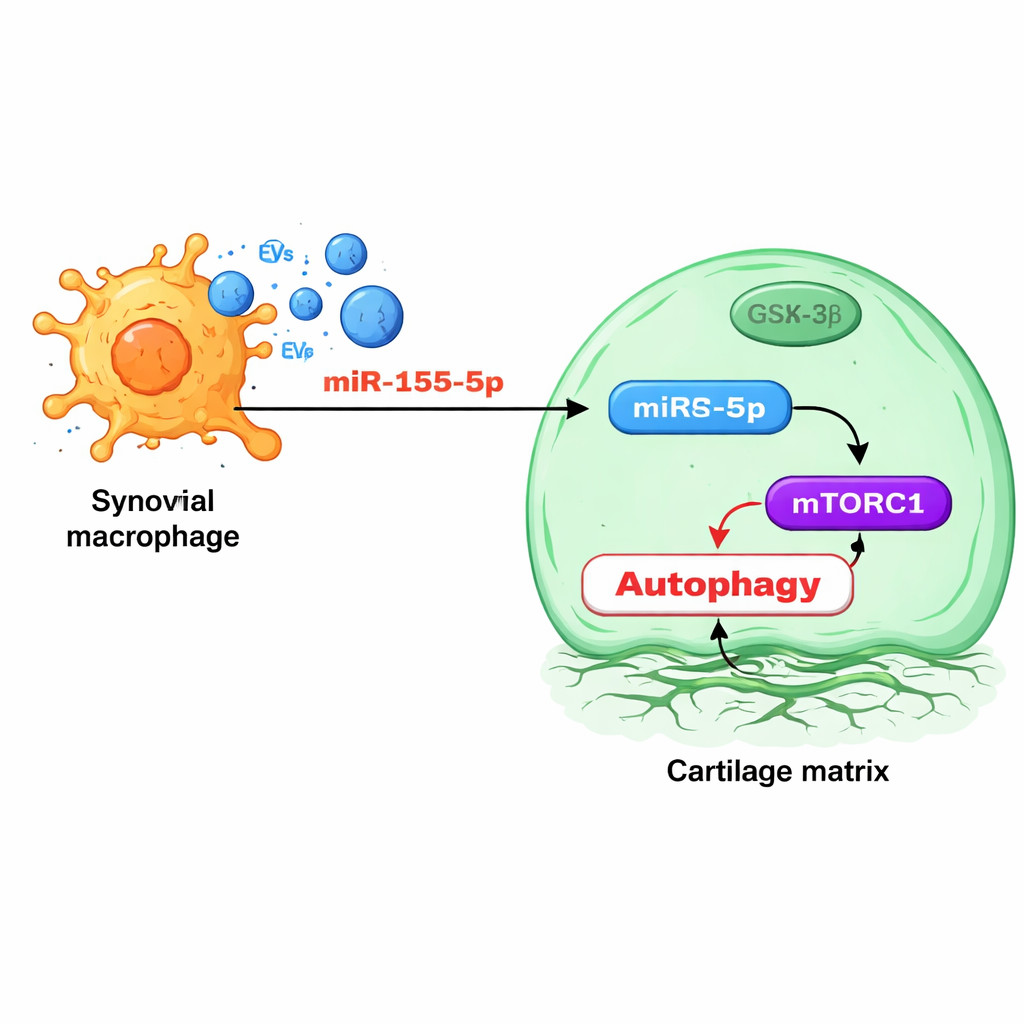
Sortierung und Zielsteuerung des schädigenden Signals
Interessanterweise fanden die Forschenden, dass Makrophagen ein spezifisches RNA‑bindendes Protein, FMRP, verwenden, um miR‑155‑5p selektiv in Vesikel zu laden. Bei erhöhten FMRP‑Spiegeln trugen Vesikel mehr miR‑155‑5p und schadeten den Knorpelzellen stärker; bei reduziertem FMRP wurden die Vesikel weniger toxisch und die Autophagie der Chondrozyten erholte sich. Die FMRP‑Spiegel in zirkulierenden Vesikeln im Blut stiegen parallel zum Fortschreiten der Arthrose bei Ratten und menschlichen Patientinnen und Patienten an, was darauf hindeutet, dass dieses Protein oder die es tragenden Vesikel als blutbasierter Marker für Krankheitsaktivität dienen könnten, ohne Bildgebung oder invasive Eingriffe zu benötigen.
Eine zellfreie Therapie, die die richtigen Zellen ansteuert
Aufbauend auf diesen mechanistischen Erkenntnissen entwickelten die Forschenden eine potenzielle Therapie mit Vesikeln aus adipös‑abgeleiteten stromalen Zellen, einer Art stammzellähnlicher Zellen aus Fettgewebe. Sie dekorierten diese Vesikel mit einem kleinen Peptid, das wie ein „Homing‑Device“ für proinflammatorische Makrophagen wirkt, und luden sie mit AntagomiR‑155‑5p. In arthrotischen Ratten reduzierten wiederholte Injektionen dieser zielgerichteten Vesikel die synoviale Entzündung, verschoben Makrophagen in einen eher „heilenden“ Zustand, senkten die miR‑155‑5p‑Spiegel im Gelenk, stellten GSK‑3β wieder her und verbesserten Knorpelstruktur und -zusammensetzung stärker als nicht zielgerichtete Vesikel. Als man die konstruierten Vesikel an humanem Synovialgewebe im Labor anwandte, reduzierten sie ebenfalls Entzündungsmarker und stärkten anti‑entzündliche Signale.
Was das für Menschen mit Arthrose bedeutet
Diese Arbeit zeichnet Arthrose nicht mehr nur als mechanisch bedingte Verschleißkrankheit, sondern als eine Krankheit, die durch einen molekularen Dialog zwischen entzündeten Gelenkinnenhaut‑Zellen und Knorpel getrieben wird. Proinflammatorische Makrophagen senden Vesikel mit miR‑155‑5p aus, die die Selbstreparatursysteme der Knorpelzellen über den GSK‑3β/mTORC1‑Weg herunterfahren und den Gewebeabbau beschleunigen. Durch das Blockieren dieses Signals — genetisch oder mit zielgerichteten therapeutischen Vesikeln — konnten die Forschenden sowohl Entzündung als auch Knorpelschäden in Tiermodellen und humanen Geweben lindern. Obwohl noch viel Arbeit nötig ist, bevor solche Strategien klinisch verfügbar sind, öffnet die Studie neue Möglichkeiten: Bluttests auf Basis von Vesikel‑Fracht zur Krankheitsverfolgung und präzise, zellfreie Behandlungen, die schädliche Entzündung dämpfen und zugleich den Knorpel in seiner Schutzfunktion unterstützen.
Zitation: Zhao, S., Wang, J., Xue, M. et al. Synovial inflammatory macrophage-derived extracellular vesicles exacerbate cartilage lesions with a FMRP-selectively sorted manner in osteoarthritis. Bone Res 14, 26 (2026). https://doi.org/10.1038/s41413-025-00502-4
Schlüsselwörter: Arthrose, extrazelluläre Vesikel, Makrophagen, Knorpel, MicroRNA‑155