Clear Sky Science · de
Wirksamkeit einer Stammzell-Boost (SCB) bei CAR‑T‑Therapie‑bedingter hämatologischer Toxizität bei Patient:innen mit rezidiviertem/refraktärem Multiplen Myelom (RRMM) — Real‑World‑Erfahrungen des US Multiple Myeloma Immunotherapy Consortium
Warum das für Patient:innen und Familien wichtig ist
Für Menschen mit schwer behandelbarem Multiplem Myelom ist die CAR‑T‑Zelltherapie ein großer Durchbruch, kann aber das Knochenmark so belasten, dass die Neubildung von Blutzellen gestört bleibt. Diese Studie untersucht, ob das Verabreichen eines „Boosts“ mit zuvor entnommenen eigenen Stammzellen die Erholung der Blutwerte sicher beschleunigen kann — und damit möglicherweise Infektionen, Blutungen, Klinikaufenthalte und die Belastung durch anhaltende Schwäche und Transfusionen reduziert.
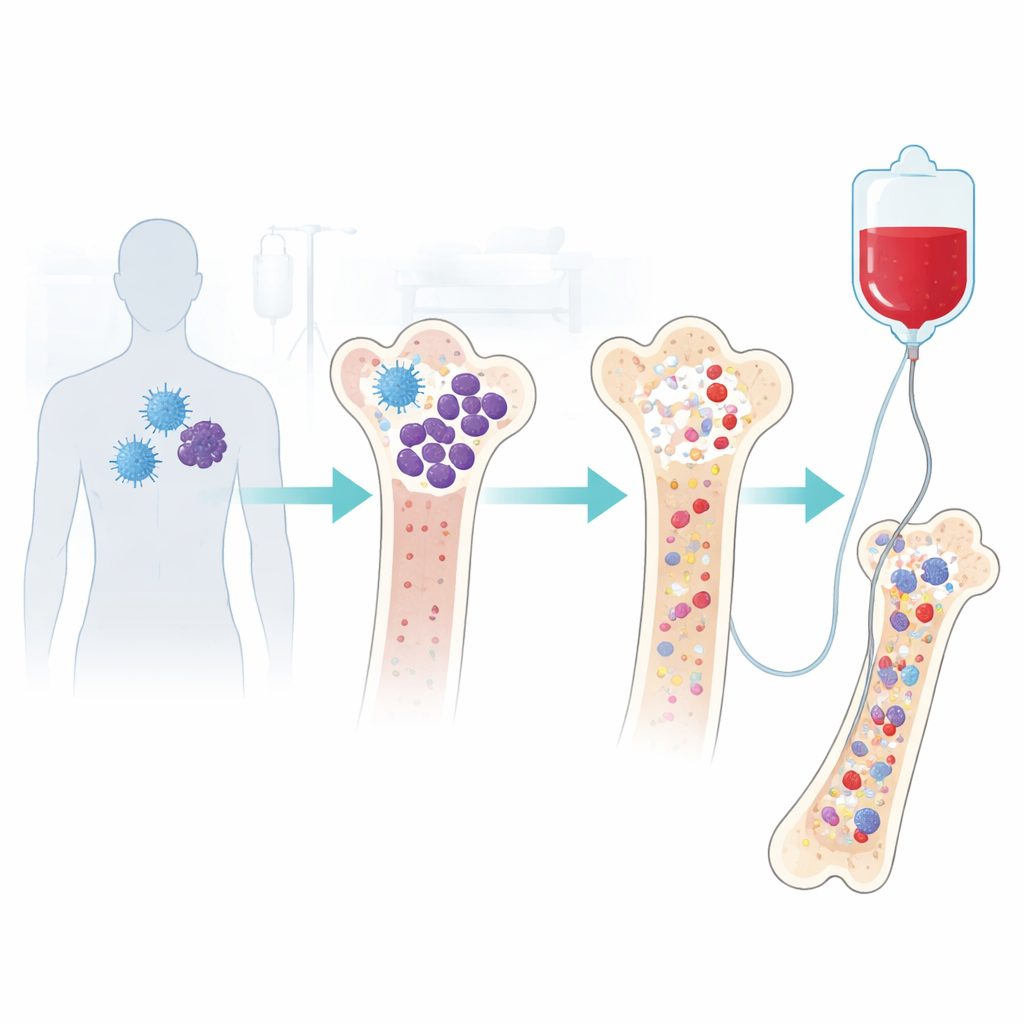
Eine starke Behandlung mit einem anhaltenden Nachteil
Die CAR‑T‑Zelltherapie rüstet die körpereigenen Immunzellen so um, dass sie Myelomzellen erkennen und zerstören. Obwohl sie häufig wirksam ist, kann diese intensive Behandlung das Knochenmark — unsere innere Blutfabrik — vorübergehend schädigen. Viele Patient:innen sehen eine Erholung der Blutwerte innerhalb eines bis drei Monaten. Ein beträchtlicher Teil entwickelt jedoch anhaltende Zytopenien, also gefährlich niedrige Werte von weißen und roten Blutkörperchen sowie Thrombozyten. Das erhöht das Risiko für schwere Infektionen, Erschöpfung und Blutungen und kann Patient:innen an regelmäßige Transfusionen und Wachstumsfaktor‑Injektionen binden. Ärzt:innen brauchten bessere Wege, diesen Patient:innen zur Erholung zu verhelfen, ohne den Nutzen der CAR‑T zu schmälern.
Ein realer Test einer einfachen Idee
Die Forschenden untersuchten 590 Erwachsene mit rezidiviertem oder refraktärem Multiplem Myelom, die mit kommerziellen CAR‑T‑Produkten an 19 US‑Krebszentren behandelt wurden. 91 entwickelten anhaltend niedrige Blutwerte; davon erhielten 39 einen autologen Stammzell‑Boost und 52 nur die standardmäßige supportive Versorgung. Der Boost verwendete Stammzellen, die zuvor gesammelt und eingefroren worden waren, oft im Rahmen einer früheren Stammzelltransplantation. Vor dem Boost wurde keine zusätzliche Chemotherapie verabreicht. Um einen fairen Vergleich zu ermöglichen, wurden Kontrollpatient:innen ausgewählt, weil sie 30 Tage nach CAR‑T ähnliche schwere Neutropenien und Thrombozytopenien aufwiesen.
Schnellere, vollständigere Blutwerterholung
In der Gruppe mit Stammzell‑Boost erreichte beinahe jede auswertbare Person (97,4 %) eine Erholung der Blutwerte nach gängigen Transplantationskriterien. Nach dem Boost erholten sich die Neutrophilen (infektionsbekämpfende weiße Zellen) typischerweise in etwa 13 Tagen, die Thrombozyten in 18 Tagen und das Hämoglobin in 24 Tagen. 90 Tage nach CAR‑T hatten Patient:innen mit Boost deutlich bessere Blutwerte als die gematchten Kontrollpatient:innen: höheres Hämoglobin und deutlich höhere Thrombozytenzahlen, mit einem Trend zu besseren weißen Blutwerten. Diese Vorteile zeigten sich auch, wenn man nur die schwerste Untergruppe innerhalb der Boost‑Empfänger betrachtete, was darauf hindeutet, dass der Effekt nicht nur auf der Auswahl weniger schwerer Fälle beruhte.
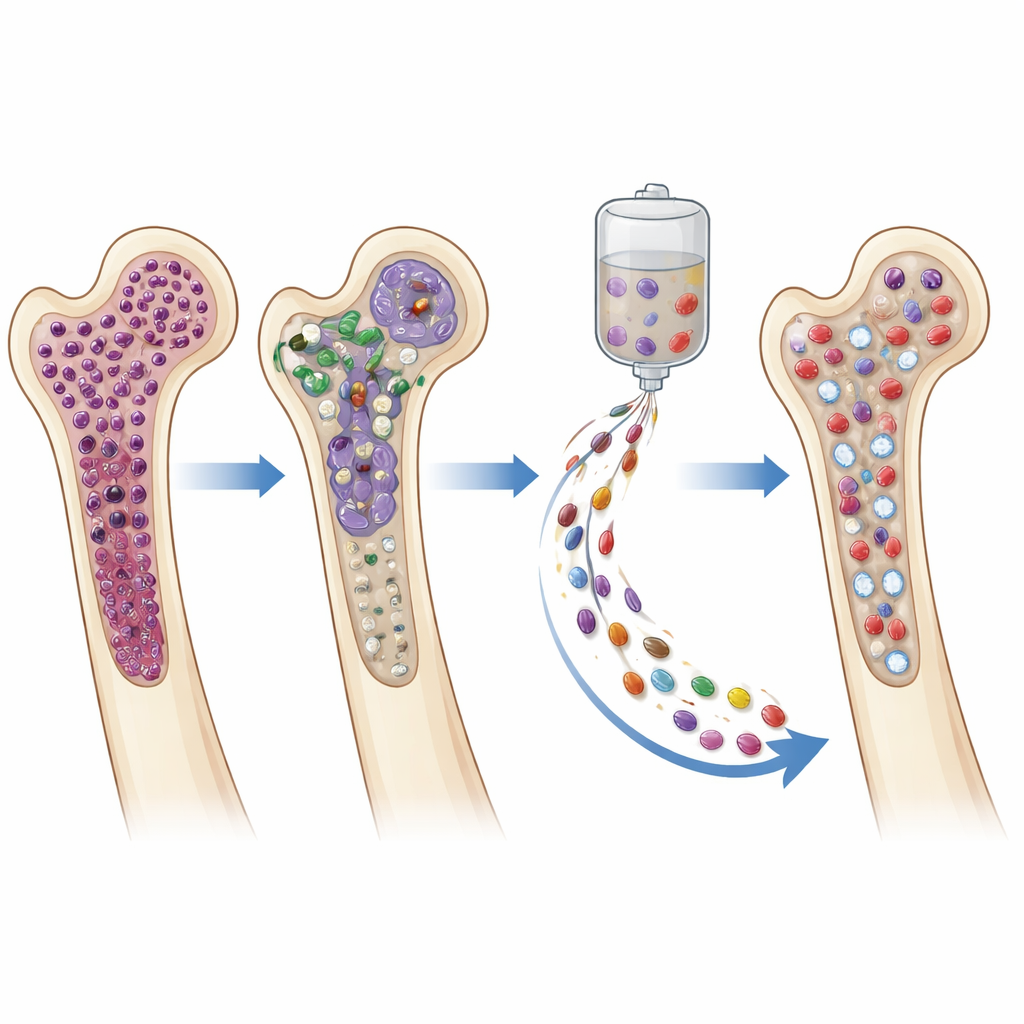
Sicherheit, Infektionen und Krebs‑Kontrolle
Wichtig ist, dass der Stammzell‑Boost keine neuen Sicherheitsprobleme einführte. Keine Komplikationen wurden direkt dem Boost zugeschrieben, und schwere Infektionen in der Boost‑Gruppe traten vor, nicht nach der Verabreichung der Stammzellen auf. Einige Patient:innen hatten komplexe immunologische Probleme im Zusammenhang mit der CAR‑T‑Therapie, aber es zeigte sich kein Hinweis darauf, dass der Boost diese Probleme in dieser Kohorte verschlimmerte. Ebenso wichtig: Die zusätzlichen Stammzellen schienen die krebsbekämpfende Wirkung der CAR‑T nicht zu beeinträchtigen. Raten für tiefe Remissionen und Negativität von minimaler Residualerkrankung waren zwischen den Gruppen ähnlich, und die Überlebensdaten waren im Boost‑Arm mindestens ebenso gut — wobei zu berücksichtigen ist, dass Patient:innen lange genug leben mussten, um den Boost zu erhalten.
Was das für die künftige Versorgung bedeuten könnte
Für Patient:innen lautet die Kernbotschaft: Das Einfrieren eigener Stammzellen kann eine wirksame Rescue‑Option bieten, falls die Blutwerte nach CAR‑T stagnieren. In dieser großen Real‑World‑Serie war ein Stammzell‑Boost — ohne zusätzliche Chemotherapie — sicher und führte bei nahezu allen behandelten Patient:innen zu einer schnellen, zuverlässigen Wiederherstellung der Blutbildung, ohne die krebsbekämpfenden Effekte der CAR‑T zu gefährden. Die Autor:innen schlagen praktische Kriterien vor, wann ein Boost in Betracht gezogen werden sollte, etwa anhaltender Transfusionsbedarf über 30 Tage hinaus und sehr niedrige Werte ohne Anzeichen der Besserung. Prospektive Studien sind weiterhin erforderlich, aber diese Ergebnisse unterstützen, die Sammlung und Lagerung von Stammzellen routinemäßig in die Planung einer CAR‑T‑Therapie bei Hochrisiko‑Myelom einzubeziehen.
Zitation: Varga, C., Robinson, M., Davis, J.A. et al. Efficacy of stem cell boost (SCB) for chimeric antigen receptor-T cell therapy (CAR-T)-related hematologic toxicity in patients with relapsed/refractory multiple myeloma (RRMM)—real world experience from the US multiple myeloma immunotherapy consortium. Blood Cancer J. 16, 39 (2026). https://doi.org/10.1038/s41408-026-01469-z
Schlüsselwörter: CAR‑T‑Therapie, Multiples Myelom, Stammzell‑Boost, Knochenmarkserholung, hämatologische Toxizität