Clear Sky Science · de
Genomische strukturelle Varianten tragen zur Prognoseabschätzung bei Patienten mit zytogenetisch normalem akuten myeloischen Leukämie bei
Warum winzige DNA-Veränderungen für Leukämiepatienten wichtig sind
Bei erwachsenen Patienten mit akuter myeloischer Leukämie (AML) nutzen Ärzte zunehmend Gentests, um vorherzusagen, wie gut eine Behandlung voraussichtlich wirken wird. Für fast die Hälfte dieser Patienten erscheinen die Standard-Chromosomenuntersuchungen jedoch „normal“, sodass ihre Zukunft schwer vorherzusagen bleibt. Diese Studie zeigt, dass versteckte, kleinräumige Umbauten in der DNA — zu klein, um unter dem Mikroskop sichtbar zu sein — eine Patientengruppe deutlich abgrenzen, deren Erkrankung weitaus aggressiver verläuft als es die aktuellen Instrumente vermuten lassen.
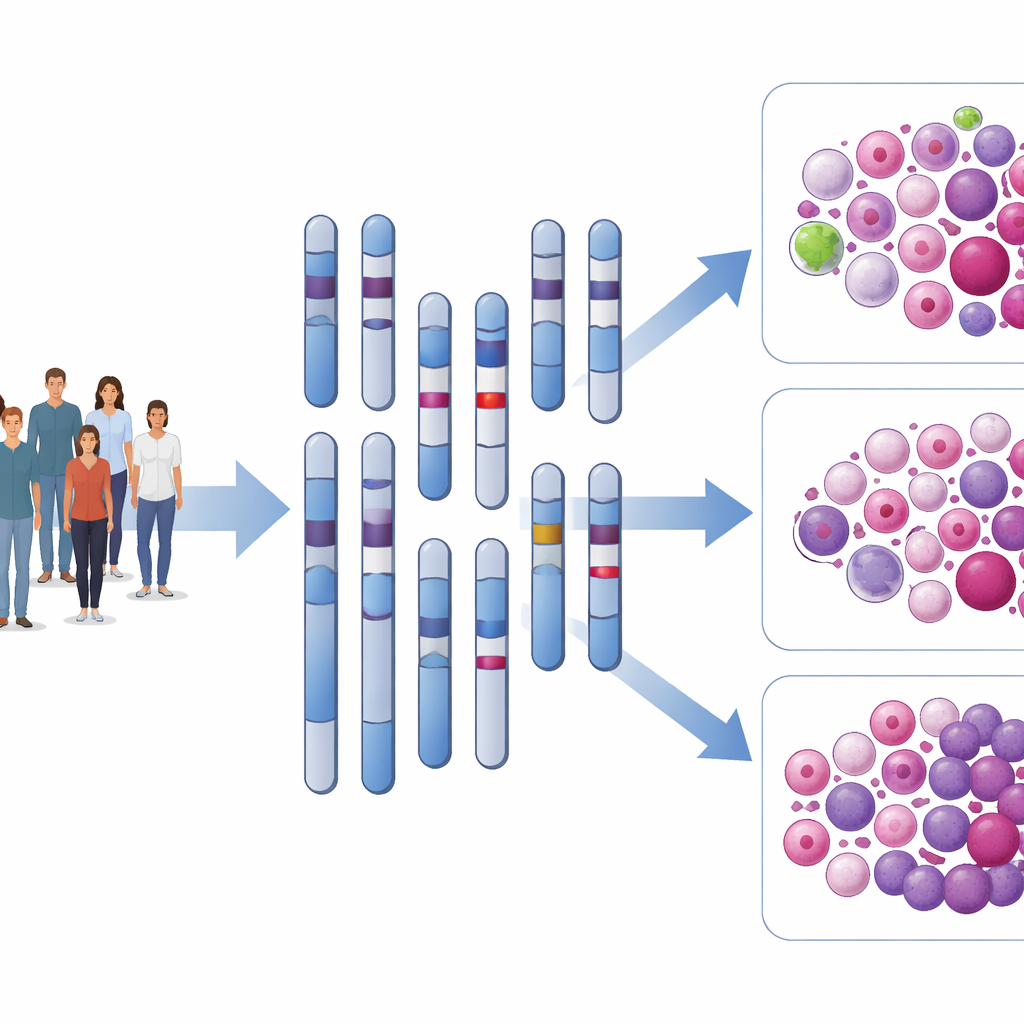
Hinter normal aussehenden Chromosomen sehen
AML ist eine Blutkrebserkrankung, bei der unreife weiße Blutzellen das Knochenmark und die gesunden Zellen verdrängen. Ärzte untersuchen routinemäßig Chromosomen und bekannte Genmutationen, um Patienten in günstige, intermediäre oder ungünstige Risikogruppen einzuordnen; diese Einteilung beeinflusst Entscheidungen wie das frühzeitige Angebot einer Stammzelltransplantation. Bei etwa 45 % der Patienten ist jedoch die AML „zytogenetisch normal“ — das heißt, die Chromosomen erscheinen intakt — obwohl die klinischen Verläufe von langfristigem Überleben bis zu schnellem Rückfall reichen. Die Autoren vermuteten, dass subvisuelle DNA-Umbauten, bekannt als strukturelle Varianten, zur Erklärung dieser verborgenen Vielfalt beitragen könnten.
Langlese-Sequenzierung als genetische Lupe
Um diese kryptischen Veränderungen aufzuspüren, nutzte das Team Langlese-Ganzgenomsequenzierung, eine Technologie, die sehr lange DNA-Abschnitte liest und besonders geeignet ist, Einschlüsse, Deletionen und andere Umlagerungen zu entdecken. Sie wendeten diese Methode auf Leukämiezellen von 162 intensiv behandelten Erwachsenen mit zytogenetisch normaler AML an, die in zwei klinischen Studien eingeschlossen waren. Nach strenger Filterung zur Entfernung vererbter Varianten und technischer Artefakte reduzierten sie mehr als zweitausend Rohbefunde auf 118 verlässliche strukturelle Varianten, verteilt über die Autosomen. Die meisten waren kleine Insertions- oder Deletionsereignisse in nicht-codierenden Bereichen des Genoms, etwa Introns und regulatorischen Regionen, und nicht direkt in proteinkodierenden Sequenzen.
Fünf kleine Veränderungen definieren eine Hochrisikogruppe
Die Forschenden untersuchten dann, welche dieser 118 Varianten mit der Überlebenszeit der Patienten und der Dauer bis zu Ereignissen wie Rückfall oder Therapieversagen korrelierten. Mithilfe von maschinellem Lernen und Überlebensmodellen identifizierten sie fünf spezifische strukturelle Varianten, die unabhängig voneinander deutlich schlechtere Outcomes signalisierten. Patienten mit mindestens einer dieser „Hochrisikovarianten“ — etwa 13–15 % der untersuchten Personen — hatten geringere Chancen auf vollständige Remission, erlitten häufiger Rückfälle und wiesen deutlich verkürzte Überlebenszeiten auf, meist unter einem Jahr. Diese Effekte blieben bestehen, selbst nach Adjustierung für bekannte Mutationen wie FLT3 und NPM1, und bestätigten sich in einer zweiten, realen Kohorte von 149 weiteren Patienten, die mit gezielten Tests untersucht wurden.
Bestehende Risikoscores verbessern und biologisch erklären
Aktuelle europäische Risikorichtlinien ordnen alle zytogenetisch normalen Patienten in breite Kategorien auf Basis bestimmter Mutationen ein, schaffen aber oft keine saubere Trennung zwischen intermediärem und ungünstigem Risiko. Durch Hinzufügen des Vorhandenseins einer der fünf Hochrisikovarianten als neue „sehr ungünstige“ Stufe entwickelten die Autoren ein aktualisiertes vierstufiges Schema. Dieser verfeinerte Score sagte Gesamt- und ereignisfreies Überleben genauer voraus als das Standardmodell, insbesondere bei Patienten mit NPM1-Mutationen, die normalerweise als günstig gelten, aber sehr schlecht abschnitten, wenn sie zusätzlich diese strukturellen Veränderungen trugen. Laboruntersuchungen stützten eine biologische Grundlage: Die Hochrisikovarianten waren mit veränderter Aktivität benachbarter Gene verbunden, und experimentelle Modulation der Expression einiger dieser Gene in Zellmodellen störte normales Zellwachstum und Zellzyklus-Kontrolle — Merkmale, die zu einem aggressiveren Leukämieverlauf passen.
Was das für Patienten und die Versorgung bedeutet
Praktisch bedeutet diese Arbeit, dass einige AML-Patienten, deren Chromosomen normal erscheinen und die derzeit als „intermediär“ oder sogar „günstig“ eingestuft werden, tatsächlich eine weitaus gefährlichere Form der Erkrankung in sich tragen können. Eine kleine Anzahl winziger DNA-Umlagerungen — nachweisbar mit moderner Sequenzierung oder gezielten Nachtests — kann diese Patienten früh identifizieren. Das Erkennen dieser verborgenen sehr-hochrisikogruppe könnte Ärzten helfen, Betroffene zu intensiveren oder experimentellen Therapien und engmaschigerer Überwachung zu raten, mit dem Ziel, die derzeit schlechten Behandlungsergebnisse zu verbessern.
Zitation: Bartalucci, N., Mannelli, F., Tarantino, D. et al. Genomic structural variations contribute to inform prognosis in patients with cytogenetically normal acute myeloid leukemia. Blood Cancer J. 16, 37 (2026). https://doi.org/10.1038/s41408-026-01465-3
Schlüsselwörter: akute myeloische Leukämie, strukturelle Variante, genomische Risikostratifizierung, Langzeitsequenzierung, NPM1-Mutation