Clear Sky Science · de
Astrozytäre APOE3-Christchurch-Expression mildert Amyloid-β-Pathologie im Gehirn von 5xFAD-Mäusen
Warum diese Gehirnvariante wichtig ist
Die Alzheimer-Krankheit wird meist als ein unaufhaltsames Anhäufen schädlicher Proteinklumpen im Gehirn dargestellt. Doch eine Handvoll Menschen wirkt ungewöhnlich widerstandsfähig und bleibt geistig fit, obwohl sie ein hohes genetisches Risiko trägt. Diese Studie richtet den Blick auf eine solche schützende Abweichung in einem verbreiteten Gen für den Cholesterinstoffwechsel und stellt eine praktische Frage: Führt eine verstärkte Zufuhr dieser Schutzvariante — gezielt aus den Stütz‑/Versorgungszellen, den Astrozyten — dazu, dass Alzheimer‑ähnliche Veränderungen weniger schädlich werden?
Eine schützende Genvariante im Rampenlicht
Die Arbeit konzentriert sich auf eine seltene Variante des APOE-Gens, genannt APOE3-Christchurch. In einem bemerkenswerten realen Fall blieb eine Frau, die eine starke familiäre Früherkrankungs‑Mutation trug, jahrzehntelang kognitiv intakt — und diese APOE‑Variante schien ein wesentlicher Grund dafür zu sein. Frühere Tierstudien deuteten darauf hin, dass APOE3-Christchurch die Ausbreitung eines weiteren Alzheimer‑Kennzeichens, des Tau‑Proteins, verlangsamen kann. Ihr Einfluss auf Amyloid‑beta, das Protein, das die klassischen Plaques in Alzheimer‑Gehirnen bildet, war jedoch noch nicht vollständig geklärt. Die Forschenden wollten herausfinden, wie sich diese Variante verhält, wenn sie spezifisch von Astrozyten exprimiert wird — den sternförmigen Zellen, die Neuronen nähren und schützen.
Test der Variante in einer Alzheimer‑ähnlichen Maus
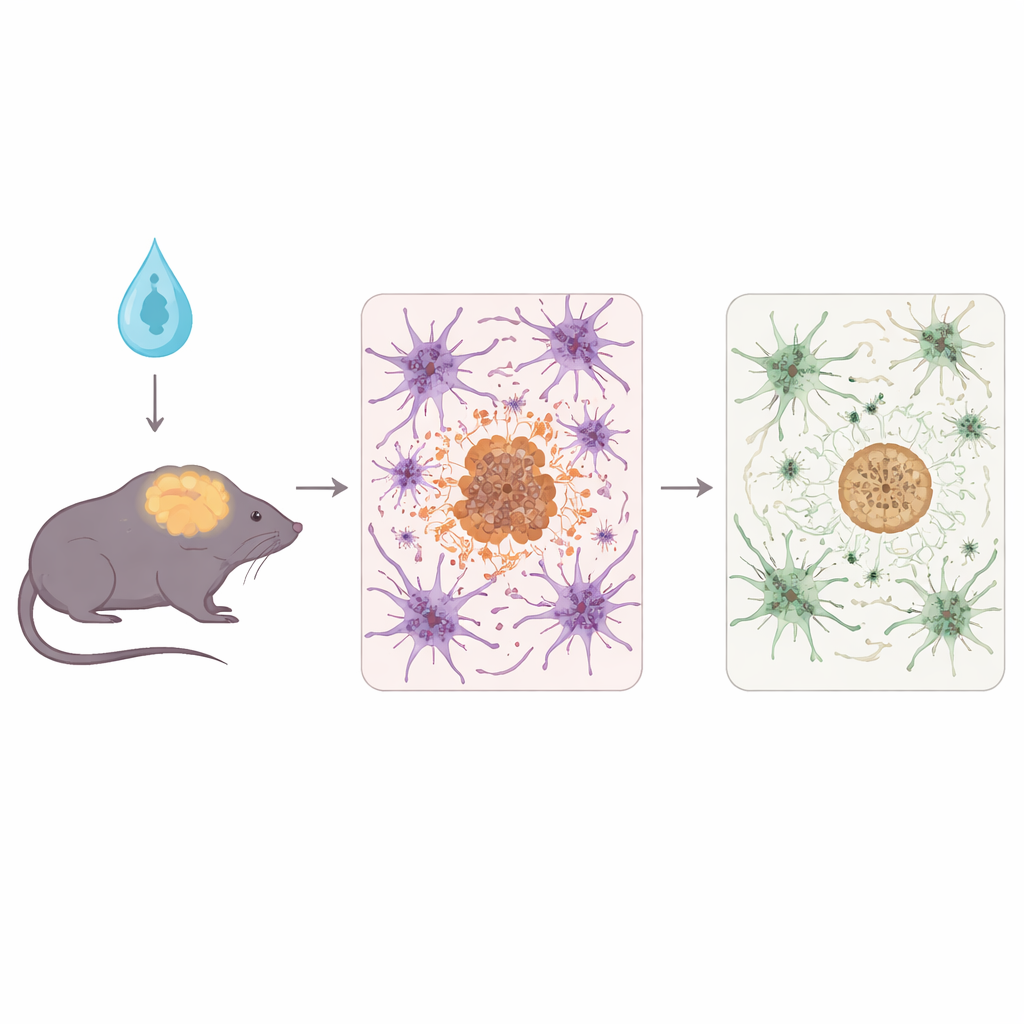
Um dies zu untersuchen, nutzte das Team 5xFAD‑Mäuse, ein etabliertes Modell, das rasch starke Amyloidablagerungen und damit verbundene Hirnschäden entwickelt. Kurz nach der Geburt erhielten die Mäuse einen harmlosen viralen Vektor, der ihre Astrozyten dazu brachte, entweder das normale humane APOE3, die schützende APOE3‑Christchurch‑Variante oder ein neutrales Kontrollprotein herzustellen. Anschließend analysierten die Wissenschaftler die Tiere in einem fortgeschrittenen Krankheitsstadium und untersuchten Hirngewebe mit biochemischen Tests, Fluoreszenzmikroskopie und RNA‑Sequenzierung, um zu sehen, wie Amyloid, benachbarte Nervenfasern und Immunreaktionen verändert waren.
Plaques weniger toxisch machen, nicht nur weniger werden
Beide von Astrozyten produzierten APOE‑Formen reduzierten die Gesamtlast an Amyloid‑Plaques und die – im Umfeld der Plaques sichtbaren – Schädigungszeichen im Vergleich zu Kontrollen. APOE3‑Christchurch zeigte jedoch wichtige Unterschiede. Es verschob Amyloid hin zu kompakteren, kugeligen, fibrillären Plaques und senkte die Mengen bestimmter löslicher und oligomerer Amyloid‑beta‑Formen — Spezies, die als besonders synaptotoxisch gelten. Die Neuriten, die dünnen Ausläufer von Nervenzellen in Plaquenähe, zeigten bei Vorhandensein von APOE3‑Christchurch weniger Verformung und Schädigung. Parallel dazu waren die Gehirn‑Immunzellen, Mikroglia und Astrozyten, insgesamt weniger reaktiv, und Transkriptomanalysen offenbarten abgeschwächte Immun‑ und Protein‑Stress‑Wege, was auf eine ruhigere, weniger feindselige Umgebung für Neuronen hindeutet.
Hinweise aus Zellkulturen und Genaktivität
Um zu bestätigen, dass diese Effekte nicht auf Mäuse beschränkt sind, verwendete das Team außerdem aus menschlichen Stammzellen gewonnene Astrozyten, die so verändert wurden, dass sie entweder APOE3 oder die Christchurch‑Variante tragen. Astrozyten mit APOE3‑Christchurch sezernierten mehr APOE‑Protein, und ihr konditioniertes Medium verringerte in einem kontrollierten Reagenzglas‑Test die Bildung von Amyloid‑beta‑Oligomeren. In Mäusegehirnen veränderte die Expression von APOE3‑Christchurch Netzwerke von Genen, die an Proteinfaltung, zellulärem Stress und Immun‑Signalgebung beteiligt sind, und senkte die Spiegel von Proteinen, die mit Stressreaktionen und gestörtem Lipidstoffwechsel verknüpft sind. Zusammengenommen deuten diese Befunde darauf hin, dass APOE3‑Christchurch nicht einfach die Menge an Amyloid ändert — es verändert seine Form und die Art und Weise, wie Gehirnzellen darauf reagieren.
Was das für zukünftige Behandlungen bedeuten könnte
Die hier beobachteten schützenden Effekte sind eher moderat als spektakulär, aber sie sind sehr aufschlussreich. Die Studie zeigt, dass das gezielte Verstärken von APOE3‑Christchurch in Astrozyten Amyloidablagerungen kompakter und scheinbar weniger toxisch machen, umliegende Nervenschäden reduzieren und entzündliche sowie Stress‑Signale dämpfen kann, selbst wenn Amyloid nicht vollständig eliminiert wird. Für eine nichtfachliche Leserschaft ist die zentrale Erkenntnis, dass nicht alle Plaques gleich schädlich sind: Ihre Umformung und Neutralisierung kann ebenso wichtig sein wie ihr Abbau. Diese Ergebnisse stützen die Idee, dass von APOE3‑Christchurch inspirierte Therapien — etwa über Gentherapie oder Medikamente, die sein Verhalten nachahmen — dem Gehirn helfen könnten, besser mit Amyloid zu leben und möglicherweise den Verlauf der Alzheimer‑Krankheit zu verlangsamen oder abzumildern.
Zitation: Raulin, AC., Alnobani, A., Rodriguez-Martinez, P. et al. Astrocytic APOE3-Christchurch expression ameliorates brain amyloid-β pathology in 5xFAD mice. Transl Psychiatry 16, 224 (2026). https://doi.org/10.1038/s41398-026-04002-9
Schlüsselwörter: Alzheimer-Krankheit, APOE3-Christchurch, Amyloid-beta, Astrozyten, Gentherapie