Clear Sky Science · de
MicroRNA-132/212 modulieren die Opioid-Belohnung negativ, indem sie den Dopamintransporter im ventralen Tegmentum anvisieren
Warum diese Forschung für den Alltag wichtig ist
Opioid-Schmerzmittel und verwandte Substanzen können Linderung bringen, bergen aber auch ein hohes Abhängigkeitsrisiko. Diese Studie blickt in das Belohnungssystem des Gehirns und identifiziert winzige genetische Schalter, die beeinflussen, wie stark Opioide als belohnend empfunden werden. Durch das Verständnis dieser Schalter hoffen Wissenschaftler, gezieltere Behandlungen zu entwickeln, die Schmerzen lindern oder Abhängigkeit verringern, ohne die Lustkreisläufe des Gehirns zu kapern.
Kleine Moleküle mit großer Wirkung
Unser Gehirn nutzt das Botenstoff Dopamin, um Vergnügen zu signalisieren und uns zu motivieren, belohnende Erfahrungen anzustreben — von leckerem Essen bis zu suchterzeugenden Drogen. Stärke und Dauer dieses Signals werden teilweise durch ein Protein gesteuert, den Dopamintransporter, der wie ein Staubsauger Dopamin wieder in Nervenzellen aufnimmt. Die Autor:innen richteten ihr Augenmerk auf zwei sehr kleine genetische Elemente, microRNA-132 und microRNA-212, die die Produktion bestimmter Proteine herunterregeln können. Frühere Arbeiten verknüpften diese microRNAs mit Kokainkonsum und Stress. In dieser Arbeit untersuchte das Team, ob sie auch die Reaktion des Gehirns auf Opioide, insbesondere Morphin, mitbestimmen.
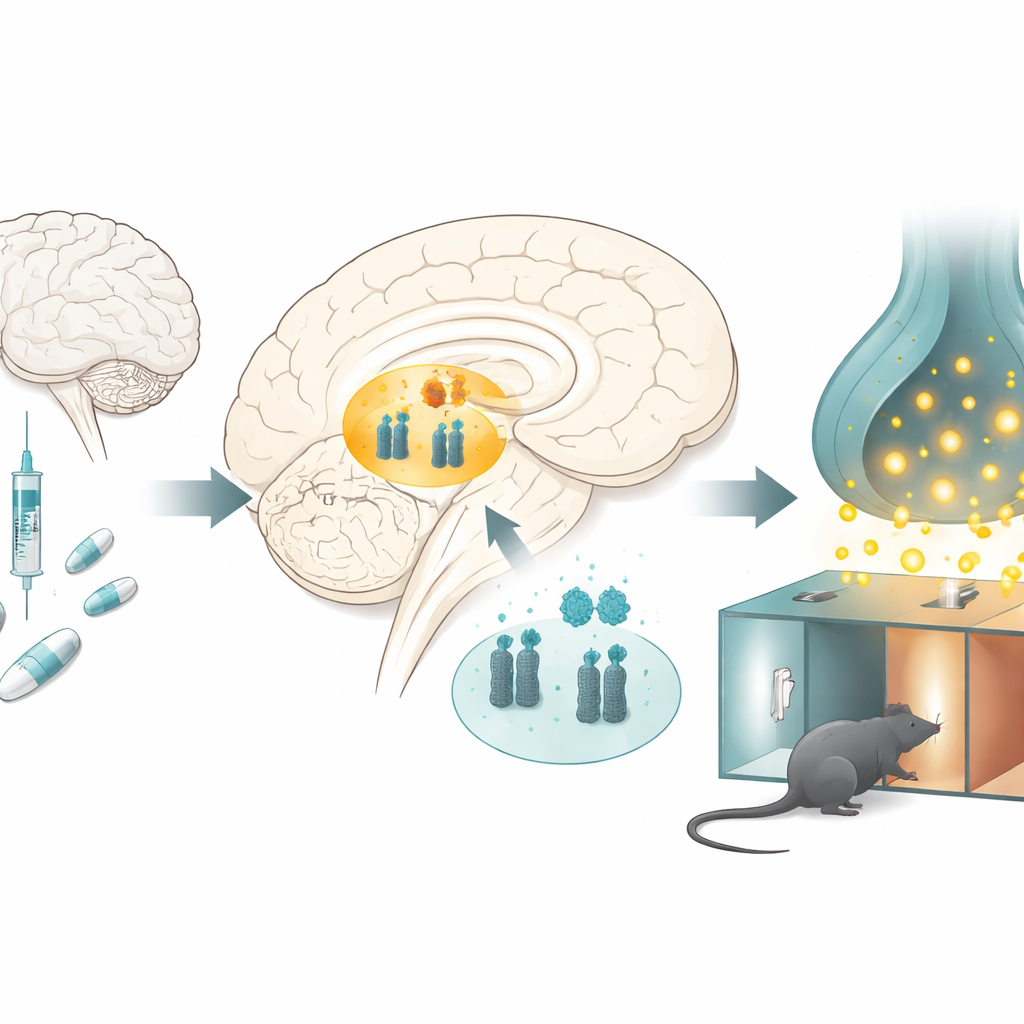
Wie Opioide das Belohnungszentrum des Gehirns verändern
Die Forschenden untersuchten Ratten, die wiederholt Morphin erhielten, in einem klassischen Test für Drogenbelohnung, bei dem Tiere lernen, einen mit der Droge assoziierten Raum zu bevorzugen. Nach mehreren Tagen verbrachten die Morphin-behandelten Ratten mehr Zeit in der Morphin-gekoppelten Kammer, was zeigt, dass die Substanz belohnend wirkte. Bei der Analyse einer zentralen Belohnungsregion tief im Gehirn, dem ventralen Tegmentum, fanden sie ein auffälliges Muster: Die Spiegel von microRNA-132 und microRNA-212 waren reduziert, während die des Dopamintransporters erhöht waren. Ähnliche Veränderungen traten auf, wenn Ratten Morphin ohne die Orts-Lernaufgabe erhielten, was darauf hindeutet, dass chronische Drogenexposition selbst dieses molekulare Gleichgewicht verschiebt.
Ein direkter molekularer Zusammenhang
Um zu prüfen, ob diese microRNAs den Dopamintransporter tatsächlich kontrollieren, wandte sich das Team menschlichen, nervenähnlichen Zellen im Labor zu. Durch künstliches Hochregulieren von microRNA-132 oder microRNA-212 beobachteten sie einen Rückgang sowohl der Boten-RNA als auch des Transporterproteins. Das Blockieren der microRNAs hatte den entgegengesetzten Effekt. Danach konstruierten sie einen Reporter, bei dem ein Licht erzeugendes Enzym mit dem regulatorischen Abschnitt des Transporters verknüpft war. Das Hinzufügen der microRNAs dimmte das Lichtsignal, dieser Effekt verschwand jedoch, wenn einige Schlüsselbasen in der Bindungsstelle mutiert wurden. Zusammengenommen zeigten diese Experimente, dass microRNA-132 und microRNA-212 direkt an die Botschaft des Transporters binden und seine Produktion unterdrücken.
Von Molekülen zu Dopaminspiegeln und Verhalten
Als Nächstes fragten die Forschenden, wie sich diese molekulare Kontrolle in lebenden Nervenzellen auswirkt. In kultivierten Nervenzellen reduzierte die Erhöhung der microRNAs die Dopaminaufnahme, während deren Blockade die Dopaminbeseitigung verstärkte. Als sie künstlich die Menge des Dopamintransporters erhöhten oder verringerten, stieg bzw. fiel der Einfluss der microRNAs entsprechend — ein Hinweis darauf, dass der Transporter der wesentliche Vermittler ist. In lebenden Ratten führte das Hochregulieren von microRNA-132 im ventralen Tegmentum zu höheren Dopaminspiegeln in verbundenen Regionen, was auf verminderte Transporteraktivität hindeutet. Verhaltensmäßig bewirkte das virale Einsetzen von „Sponges“ zur Aufnahme (Bindung) von microRNA-132 oder microRNA-212 in dieser Gehirnregion, dass Ratten eine stärkere Präferenz für Morphin erlernten und zugleich höhere Transporterspiegel aufwiesen. Umgekehrt senkte das gezielte Zufügen zusätzlicher microRNA-132 in derselben Region die Transporterspiegel und schwächte die Morphinpräferenz bei männlichen, weiblichen und jugendlichen Tieren, ohne Bewegung oder die Freude an natürlichen Belohnungen wie zuckerhaltigem Wasser zu beeinträchtigen.
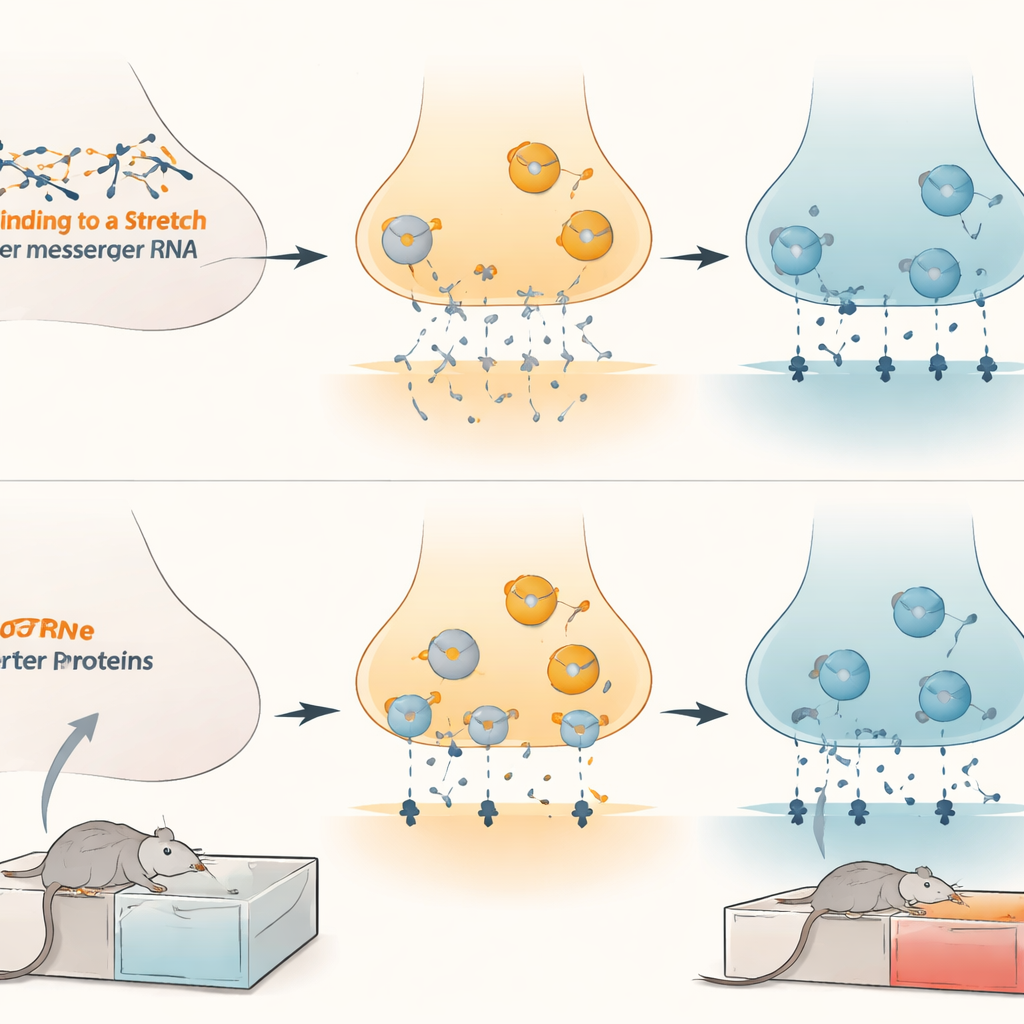
Folgen für die Behandlung von Opioidabhängigkeit
Diese Befunde legen ein fein abgestimmtes Bremssystem innerhalb der Belohnungsschaltkreise des Gehirns offen: microRNA-132 und microRNA-212 halten den Dopamintransporter in Schach und prägen dadurch, wie stark Opioide als belohnend erlebt werden. Chronisches Morphin scheint diese Bremse durch Senkung der microRNAs zu lösen, wodurch die Transporterspiegel ansteigen und die Konsolidierung drogenbezogener Belohnungssignale begünstigt wird. Indem man die Wirkung dieser microRNAs gezielt im ventralen Tegmentum wiederherstellt oder nachahmt, könnte man die Wirkkraft der Opioid-Belohnung abschwächen, ohne allgemeines Vergnügen oder Bewegung zu dämpfen. Zwar ist noch viel Arbeit nötig, bevor solche Ansätze am Menschen getestet werden können, doch weist diese Studie auf eine neue, hochspezifische Route für künftige Behandlungen hin, die Sucht auf Ebene der molekularen Stellräder des Gehirns angehen.
Zitation: Meng, J., Li, Z., Zhang, Y. et al. MicroRNA-132/212 negatively modulates opioid reward by targeting dopamine transporter in the ventral tegmental area. Transl Psychiatry 16, 152 (2026). https://doi.org/10.1038/s41398-026-03915-9
Schlüsselwörter: Opioidabhängigkeit, Dopamintransporter, microRNA-132, ventrales Tegmentum, Morphin-Belohnung