Clear Sky Science · de
Niedrige Konzentrationen von Amyloid‑Beta‑Oligomeren induzieren eine für leichte kognitive Beeinträchtigung typische Synaptogenese und verändern das de novo‑Proteom
Frühe Veränderungen, die auf Gedächtnisprobleme hinweisen können
Bevor die Alzheimer‑Krankheit Menschen das Gedächtnis raubt, durchläuft das Gehirn eine diffuse Zwischenphase, die als leichte kognitive Beeinträchtigung bekannt ist. In diesem Stadium sind Denkstörungen bemerkbar, das Alltagsleben läuft aber oft weiter. Merkwürdigerweise zeigen einige Hirnregionen in dieser Phase mehr, nicht weniger Verbindungen zwischen Nervenzellen. Die Studie fragt, ob kleine Mengen eines für Alzheimer typischen schädlichen Moleküls dieses Aufblühen neuer Verbindungen auslösen können und ob ein bereits bei Krebspatienten getestetes Medikament diese sehr frühen Veränderungen abschwächen könnte.
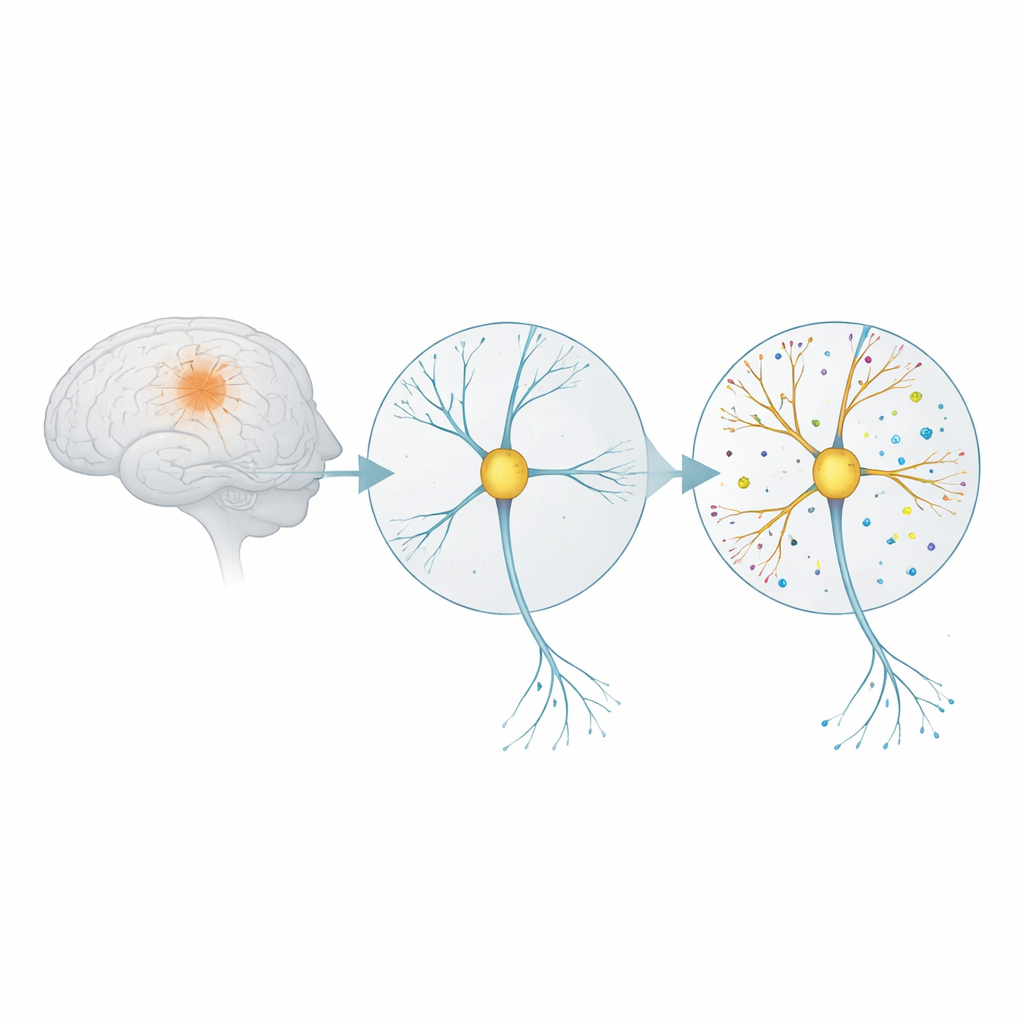
Wie Nervenkontakte auf einen toxischen Auslöser reagieren
Die Alzheimer‑Krankheit steht in engem Zusammenhang mit kleinen Klumpen eines Proteinfragments namens Amyloid‑Beta. In seiner Oligomerform ist dieses Fragment besonders schädlich für Synapsen – die Kontaktstellen, an denen Nervenzellen miteinander kommunizieren. Die Forschenden züchteten Rattenhirnzellen in einer Schale, bis sie ausgereifte Netzwerke bildeten, und setzten sie dann fünf Tage lang einer niedrigen Dosis von Amyloid‑Beta‑Oligomeren aus. Zusätzlich prüften sie, was geschah, wenn ein Wirkstoff namens eFT508 hinzugegeben wurde, der ein Signalenzym (MNK) blockiert, das an der Initiation der Proteinsynthese in Zellen beteiligt ist. Dieses Experiment sollte sehr frühe Krankheitsstadien nachbilden, bevor es zu umfassendem Zelltod kommt.
Verborgene Details neuer Synapsen sichtbar machen
Um zu untersuchen, wie sich die Verbindungen veränderten, verwendete das Team die „Expansion‑Mikroskopie“, eine Technik, die konservierte Zellen in ein weiches Gel aufquellen lässt, sodass winzige Strukturen feiner sichtbar werden. Sie markierten Nervenfasern und beide Seiten der Synapse mit fluoreszierenden Farbstoffen und rekonstruierten sie in 3D. Die Exposition gegenüber Amyloid‑Beta führte zu einem deutlichen Anstieg der Anzahl von Synapsen entlang der Nervenverästelungen. Insbesondere gab es mehr einzelne Boutons – einfache Eins‑zu‑Eins‑Kontaktstellen – und ungewöhnliche „multi‑innervierte Spines“, bei denen mehr als eine eingehende Faser an einem einzigen Empfangspunkt zusammenläuft. Diese Muster ähneln den synaptischen Zunahmen, die bei Menschen mit leichter kognitiver Beeinträchtigung beschrieben wurden. In Gegenwart von eFT508 sanken die Synapsenzahlen wieder in Richtung Normalwert, was darauf hindeutet, dass das Medikament diesem frühen Überwuchs entgegentreten könnte.
Neue Proteine verändern sich, auch wenn die Gesamtmenge gleich bleibt
Synapsen werden ständig durch Auf‑ und Abbau von Proteinen umgebaut. Das Team untersuchte als Nächstes, welche Proteine während und nach der Amyloid‑Beta‑Exposition neu hergestellt wurden. Sie fütterten die Neuronen mit einer harmlosen künstlichen Aminosäure, die in frisch synthetisierte Proteine eingebaut wird, und nutzten dann chemische „Click“‑Reaktionen und Massenspektrometrie, um diese Moleküle zu isolieren und zu identifizieren. Überraschenderweise änderte sich die Gesamtmenge des neu gebildeten Proteins nach mehreren Tagen mit niedriger Amyloid‑Beta‑Dosis weder mit noch ohne eFT508. Betrachtete man jedoch, welche spezifischen Proteine produziert wurden, zeigte sich ein anderes Bild: Es wurden über tausend neu gemachte Proteine detektiert, und Dutzende davon waren als Reaktion auf Amyloid‑Beta nach oben oder unten reguliert. Viele betrafen die synaptische Kommunikation, das zelluläre Gerüst, energieproduzierende Mitochondrien, Abfallbeseitigungssysteme und die Qualitätskontrolle von Proteinen.
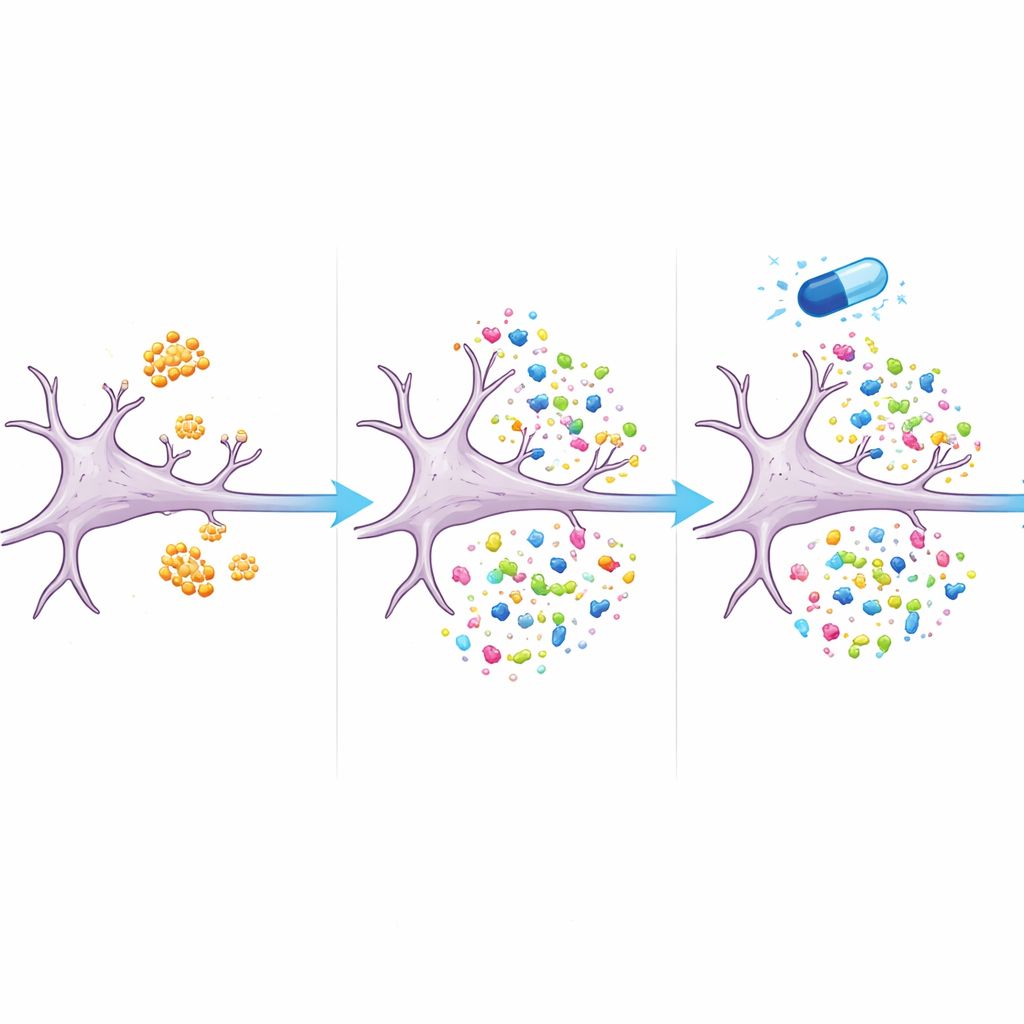
Ein Medikament, das das Proteingleichgewicht steuert
Entscheidend ist, dass viele der gestörten Proteine wieder in Richtung Normalwerte verschoben wurden, wenn die Zellen neben Amyloid‑Beta auch mit eFT508 behandelt wurden. Mehr als zwei Drittel der durch Amyloid‑Beta allein veränderten Proteine wiesen in Anwesenheit des Medikaments keine signifikanten Unterschiede zu unbehandelten Zellen mehr auf. Dazu gehörten Proteine, die mit Struktur und Funktion von Synapsen verbunden sind, sowie Komponenten der zellulären Recycling‑ und Energiesysteme. Die Ergebnisse legen nahe, dass eFT508 nicht einfach die Proteinsynthese herunterfährt; vielmehr scheint es die Zusammensetzung der produzierten Proteine umzulenken und das System von einem Alzheimer‑ähnlichen Muster zu einem gesünderen Gleichgewicht zu bewegen.
Was das für zukünftige Behandlungen bedeuten könnte
Diese Arbeit zeichnet das Bild eines frühen Alzheimer‑bezogenen Schadens als eine Phase von Übervernetzung und subtiler Fehlsteuerung der Proteinproduktion, statt eines unmittelbaren Verlusts. Niedrige Amyloid‑Beta‑Spiegel treiben die Bildung zusätzlicher, teils ungewöhnlicher Synapsen voran und verzerren selektiv das Spektrum der von Nervenzellen hergestellten Proteine. In diesem Modell in der Schale kann eFT508 sowohl die Synapsenzahlen normalisieren als auch viele der Proteinveränderungen korrigieren, was nahelegt, dass ein gezieltes Abstimmen der Proteinsynthese das Fortschreiten von leichter kognitiver Beeinträchtigung zur voll ausgeprägten Demenz verlangsamen oder verhindern könnte. Obwohl noch viel in lebenden Tieren und Menschen geprüft werden muss, hebt die Studie eine neue Denkweise über – und möglicherweise ein Eingreifen in – die frühesten Stadien der Alzheimer‑Krankheit hervor.
Zitation: Wu, K., Lee, S., Martinez-Serra, R. et al. Low concentrations of amyloid-beta oligomers induce synaptogenesis characteristic for mild cognitive impairment and alter the de novo proteome. Transl Psychiatry 16, 132 (2026). https://doi.org/10.1038/s41398-026-03905-x
Schlüsselwörter: Alzheimer‑Krankheit, Synapsenveränderungen, Amyloid‑Beta‑Oligomere, Proteinsynthese, frühe Neurodegeneration