Clear Sky Science · de
Kartierung heterogener struktureller Gehirn-Subtypen bei Alzheimer-Erkrankung und leichter kognitiver Beeinträchtigung mittels normativer Modelle
Warum diese Forschung für die Gehirngesundheit wichtig ist
Alzheimer-Erkrankung und ihre frühe Warnstufe, die leichte kognitive Beeinträchtigung, sehen nicht bei jedem Patienten gleich aus. Manche Menschen verschlechtern sich schnell, andere langsamer; einige zeigen ausgeprägte Schrumpfung des Gehirns, andere deutlich weniger. Diese Studie stellt eine praktische Frage mit großen Auswirkungen für Familien und Ärztinnen und Ärzte: Lassen sich Gehirnscans systematisch nutzen, um diese individuellen Unterschiede zu kartieren, sodass man erkennen kann, welche Patienten einen aggressiveren Verlauf haben und die Versorgung entsprechend anpassen kann?
Jedes Gehirn mit einer „Wachstumstabelle“ vergleichen
Statt Patientinnen und Patienten mit Alzheimer einfach mit einer Kontrollgruppe zu vergleichen, bauten die Forschenden etwas Ähnliches wie pädiatrische Wachstumstabellen — allerdings für das Gehirn. Anhand von MRT-Scans von mehr als tausend gesunden Erwachsenen im Alter von 18 bis 92 Jahren modellierten sie, wie sich das Graue-Materie-Volumen in 90 Hirnregionen typischerweise mit dem Alter bei Männern und Frauen verändert. Dieses „normative Modell“ definiert den erwarteten Bereich für jede Region in Abhängigkeit von Alter und Geschlecht. Für jede Person in großen Alzheimer-Datensätzen berechneten sie dann, wie stark die Hirnvolumina dieser Person regionsweise von dem abwichen, was für sie typisch wäre. Das Ergebnis ist eine personalisierte Karte, die zeigt, wo das Gehirn für die jeweilige Lebensphase ungewöhnlich geschrumpft oder erhalten ist.
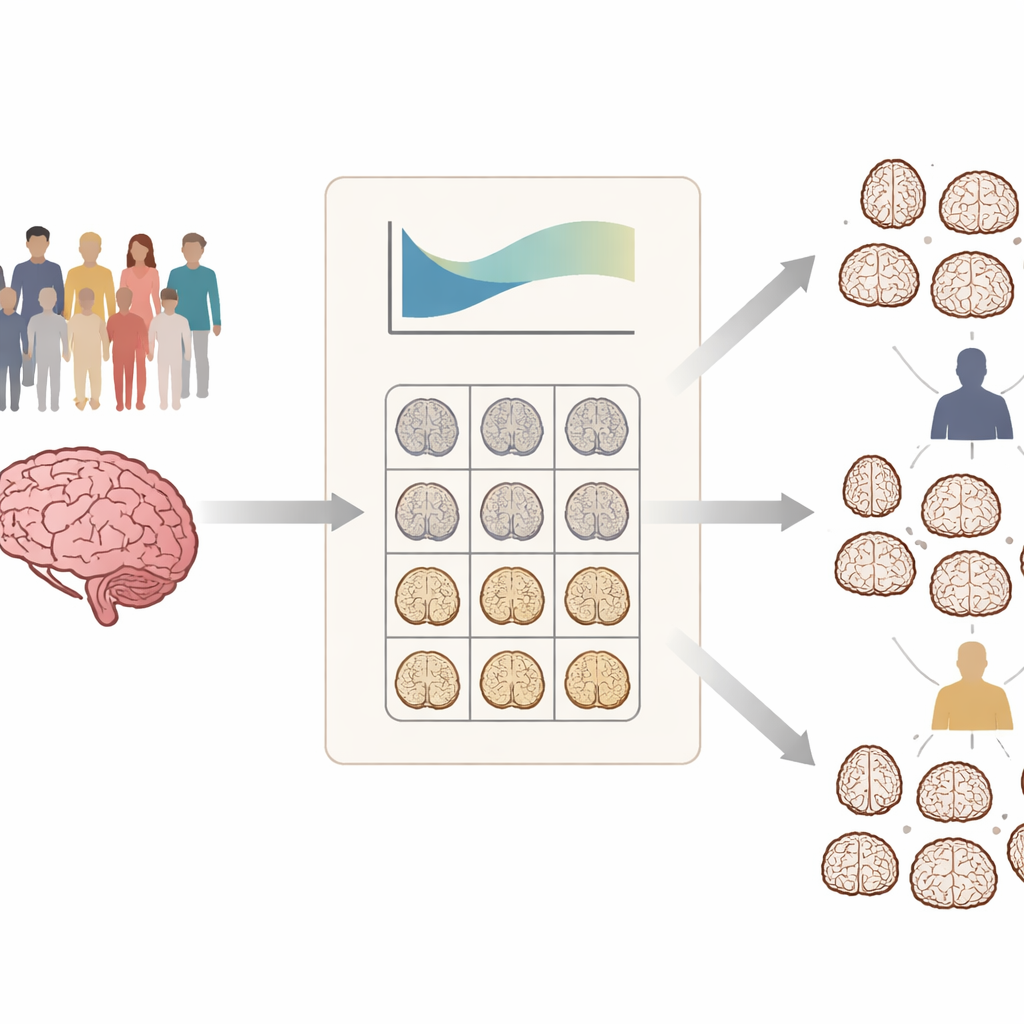
Zwei Hauptmuster der Gehirnveränderung bei Patienten
Als das Team diesen Ansatz bei hunderten Menschen mit leichter kognitiver Beeinträchtigung und Alzheimer anwandte, zeigte sich eine große Variabilität: Nicht alle Patientinnen und Patienten wiesen dieselben Schrumpfungsbereiche auf, und die Schweregrade variierten stark. Durch Clustering nach den Abweichungskarten identifizierten sie in beiden Krankheitsbildern konsistent zwei strukturelle Subtypen. Ein Subtyp zeigte relativ milde Abweichungen vom Normalen, während der andere deutlich stärkere negative Abweichungen aufwies, vor allem in tief liegenden, an Gedächtnis beteiligten Strukturen wie Hippocampus, Parahippocampus und Amygdala. Diese „stark abweichenden“ Gehirne waren in vielen Regionen deutlich stärker geschrumpft als für Alter und Geschlecht zu erwarten.
Verknüpfung von Gehirnmustern mit Kognition, Biomarkern und Verlauf
Die strukturellen Subtypen waren nicht bloß abstrakte Muster auf einem Scan; sie korrespondierten eng mit klinischen Unterschieden. Personen des schweren Subtyps schnitten bei Gedächtnis- und Denktests schlechter ab, zeigten auf PET-Aufnahmen eine niedrigere Gehirnstoffwechselrate und hatten häufiger auffällige Werte Alzheimer-assoziierter Proteine im Liquor. Über Jahre der Nachbeobachtung verschlechterten sie sich zudem schneller auf standardisierten kognitiven Skalen. Bei Menschen mit leichter kognitiver Beeinträchtigung ging der schwere Subtyp mit einem höheren Risiko einher, in eine volle Alzheimer-Erkrankung überzugehen, und dies schneller als beim milderen Subtyp. Wichtig ist, dass Individuen tendenziell ihren Subtyp beibehielten: Patienten, die in der milderen strukturellen Gruppe begannen, entwickelten meist auch einen milderen Alzheimer-Verlauf, während diejenigen aus der stärker geschädigten Gruppe überwiegend in den aggressiveren Alzheimer-Subtyp übergingen.
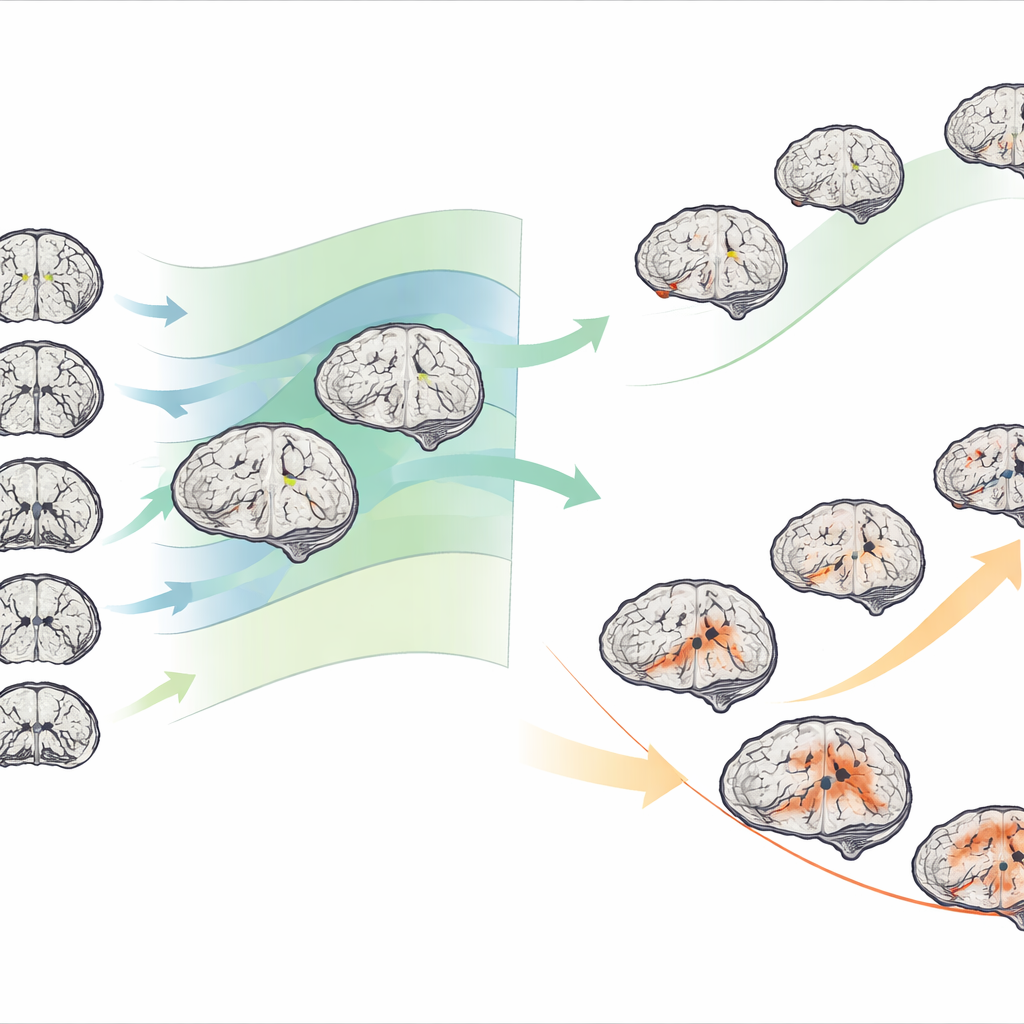
Von Gehirnkarten zur zugrunde liegenden Biologie
Um zu untersuchen, warum diese Muster unterschiedlich sind, verglichen die Autorinnen und Autoren die regionalen Schrumpfungskarten mit detaillierten Genaktivitätskarten aus gespendeten menschlichen Gehirnen. Sie fanden, dass die in den einzelnen Subtypen am stärksten betroffenen Bereiche dazu neigten, bestimmte Genmuster zu exprimieren, die an neuronalen Verbindungen und Kommunikation sowie an Zelltypen beteiligt sind, die mit Blutgefäßen und Myelin assoziiert sind. Der schwere Subtyp zeigte besonders starke Verknüpfungen zu Genen, die mit neuronalen Projektionen und Synapsen in Zusammenhang stehen, was darauf hindeutet, dass der Zusammenbruch dieser Systeme seinen aggressiveren Verlauf antreiben könnte. Außerdem bestätigten sie, dass Trägerinnen und Träger der genetischen Risikovariante APOE ε4 tendenziell stärkere negative Abweichungen und schnelleren strukturellen Verlust aufwiesen, insbesondere in der Phase der leichten kognitiven Beeinträchtigung.
Hin zu einer zielgenaueren Versorgung bei Alzheimer
Insgesamt zeigt die Studie, dass der sorgfältige Vergleich des individuellen Gehirns mit einem gut charakterisierten „Normalbereich“ aussagekräftige Subtypen von Alzheimer-Erkrankung und leichter kognitiver Beeinträchtigung offenlegen kann. Diese Subtypen unterscheiden sich in Gehirnstruktur, kognitiven Fähigkeiten, Krankheitsmarkern und Verlaufsgeschwindigkeit und scheinen in unterschiedlichen molekularen Signaturen verwurzelt zu sein. Für Patientinnen, Patienten und Klinikerinnen und Kliniker deutet dies darauf hin, dass künftige diagnostische Werkzeuge solche individualisierten Gehirnkarten nutzen könnten, um Hochrisikopersonen früher zu identifizieren, passendere Überwachungsintervalle oder Therapieansätze zu wählen und Studien so zu gestalten, dass Teilnehmende nach biologischen Subtypen und nicht nur nach einer breiten Diagnose gruppiert werden.
Zitation: Wei, X., Zhang, T., Xiong, R. et al. Mapping heterogeneous brain structural subtypes in alzheimer’s disease and mild cognitive impairment using normative models. Transl Psychiatry 16, 168 (2026). https://doi.org/10.1038/s41398-026-03902-0
Schlüsselwörter: Alzheimer-Erkrankung, leichte kognitive Beeinträchtigung, Hirn-MRT, normative Modellierung, personalisierte Neurologie