Clear Sky Science · de
Pränatale und postnatale Auswirkungen mütterlicher Immunaktivierung auf synaptische und neuroentwicklungsbezogene Pfade über epigenetische Mechanismen
Wie das Immunsystem der Mutter das Gehirn des Kindes formt
Infektionen während der Schwangerschaft werden seit langem mit einem erhöhten Risiko für Erkrankungen wie Schizophrenie, Autismus und ADHS bei Kindern in Verbindung gebracht, doch die biologische „Brücke“ zwischen einer erkrankten Mutter und einem später verletzlichen Gehirn war bisher unklar. Diese Studie verwendet Mäuse, um zu zeigen, wie die Immunantwort einer Mutter auf Grippe während der Schwangerschaft langanhaltende chemische Spuren im sich entwickelnden Gehirn hinterlassen kann, die die Kommunikation der Gehirnzellen verändern und potenziell das Risiko für spätere psychische und neurologische Probleme erhöhen.
Erkrankung in der Schwangerschaft und lebenslanges Hirnrisiko
Epidemiologische Studien beim Menschen haben gezeigt, dass Kinder von Frauen, die während der Schwangerschaft Infektionen durchmachten, im Erwachsenenalter häufiger eine Reihe psychiatrischer und neuroentwicklungsbezogener Störungen entwickeln. Die Autoren konzentrieren sich auf die mütterliche Immunaktivierung, die Kaskade von Immunsignalen, die freigesetzt wird, wenn der Körper eine Infektion bekämpft. Diese Signale können die Plazenta beeinflussen oder passieren und mit dem sich entwickelnden Gehirn in einer Phase interagieren, in der Schaltkreise angelegt werden. Der Frontalkortex – entscheidend für Planung, Entscheidungsfindung und emotionale Kontrolle – entwickelt sich über einen langen Zeitraum und ist besonders empfindlich gegenüber frühen Störungen.
Unterscheidung von vorgeburtlichen und nachgeburtlichen Effekten
Um zu trennen, was im Mutterleib von dem zu unterscheiden, was nach der Geburt geschieht, infizierten die Forschenden trächtige Mäuse mit einem milden, nicht tödlichen Influenzavirus während einer frühen Gestationsphase, die dem Ende des ersten Trimesters beim Menschen entspricht. Einige Welpen blieben bei ihren Geburtsmüttern, andere wurden innerhalb von 24 Stunden nach der Geburt zu Pflegemüttern gegeben. Dadurch entstanden vier Gruppen: Nachkommen ohne Exposition vor oder nach der Geburt, nur vorgeburtlich exponierte, nur postnatal exponierte und in beiden Zeiträumen exponierte Nachkommen. Als die Tiere das Erwachsenenalter erreichten, untersuchte das Team Neuronen aus dem Frontalkortex und betrachtete sowohl Genaktivität als auch „epigenetische“ Markierungen – chemische Tags an den DNA-verpackenden Proteinen, die helfen zu steuern, welche Gene ein- oder ausgeschaltet werden. 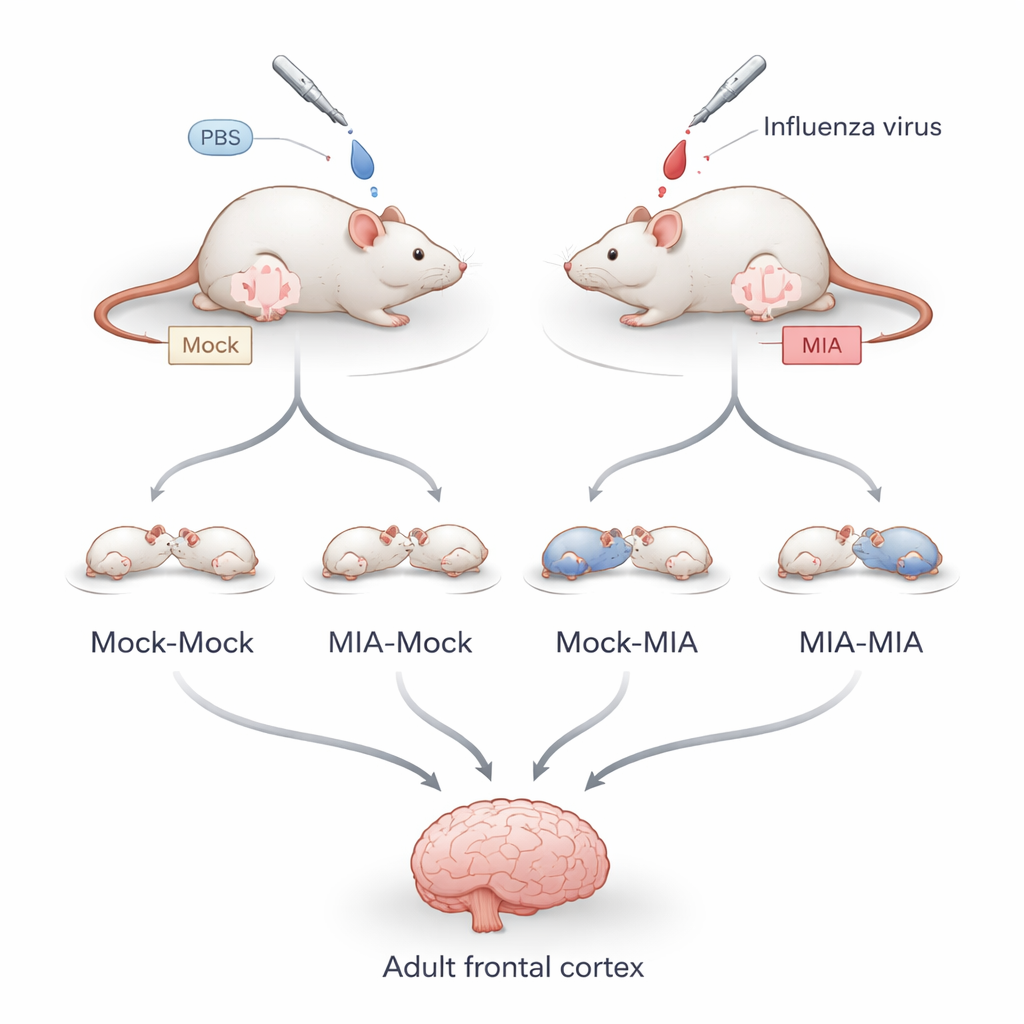
Anhaltende chemische Spuren auf der DNA des Gehirns
Die Studie konzentrierte sich auf zwei Histonmarken, H3K27ac und H3K4me3, die aktive Schalter und Startpunkte für Gene markieren. Mit empfindlichen Sequenziermethoden kartierten die Autoren Zehntausende dieser regulatorischen Regionen und maßen, welche Gene in den einzelnen Gruppen stärker oder schwächer aktiv waren. Sie fanden heraus, dass mütterliche Immunaktivierung vor der Geburt weitreichende und anhaltende Veränderungen in Enhancer-Regionen – DNA-Abschnitten, die als Einstellräder für Genaktivität fungieren – verursachte. Diese Veränderungen waren besonders angereichert in Genen, die am Aufbau des Vorderhirns, der Führung wachsender Nervenfasern und der Einrichtung früher Kommunikationspunkte zwischen Neuronen beteiligt sind. Viele derselben Gene zeigten auch nach der Geburt veränderte Aktivität, wenn die Welpen von immunaktivierten Müttern aufgezogen wurden, was auf eine anhaltende regulatorische Entwicklung über die Zeit statt auf einen kurzlebigen Schock hinweist.
Von epigenetischen Verschiebungen zu Synapsen- und Schaltkreisveränderungen
Sowohl vor- als auch postnatale Expositionen beeinflussten molekulare Pfade, die steuern, wie Neuronen miteinander kommunizieren. Gene, die mit Glutamat (dem wichtigsten exzitatorischen Neurotransmitter), GABA (dem wichtigsten inhibitorischen Neurotransmitter) und Dopamin (wichtig für Motivation und Belohnung) verbunden sind, zeigten koordinierte Veränderungen in ihren regulatorischen Elementen und Expressionsniveaus. Diese Systeme werden wiederholt mit Schizophrenie, Depression, Autismus und Sucht in Verbindung gebracht. Die Autoren fanden auch Veränderungen in Genen, die an Synapsenorganisation, Axonwachstum und der Verfeinerung von Hirnschaltkreisen beteiligt sind, besonders nach postnataler Exposition. Das deutet darauf hin, dass mütterliches Verhalten und anhaltende immunbezogene Veränderungen nach der Geburt die Verdrahtung und Feinabstimmung neuronaler Netzwerke mitformen. Netzwerkanalysen hoben einen Kern von Transkriptionsfaktoren – Masterregulatoren der Genaktivität – hervor, die in beiden Zeitfenstern gestört waren.
Bezüge zum psychiatrischen Risiko beim Menschen
Um zu prüfen, wie relevant diese Mausveränderungen für menschliche Erkrankungen sind, überführten die Forschenden die Maus-Enhancer- und Promotor-Positionen in ihre nächstliegenden menschlichen Gegenstücke und verglichen sie mit großen genetischen Studien psychiatrischer Störungen. Von mütterlicher Immunaktivierung veränderte Regionen zeigten eine starke Anreicherung in menschlichen Risikoloci für Schizophrenie, bipolare Störung, Depression, Neurotizismus und ADHS, jedoch nicht in den meisten nicht-psychiatrischen Erkrankungen. Dieses Muster legt nahe, dass dieselben Arten regulatorischer DNA-Regionen, die vererbtes genetisches Risiko für psychische Erkrankungen tragen, auch empfindlich gegenüber immunologischen Herausforderungen während der Schwangerschaft und im frühen Leben sind und damit einen Konvergenzpunkt für Gene und Umwelt bilden.
Was das für die menschliche Gesundheit bedeutet
Für eine allgemeine Leserschaft lautet die Hauptbotschaft, dass die Immunantwort einer Mutter – nicht nur die Infektion selbst – dauerhafte „Notizen am Rand“ im Anleitungsbuch des sich entwickelnden Gehirns hinterlassen kann. Diese epigenetischen Notizen, geschrieben vor und kurz nach der Geburt, können subtil beeinflussen, wie Gehirnzellen wachsen und in Schaltkreisen miteinander kommunizieren, die Denken, Stimmung und Verhalten steuern. Während die meisten Kinder erkrankter Mütter keine psychiatrischen Störungen entwickeln werden, trägt diese Arbeit dazu bei zu erklären, warum manche anfälliger sein könnten, und unterstreicht die Bedeutung der Prävention und Behandlung von Infektionen und Entzündungen während der Schwangerschaft und im frühen Leben als Teil langfristiger Gehirngesundheit.
Zitation: Zhu, B., Li, G., Saunders, J.M. et al. Prenatal and postnatal effects of gestational immune activation on synaptic and neurodevelopmental pathways via epigenetic mechanisms. Transl Psychiatry 16, 82 (2026). https://doi.org/10.1038/s41398-026-03884-z
Schlüsselwörter: mütterliche Immunaktivierung, Epigenetik, Neuroentwicklung, synaptische Signalübertragung, psychiatrisches Risiko