Clear Sky Science · de
Biologische Grundlagen und genetische Veranlagung für Schizophrenie innerhalb der miR-137-Regulationswege während der Gehirnentwicklung
Wie ein winziges Molekül das Schizophrenierisiko beeinflussen kann
Schizophrenie gilt oft als rätselhaftes Hirnleiden, das sich im späten Jugendalter oder frühen Erwachsenenalter zeigt, doch ihre Wurzeln reichen möglicherweise bis in die vorgeburtliche Zeit zurück. Dieser Artikel untersucht, wie ein kleines regulatorisches Molekül, die microRNA-137 (miR-137), die Entwicklung und Kommunikation von Gehirnzellen beeinflussen kann und damit sowohl die Wahrscheinlichkeit, an Schizophrenie zu erkranken, als auch die Art der auftretenden Symptome mitgestaltet. Indem die Wirkungen von miR-137 vom pränatalen Gehirn bis ins Erwachsenenalter nachgezeichnet werden, wollen die Forschenden klären, warum einige Personen anfälliger für Psychosen und verwandte psychische Erkrankungen sind.
Ein winziger Regulator mit großer Wirkung
MiR-137 ist ein kurzes RNA-Stück, das selbst keine Proteine codiert, sondern als Feinregler anderer Gene fungiert. Es bestimmt mit, wann und wie stark viele gehirnbezogene Gene ein- oder ausgeschaltet werden. Frühere genetische Studien zeigten, dass häufige Varianten in der Nähe des MIR137-Gens zu den stärksten bekannten Risikofaktoren für Schizophrenie gehören. Viele der Gene, die von miR-137 reguliert werden, sind an Aufbau von Neuronen, Ausformung ihrer Verzweigungen und an der Bildung von Synapsen — den Verbindungsstellen, über die Nervenzellen kommunizieren — beteiligt. Allerdings beruhten die meisten früheren Arbeiten auf Computerprognosen oder stark vereinfachten Zellmodellen, die übersehen können, dass miR-137 in verschiedenen Entwicklungsphasen und Hirnregionen unterschiedlich wirkt.
Direkter Blick ins menschliche Gehirn
Um ein realistischeres Bild zu gewinnen, konzentrierten sich die Autorinnen und Autoren auf „direkte Zielgene“ von miR-137, die in tatsächlichem menschlichem Hirngewebe mit einer Methode identifiziert wurden, die physisch abbildet, wo miRNAs an ihre Zielgene binden. Sie kombinierten Daten aus zwei wichtigen Zeiträumen: der frühen pränatalen Entwicklung und dem Erwachsenenalter. Daraus bauten sie zwei getrennte Genmengen auf: eine pränatale Zielgruppe und eine adulte Zielgruppe. Diese verglichen sie dann mit mehreren traditionelleren Sets, die aus Computer-Vorhersagen oder Labormanipulationen an Zellen stammten. Mit verschiedenen statistischen Methoden untersuchten sie, wie jede Genmenge in Hirnregionen und Lebensphasen exprimiert wird, in welchen Zelltypen sie vorkommt und wie stark sie mit genetischem Risiko für Schizophrenie und verwandte Störungen überlappt.
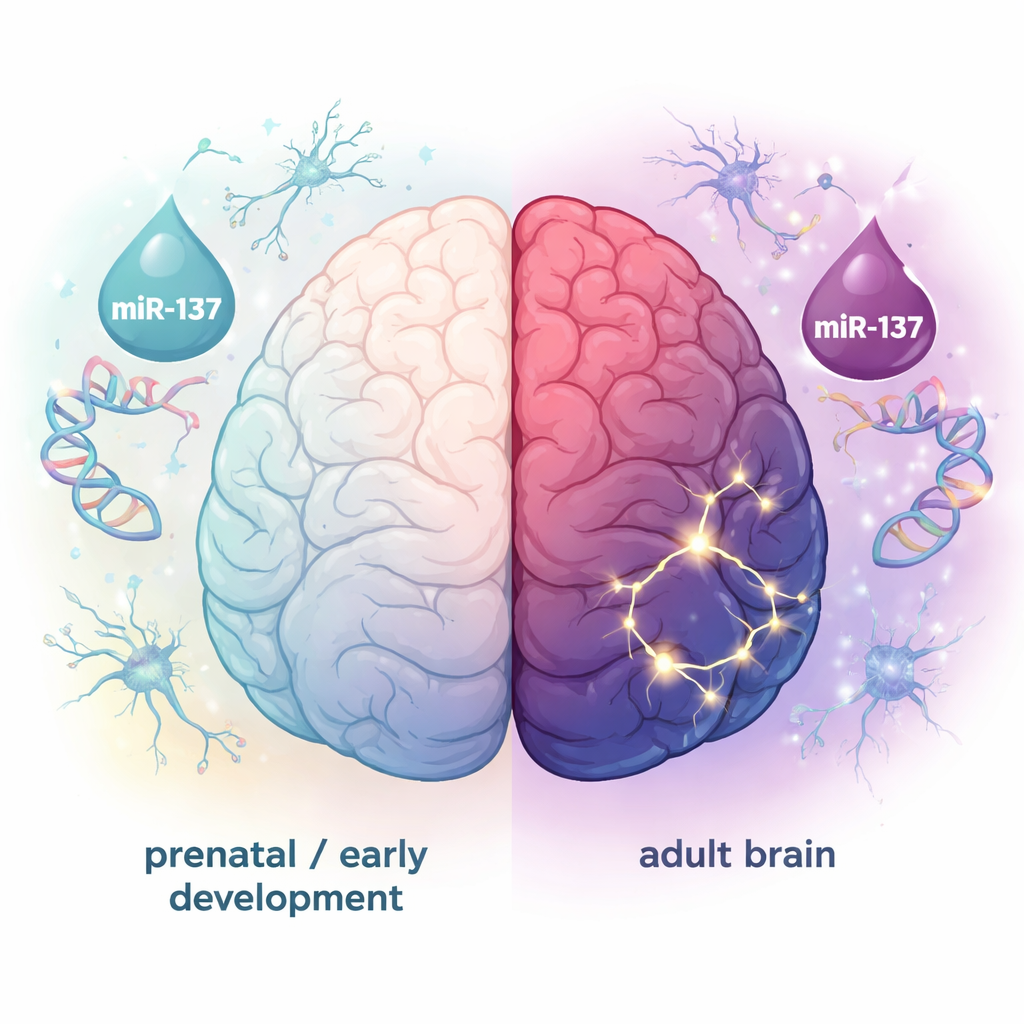
Verschiedene Stadien, verschiedene Hirnfunktionen
Die pränatalen und adulten miR-137-Zielgruppen erwiesen sich größtenteils als unterschiedlich und teilten nur eine kleine Anzahl von Genen. Pränatale Ziele standen am stärksten mit frühen Aufbauaufgaben des Gehirns in Verbindung, etwa der Erzeugung neuer Neuronen und Gliazellen und der Steuerung ihrer ersten Entwicklungsschritte. Ihre Aktivität war vergleichsweise hoch in frühen Lebensphasen und ging danach zurück, mit einer bemerkenswerten Ausnahme im erwachsenen Kleinhirn. Im Gegensatz dazu waren adulte Ziele angereichert für Gene, die an Synapsen, Neuriten und der zellulären Kommunikation beteiligt sind. Diese Gene waren in vielen Hirnregionen des Erwachsenen besonders aktiv, vor allem in Neuronen und Oligodendrozyten, und ihre Expression erreichte häufig einen Höhepunkt im jungen Erwachsenenalter — genau zu der Zeit, in der Schizophrenie oft erstmals auftritt. Andere, breiter prognostizierte Genmengen zeigten dieses klare entwicklungs- und zellspezifische Muster nicht.
Verknüpfung von Genregulation mit Krankheit und Symptomen
Beim Vergleich von Menschen mit Schizophrenie und Unbetroffenen fanden die Forschenden, dass viele adulte miR-137-Zielgene in Patientenhirngewebe durchgehend weniger aktiv waren. Ähnliche Erniedrigungen zeigten sich bei bipolaren Störungen und Autismus, was auf ein gemeinsames molekulares Muster bei schweren psychiatrischen Erkrankungen hindeutet. Genetische Analysen stützten dieses Bild: Sowohl pränatale als auch adulte miR-137-Zielgene wiesen ungewöhnlich viele häufige Risikovarianten für Schizophrenie auf, und adulte Ziele deckten zusätzlich ein gemeinsames genetisches Risiko ab, das Schizophrenie, bipolare Störung, Depression und Autismus umfasst. Wichtig war, dass polygenetische Scores, die auf diese Zielgene beschränkt waren und in einer großen spanischen Stichprobe berechnet wurden, zeigten: Scores auf Basis adulter Ziele halfen, Patienten von Kontrollen zu unterscheiden, während Scores auf Basis pränataler Ziele besonders mit der Schwere „negativer“ Symptome wie emotionaler Verflachung, Antriebsverlust und sozialem Rückzug verbunden waren.
Was das Verständnis der Schizophrenie bedeutet
Für Nicht-Fachleute lautet die Kernbotschaft, dass miR-137 nicht als einfacher An/Aus-Schalter für Schizophrenie wirkt, sondern Teil eines beweglichen Steuerpults ist, das seinen Einfluss vom pränatalen Leben bis ins Erwachsenenalter verändert. In der frühen Entwicklung scheint miR-137 die Grundstruktur neuronaler Schaltkreise zu formen, und erblich bedingte Variationen in seinen pränatalen Zielgenen könnten einige Personen gegenüber späteren schweren negativen Symptomen anfälliger machen. Im erwachsenen Gehirn gruppieren sich miR-137-Ziele in Synapsen und Kommunikationswegen, die genetisch über mehrere psychiatrische Erkrankungen geteilt werden. Durch die Fokussierung auf direkte, zeitlich spezifische Zielgene in menschlichem Hirngewebe schärft diese Arbeit unseren Blick darauf, wie ein einzelner Regulationsweg sowohl zum Psychoserisiko als auch zur konkreten Ausprägung beitragen kann und damit Wege für gezieltere Präventions- und Behandlungsstrategien eröffnet.
Zitation: Stella, C., De Hoyos, L., Mora, A. et al. Biological underpinnings and genetic predisposition to schizophrenia within microrna-137 regulatory pathways across brain development. Transl Psychiatry 16, 91 (2026). https://doi.org/10.1038/s41398-026-03859-0
Schlüsselwörter: Schizophrenie, microRNA-137, Gehirnentwicklung, genetisches Risiko, synaptische Funktion