Clear Sky Science · de
METTL3-vermittelte m6A-Modifikation reguliert CDKN1A und mildert chronisch schlafentzugsbedingte kognitive Beeinträchtigung und neuronalen Zelltod bei Ratten
Warum schlaflose Nächte Ihrem Gedächtnis schaden können
Viele Menschen schreiben chronischen Schlafmangel als normalen Bestandteil des modernen Lebens ab, doch die Forschung zeigt, dass fehlender Schlaf heimlich Hirnareale schädigen kann, die Lernen und Gedächtnis stützen. Diese Studie an Ratten geht bis auf die Ebene einzelner Moleküle in Hippokampus-Neuronen und identifiziert einen spezifischen chemischen Schalter – genannt METTL3 –, der offenbar die Gehirnzellen vor den schädlichen Folgen chronischen Schlafentzugs schützt. Das Verständnis dieses Schalters könnte langfristig zu neuen Ansätzen führen, um das Gedächtnis von Menschen zu schützen, die Schlafverlust kaum vermeiden können, etwa Schichtarbeiter, Pflegepersonen oder Patienten mit Schlafstörungen.
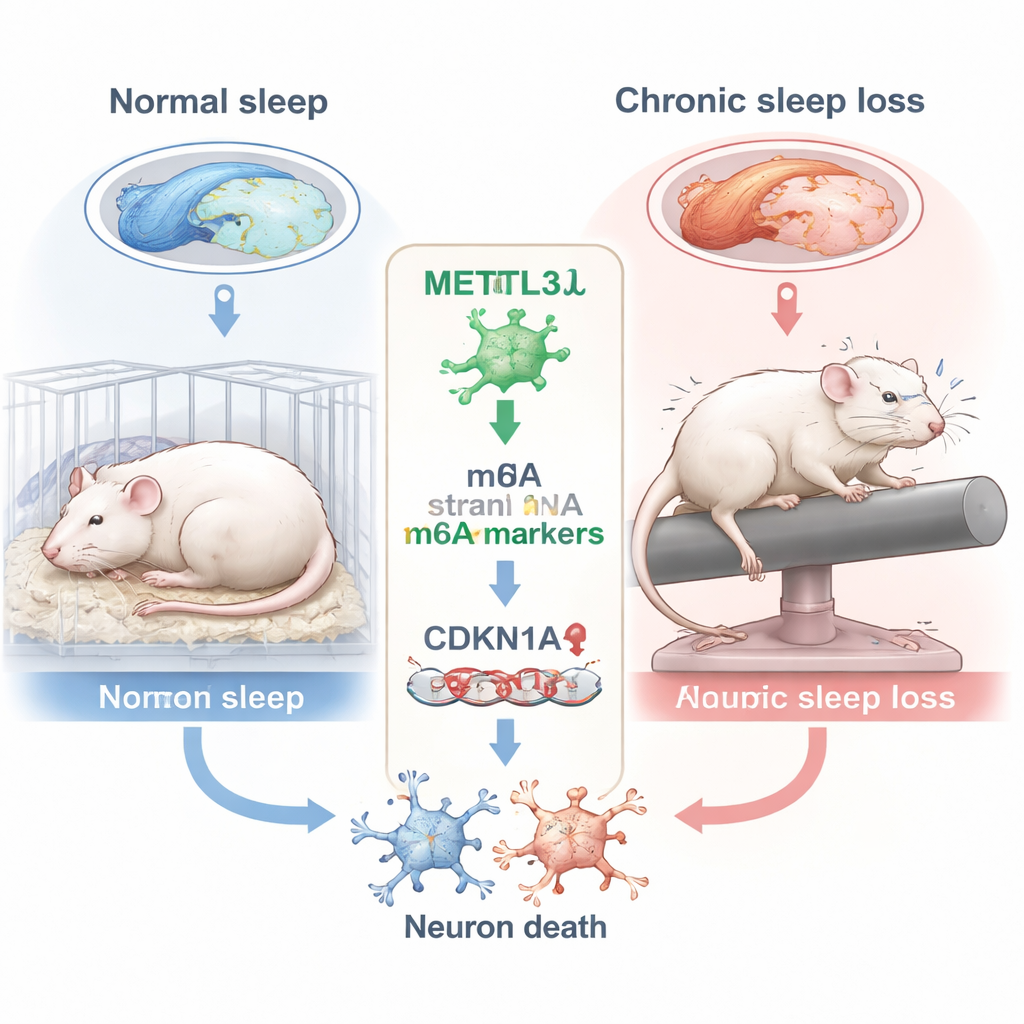
Wie langfristiger Schlafmangel das Gedächtniszentrum schädigt
Die Forschenden konzentrierten sich auf den Hippokampus, eine seepferdchenförmige Hirnregion, die für die Bildung neuer Erinnerungen essenziell ist. Innerhalb des Hippokampus zoomten sie auf eine Unterregion namens CA3, die beim Kodieren und Abrufen räumlicher Information hilft – Fähigkeiten, die bei Aufgaben wie dem Finden einer verborgenen Plattform im Wasser getestet werden. Die Ratten wurden über sechs Wochen an zehn Stunden pro Tag wachgehalten, indem eine sanft rotierende Stange sie wiederholt aus dem Schlaf weckte. Im bekannten Morris-Wasserlabyrinth nahmen schlafentzogene Ratten weniger direkte Routen, überquerten den früheren Plattformstandort seltener und verbrachten weniger Zeit im Zielquadranten – alles Anzeichen für eine beeinträchtigte räumliche Erinnerung im Vergleich zu gut erholten Tieren.
Eine chemische Markierung auf RNA, die verschwindet
Um zu verstehen, was in CA3-Neuronen vor sich ging, analysierte das Team eine chemische Markierung auf RNA namens m6A, eine der häufigsten internen Modifikationen auf messenger-RNA. Diese Markierungen helfen zu steuern, wie lange RNA-Moleküle bestehen und wie effizient sie zur Proteinsynthese genutzt werden. Ein Schlüsselenzym, das m6A-Markierungen hinzufügt, ist METTL3. Mithilfe hochdurchsatzfähiger m6A-Sequenzierung und Genexpressionsanalyse fanden die Forschenden heraus, dass chronischer Schlafentzug METTL3 in der CA3-Region signifikant reduzierte. Dieser Rückgang ließ sich sowohl auf RNA- als auch auf Proteinebene bestätigen. Das Muster der betroffenen Gene deutete auf Störungen in der Zellzykluskontrolle und Stressantworten hin, was nahelegt, dass Schlafverlust Neurone in ungesunde Zustände treiben könnte.
Vom molekularen Wandel zum Neuronensterben
Um zu sehen, wie niedrigeres METTL3 Neurone direkt beeinflussen könnte, wandten sich die Forschenden kultivierten Maus-Hippokampuszellen in Zellkultur zu. Als sie mittels kleiner interferierender RNAs METTL3 stilllegten, wurden die Zellen deutlich anfälliger für eine schädigende Behandlung mit Rapamycin, einem Neuron-stressenden Wirkstoff. Diese METTL3-depletierten Zellen zeigten höhere Spiegel klassischer „Zell-Selbstmord“-Proteine wie Bax und gespaltene Caspase-3, und mehr Zellen wurden in der Durchflusszytometrie als apoptotisch markiert. Tiefere RNA-Analysen wiesen auf ein einzelnes Gen, CDKN1A (das das Protein p21 kodiert), als Schlüsselakteur hin: Beim Herunterfahren von METTL3 stiegen die CDKN1A-Spiegel stark an.
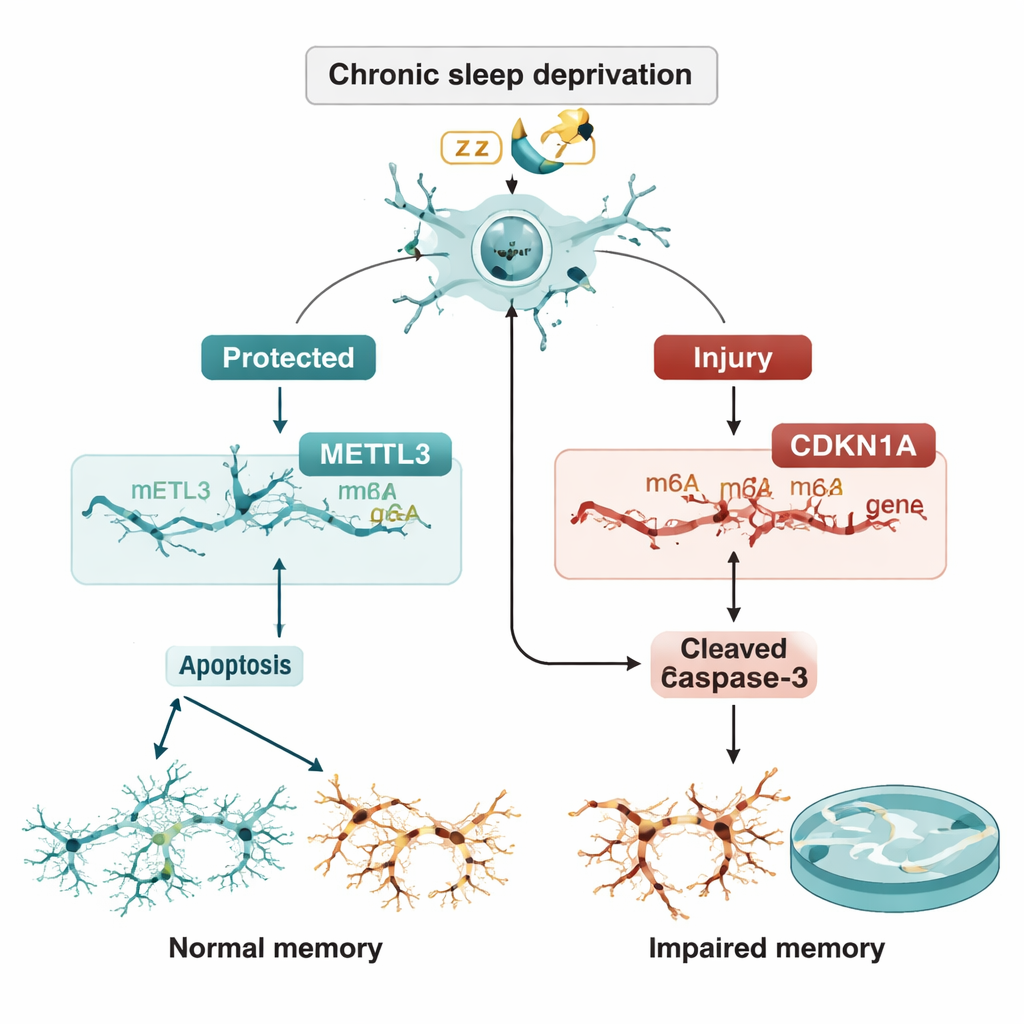
Ein fragiles Gleichgewicht zwischen Schutz und Selbstzerstörung
Das Team untersuchte dann, ob METTL3 CDKN1A über m6A-Markierung steuert. Sie zeigten, dass die Reduktion von METTL3 die m6A-Marken auf CDKN1A-RNA verringerte und diese RNA stabiler machte, sodass ihre Mengen anstiegen statt abgebaut zu werden. Höhere CDKN1A-Werte trieben wiederum Neurone in Richtung Apoptose. Entscheidenderweise wurde der zusätzliche Zelltod durch Verlust von METTL3 weitgehend aufgehoben, wenn CDKN1A selbst herunterreguliert wurde. In lebenden Ratten führte das gezielte Einbringen von zusätzlichem METTL3 direkt in die CA3-Region mittels eines viralen Vektors zu niedrigeren CDKN1A-Spiegeln, verringter Häufigkeit von Apoptose-Proteinen, Erhalt der neuronalen Struktur in Gewebefärbungen und verbesserter Leistung im Wasserlabyrinth trotz anhaltendem Schlafverlust.
Was das für Menschen bedeutet, die nicht genug schlafen
Kurz gesagt: Chronischer Schlafentzug scheint ein schützendes Enzym, METTL3, in einer kritischen Gedächtnisschaltung des Gehirns zu dämpfen. Fällt METTL3, kann es bestimmte RNAs nicht mehr korrekt markieren, insbesondere jene, die CDKN1A kodiert. Diese RNA sammelt sich dann an, treibt Neurone in programmierte Zelltodprozesse und trägt zu Gedächtnisproblemen bei. Durch die Wiederherstellung von METTL3 konnten die Forschenden CDKN1A wieder herunterregulieren, neuronalen Verlust verringern und das Gedächtnis bei schlafentzogenen Ratten retten. Auch wenn diese Arbeit noch am Tiermodell steht, identifiziert sie den METTL3–CDKN1A-Weg als vielversprechendes Ziel für künftige Medikamente, die das Gehirn vor den kognitiven Folgen chronischen Schlafmangels schützen sollen.
Zitation: Xing, F., Shi, XS., Gu, HW. et al. METTL3-mediated m6A modification regulates CDKN1A to attenuate chronic sleep deprivation-induced cognitive impairment and neuronal apoptosis in rats. Transl Psychiatry 16, 96 (2026). https://doi.org/10.1038/s41398-026-03855-4
Schlüsselwörter: chronischer Schlafentzug, Hippokampus, RNA-Methylierung, neuronaler Zelltod, Gedächtnisstörung