Clear Sky Science · de
Akute Effekte selektiver Serotonin-Wiederaufnahmehemmer auf den zerebralen Glukosestoffwechsel und die Durchblutung
Warum das für Menschen, die Antidepressiva einnehmen, wichtig ist
Selektive Serotonin-Wiederaufnahmehemmer (SSRIs) gehören zu den am häufigsten verschriebenen Antidepressiva, doch wir verstehen noch nicht vollständig, wie sie die Gehirnaktivität in den Minuten nach einer Dosis verändern. Diese Studie blickt bei gesunden Freiwilligen unter die Haube und nutzt fortgeschrittene Hirnbildgebung, um zu sehen, wie eine intravenöse Gabe des SSRI Citalopram den Energieverbrauch und die Durchblutung des Gehirns verändert. Die Ergebnisse helfen zu klären, was diese Medikamente in wichtigen Stimmungs- und sensorischen Regionen bewirken, und stellen die Vorstellung infrage, dass ihre unmittelbaren Effekte bloß Veränderungen der Blutzirkulation sind.
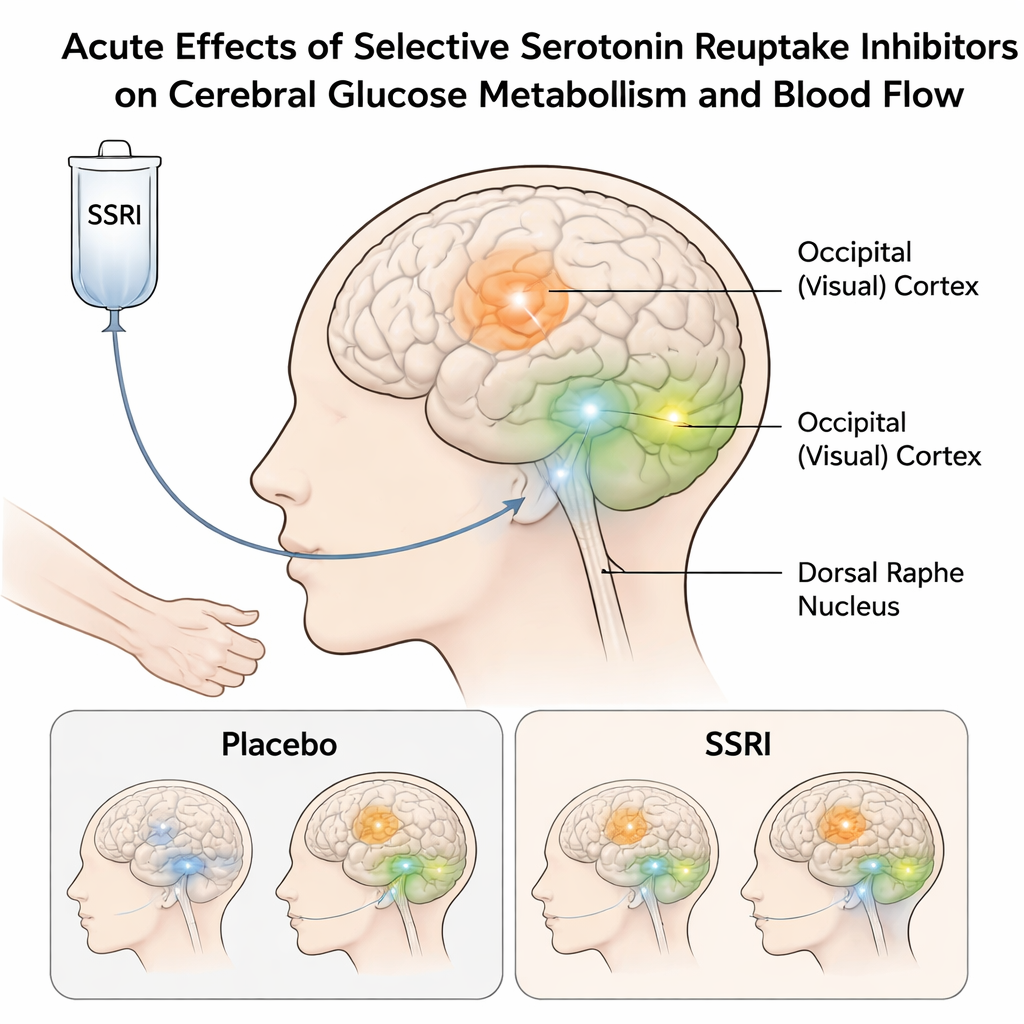
Den Treibstoffverbrauch des Gehirns in Echtzeit betrachten
Die Forschenden wollten über traditionelle MRI-Methoden hinausgehen, die Gehirnaktivität indirekt über Änderungen des Blutsauerstoffs verfolgen. Diese älteren Ansätze lieferten gemischte Ergebnisse für SSRIs, teilweise weil das Signal komplex und schwer interpretierbar ist. Stattdessen kombinierte das Team zwei Techniken in derselben Scan‑Sitzung. Die eine, funktionelle PET mit FDG, misst, wie viel Glukose (der hauptsächliche Treibstoff des Gehirns) verschiedene Areale über die Zeit verbrauchen. Die andere, arterielle Spin‑Labeling‑MRI, misst die Durchblutung des Gehirns. Sechzehn gesunde Erwachsene nahmen an einem sorgfältig kontrollierten, doppelblinden Cross‑over‑Experiment teil: An einem Tag erhielten sie eine intravenöse Infusion von Citalopram, an einem anderen Tag ein Placebo, während ihre Gehirne kontinuierlich gescannt wurden.
Wo SSRIs den Energiebedarf des Gehirns erhöhen
Durch das Verfolgen des Glukoseverbrauchs mit hoher zeitlicher Auflösung fand das Team heraus, dass eine akute Citalopram‑Gabe den Energieverbrauch in bestimmten, mit Serotonin verbundenen Regionen erhöhte. Zwei Bereiche hoben sich hervor: das Striatum, tief im Gehirn gelegen und stark an Motivation und Belohnung beteiligt, und der okzipitale Kortex im Hinterkopf, der für die primäre visuelle Verarbeitung zuständig ist. In beiden Regionen stieg der Glukosestoffwechsel unter Citalopram stärker an als unter Placebo. Eine explorative Analyse deutete außerdem auf Veränderungen im dorsalen Raphe‑Kern hin, einem winzigen Mittelhirnknoten, der Serotoninprojektionen ins ganze Gehirn sendet und als zentral für die Wirkung von SSRIs gilt. Zusammen zeigen diese Befunde, dass bereits eine einzelne niedrige intravenöse Dosis rasch den Energieverbrauch dieser Netzwerke verändern kann.
Nicht nur eine Frage der Durchblutung
Eine zentrale Frage war, ob diese metabolischen Veränderungen lediglich eine Folge veränderter Durchblutung sind. Mithilfe der arteriellen Spin‑Labeling‑Scans suchten die Autorinnen und Autoren nach übereinstimmenden Verschiebungen der zerebralen Durchblutung in denselben Regionen. Sie fanden trotz klarer Änderungen im Glukoseverbrauch keine robusten Unterschiede zwischen Citalopram und Placebo. Diese Diskrepanz legt nahe, dass die akuten Effekte von Citalopram eher mit der Arbeitsintensität lokaler neuronaler Netzwerke zusammenhängen als mit der Menge des zugeführten Bluts. Anders gesagt scheinen SSRIs in diesem Setting den Energiebedarf des Gehirns zu verändern, ohne notwendigerweise dessen „Leitungsnetz“ zu modifizieren.
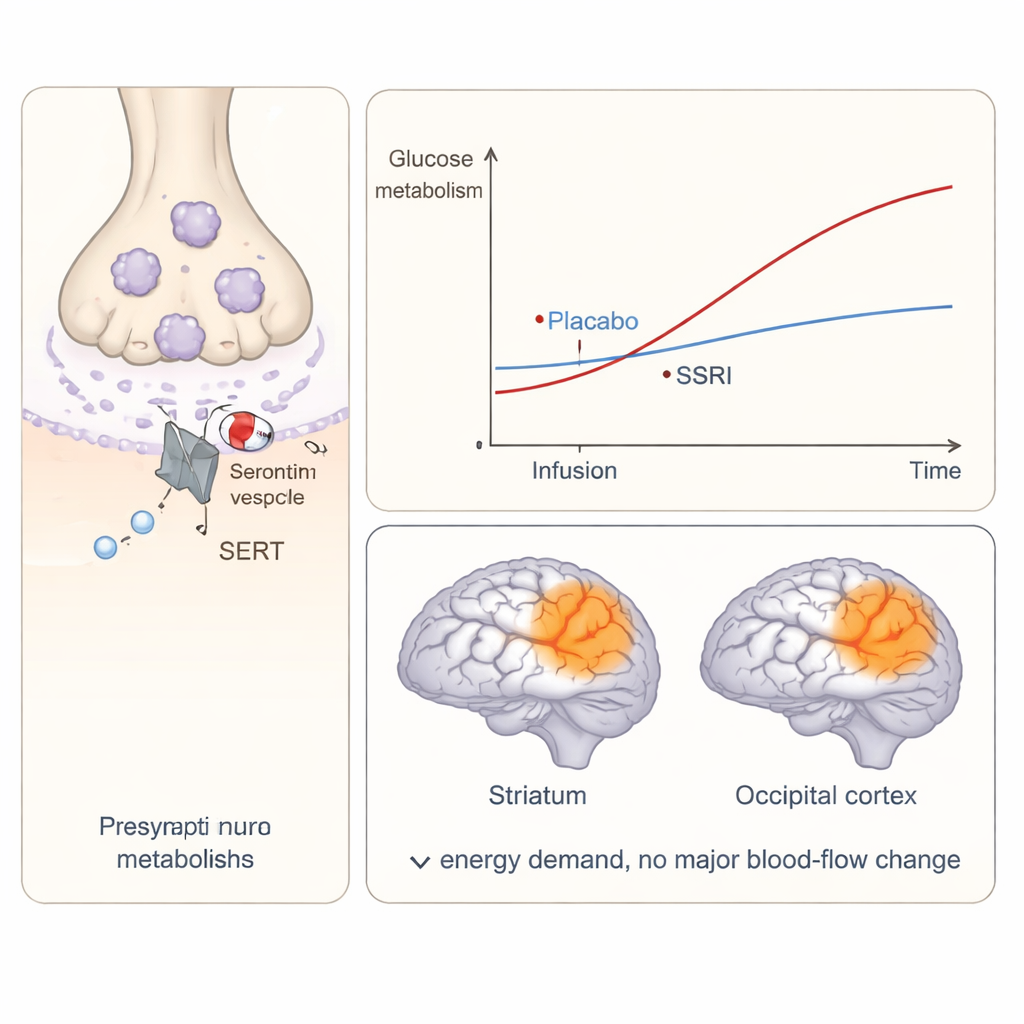
Was das für Stimmung und Wahrnehmung bedeutet
Das Muster der Veränderungen liefert interessante Hinweise darauf, wie SSRIs Symptome der Depression und emotionale Verarbeitung beeinflussen könnten. Der gesteigerte Energieverbrauch im Striatum passt zur Vorstellung, dass Serotonin eine Rolle bei Belohnung, Motivation und der Bewertung von Ereignissen spielt — alles Bereiche, die bei Depression gestört sind. Die okzipitalen Befunde deuten auf überraschend starke Effekte im visuellen System hin, das eine charakteristische Mischung aus Serotoninrezeptoren aufweist und auch von anderen serotonergen Substanzen wie Psychedelika beeinflusst wird. Die Autorinnen und Autoren schlagen vor, dass die erhöhte Aktivität im visuellen Kortex eine breitere Verschiebung in der Verarbeitung sensorischer Informationen widerspiegeln könnte, wenn die Serotoninkonzentration an Synapsen plötzlich steigt.
Großes Bild: Die Karte der Antidepressivawirkung schärfen
Für eine Leserin oder einen Leser ohne Fachwissen lautet die Kernaussage: SSRIs „heben Serotonin“ nicht nur auf vage Weise an. Innerhalb von Minuten nach einer intravenösen Dosis verändern sie den Energieverbrauch spezifischer Gehirnknoten, die an Stimmung, Belohnung und Vision beteiligt sind, ohne offensichtliche Begleitänderungen der Durchblutung zu verursachen. Indem diese Studie zeigt, dass Gehirnstoffwechsel und Blutkreislauf in diesem Kontext entkoppelt sein können, und indem sie aufzeigt, wo die Energieanforderungen zuerst ansteigen, liefert sie ein präziseres Bild davon, wie serotonerge Medikamente im lebenden menschlichen Gehirn wirken. Diese Einsicht könnte letztlich helfen, Behandlungen zu verfeinern, die Entwicklung neuer Wirkstoffe zu leiten und frühe Marker dafür zu identifizieren, wer wahrscheinlich auf eine Antidepressivatherapie anspricht.
Zitation: Silberbauer, L.R., Reed, M.B., Gryglewski, G. et al. Acute effects of selective serotonin reuptake inhibitors on cerebral glucose metabolism and blood flow. Transl Psychiatry 16, 54 (2026). https://doi.org/10.1038/s41398-026-03849-2
Schlüsselwörter: SSRIs, Gehirnstoffwechsel, Citalopram, Serotonin, PET MRI