Clear Sky Science · de
Vielfältige und ortsspezifische Rollen von PlexinA2, PlexinA4 und NCAM bei der Entwicklung hippocampaler Moosfasern
Wie Nervenbahnen Gedächtnisschaltkreise formen
Der Hippocampus, eine für Gedächtnisbildung und -abruf zentrale Gehirnregion, wird von feinen Nervenfasern verdrahtet, die sich in der frühen Entwicklung präzise zurechtfinden müssen. Diese Studie stellt eine auf den ersten Blick einfache Frage: Wie wissen diese wachsenden Fasern genau, wohin sie gehen sollen — und was geschieht, wenn ihr Leitsystem fehlgeht und so möglicherweise zu Erkrankungen wie Schizophrenie, Autismus oder Epilepsie beiträgt?
Zwei Einfahrten ins Gedächtniszentrum
Im Hippocampus senden Nervenzellen in der sogenannten Gyrus dentatus lange Fasern, die als Moosfasern bezeichnet werden, in Richtung einer anderen Region, CA3. Beim Eintritt in CA3 teilen sich diese Fasern normalerweise in zwei getrennte „Autobahnen“: eine oberhalb einer Schicht von CA3-Zellkörpern und eine unterhalb. Jede dieser Bahnen verbindet sich mit unterschiedlichen Teilen der CA3-Zellen und hilft, das Aktivitätsgleichgewicht in diesem Gedächtnisschaltkreis zu etablieren. Gelingen diese Aufteilungen nicht korrekt, können Fasern an falschen Orten landen und so den Informationsfluss im Hippocampus stören.
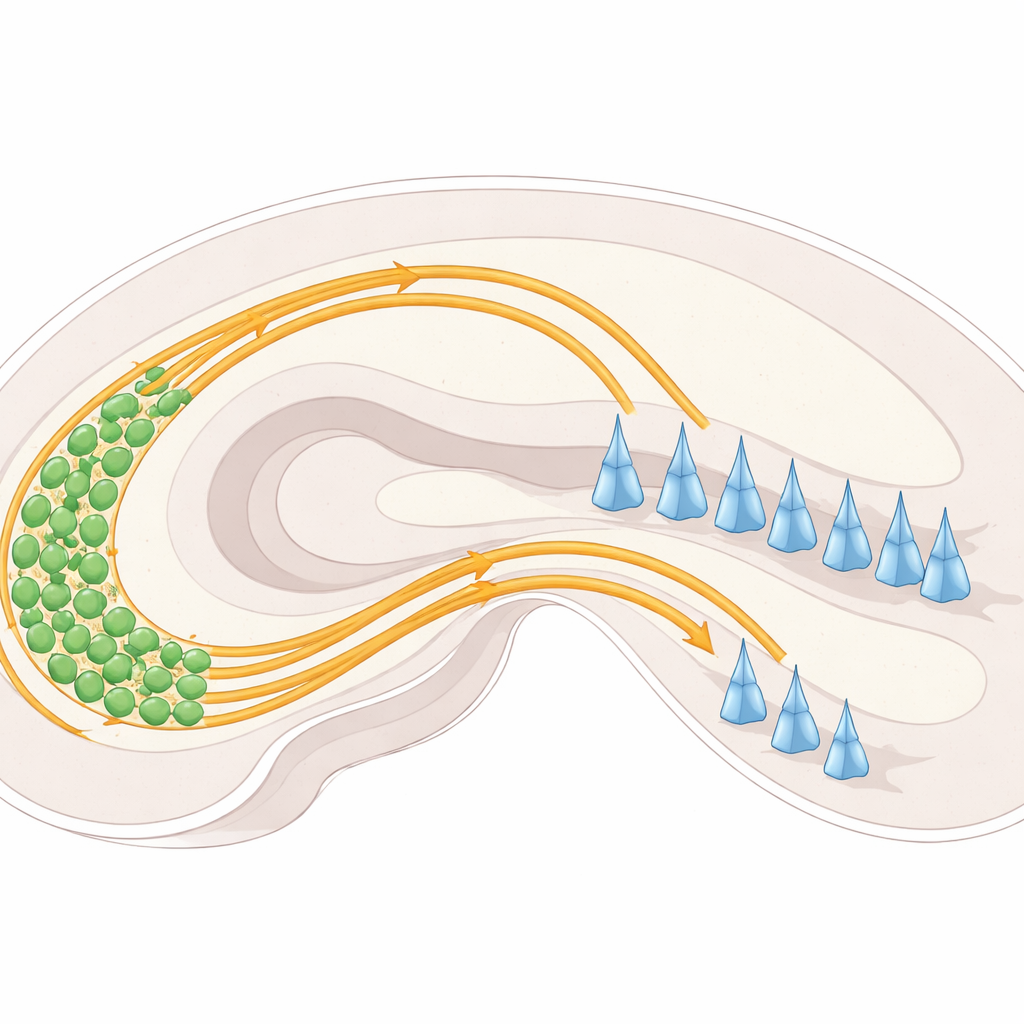
Leitsignale: Stößen, Ziehen und Zell‑zu‑Zell‑Griff
Die Untersuchenden konzentrierten sich auf eine Reihe molekularer Wegweiser und oberflächenständiger „Griffe“ an Nervenzellen, die Moosfasern steuern. Eine Proteinfamilie namens Plexine (PlexinA2 und PlexinA4) sitzt auf der Zelloberfläche und reagiert auf Partnermoleküle, die Semaphorine genannt werden, insbesondere Sema6A. Diese Interaktionen können wie „Betreten verboten“-Signale wirken, die Fasern aus bestimmten Regionen wegdrängen, oder sie können feinjustieren, wie stark benachbarte Fasern aneinanderhaften. Ein anderes Oberflächenprotein, NCAM, verhält sich eher wie Klettverschluss, fördert die Adhäsion und hilft, Faserbündel zusammenzuhalten. Indem sie untersuchten, wo diese Proteine exprimiert werden und welche Folgen ihr Entfernen oder Verändern bei Mäusen hat, kartierten die Forschenden, wie diese Faktoren im lebenden Gehirn zusammenwirken — nicht nur in isolierten Zellsystemen.
Rollen aufschlüsseln mit konstruierten Mäusen
Um die jeweilige Rolle der Komponenten zu unterscheiden, erzeugten die Wissenschaftlerinnen und Wissenschaftler 27 verschiedene Mauslinien und kombinierten sie. Einige Tiere fehlten Sema6A komplett, andere PlexinA2 oder PlexinA4, und wieder andere trugen subtile Punktmutationen, die nur einen bestimmten „enzymatischen Kern“ innerhalb der Plexine deaktivierten, während der Rest des Moleküls intakt blieb. Außerdem entfernten sie Sema6A oder NCAM selektiv aus bestimmten Zelltypen, etwa den Körnerzellen des Gyrus dentatus, um zu testen, wo das Signal wirklich relevant ist. In Mäusen, denen Sema6A in diesen Körnerzellen fehlte, teilten sich die Moosfasern nicht sauber in obere und untere Bündel und das untere Bündel wuchs zu weit und überschoss seinen normalen Endpunkt. Ähnliche, aber nicht identische Verdrahtungsfehler traten in Mäusen ohne PlexinA2 oder PlexinA4 auf, was zeigte, dass diese Proteine an unterschiedlichen Kontrollpunkten entlang desselben Pfads wirken.
Mechanismen und Partnerschaften im Detail
Als die Autorinnen und Autoren den katalytischen Kern von PlexinA4 außer Funktion setzten, traten viele — aber nicht alle — der Defekte wieder auf, die auch bei vollständigen PlexinA4‑Nullmutanten beobachtet wurden. Das zeigte, dass PlexinA4 häufig auf diesen Kern angewiesen ist, um das innere Skelett wachsender Nervenfasern umzubauen, damit sie sich korrekt bündeln und an der richtigen Schicht stoppen. PlexinA2 erwies sich als anders: Einige seiner Funktionen hingen von seinem katalytischen Kern ab, andere nicht, was auf zusätzliche, enzymunabhängige Signalwege hindeutet. Das Team nutzte anschließend eine Proximitätsmarkierungstechnik, um Nachbarproteine in der Nähe von PlexinA2 auf jungen hippocampalen Neuronen zu identifizieren. Mehrere Zelladhäsionsmoleküle traten zutage, wobei NCAM besonders hervortrat. Genetisch führte die gleichzeitige Reduktion von PlexinA2 und NCAM zu stärkeren Moosfaser‑Fehlleitungen als die Reduktion eines der beiden alleine, was zeigt, dass diese Systeme zusammenarbeiten: NCAM liefert die Adhäsion, während PlexinA2‑vermittelte Abstoßung die Aufteilung in obere und untere Bahnen und das Ausmaß des unteren Bündels kalibriert.
Wenn Signale in umgekehrter Richtung laufen
Interessanterweise wirkt Sema6A nicht nur als äußeres „Schild“, das Plexine lesen; es kann auf den Moosfasern selbst auch als Empfänger fungieren. Die Forschenden untersuchten Mäuse, bei denen der innere Schwanz von Sema6A gelöscht war, während der äußere Teil erhalten blieb. Bei diesen Tieren blieben einige Führungsfehler bestehen — besonders das Überwachsen des unteren Bündels — was darauf hinweist, dass Signale, die über den Schwanz von Sema6A nach innen fließen („Reverse Signaling“), für normales Beschneiden und Formen der Moosfasern notwendig sind. Dieser Reverse‑Modus arbeitet wahrscheinlich stadien‑ und ortsspezifisch neben der bekannteren plexinbasierten Signalgebung.
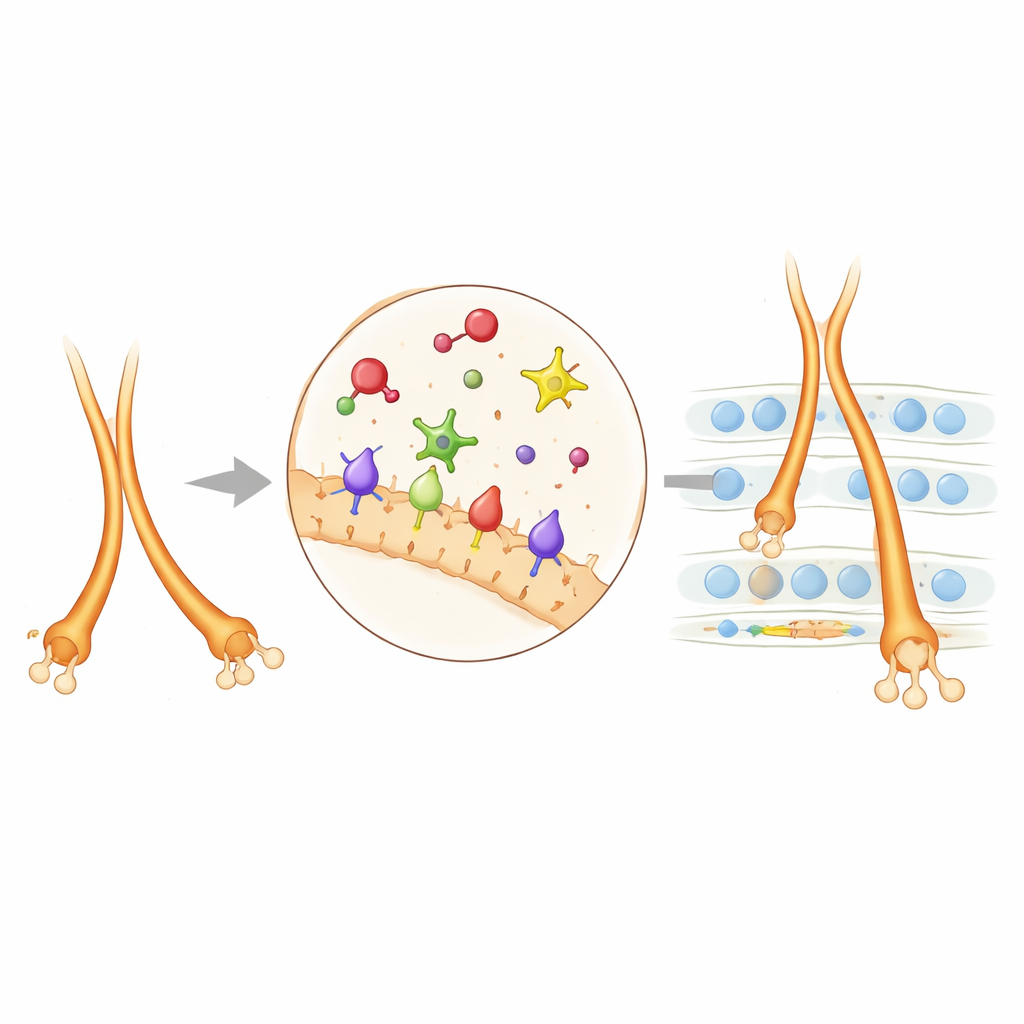
Warum diese Verdrahtung für die Gehirngesundheit wichtig ist
Mutationen in den menschlichen Genen PLXNA2, SEMA6A und NCAM1 wurden mit neuroentwicklungsbedingten und psychiatrischen Erkrankungen in Verbindung gebracht, von geistiger Behinderung bis zu Schizophrenie und Autismus. Indem die Studie zeigt, wie diese Moleküle zusammenarbeiten, um die Moosfaserbahnen bei Mäusen zu formen, liefert sie ein konkretes Modell dafür, wie subtile genetische Veränderungen die Entstehung, Trennung und das Beschneiden wichtiger Gedächtnisschaltkreise stören könnten. Alltagssprachlich deutet die Arbeit darauf hin, dass das Leitsinstrumentarium des Gehirns eine sorgfältig getimte Mischung aus ‚Stoß‘, ‚Zug‘ und ‚Klebrigkeit‘ nutzt, um das Verdrahtungsdiagramm des Hippocampus zu bauen — und dass schon kleine Störungen in diesem Werkzeugkasten weitreichende Folgen für Lernen, Gedächtnis und psychische Gesundheit haben können.
Zitation: Zhao, XF., Kohen, R., Van Battum, E.Y. et al. Diverse and location-specific roles of PlexinA2, PlexinA4, and NCAM in developing hippocampal mossy fibers. Transl Psychiatry 16, 126 (2026). https://doi.org/10.1038/s41398-026-03846-5
Schlüsselwörter: hippocampale Moosfasern, Axonführung, Semaphorin‑Plexin‑Signalgebung, NCAM und Zelladhäsion, neuroentwicklungsbedingte Störungen