Clear Sky Science · de
Auswirkungen chronischen Ethanolkonsums auf die GLP-1R-Genexpression im Gehirn bei Mäusen und Menschen
Warum diese Forschung wichtig ist
Viele Menschen wissen, dass starker Alkoholkonsum das Gehirn schädigen kann, doch wie genau dies auf molekularer Ebene geschieht, wird noch erforscht. Diese Studie beleuchtet einen überraschenden Akteur: einen Hormonrezeptor, der eher für die Steuerung von Blutzucker und Appetit bekannt ist. Anhand von Gehirnen sowohl von Mäusen als auch von Menschen mit langfristigen Alkoholproblemen zeigen die Forschenden, dass dieser Rezeptor und zwei weitere wichtige Hirnmoleküle in Bereichen, die Belohnung, Gedächtnis und Entscheidungsfindung steuern, durchgängig herunterreguliert sind. Die Arbeit könnte erklären, warum einige Diabetesmedikamente, die auf diesen Rezeptor wirken, auch den Alkoholkonsum verringern, und sie weist auf neue Ansätze zur Diagnose und Behandlung der Alkoholgebrauchsstörung hin.
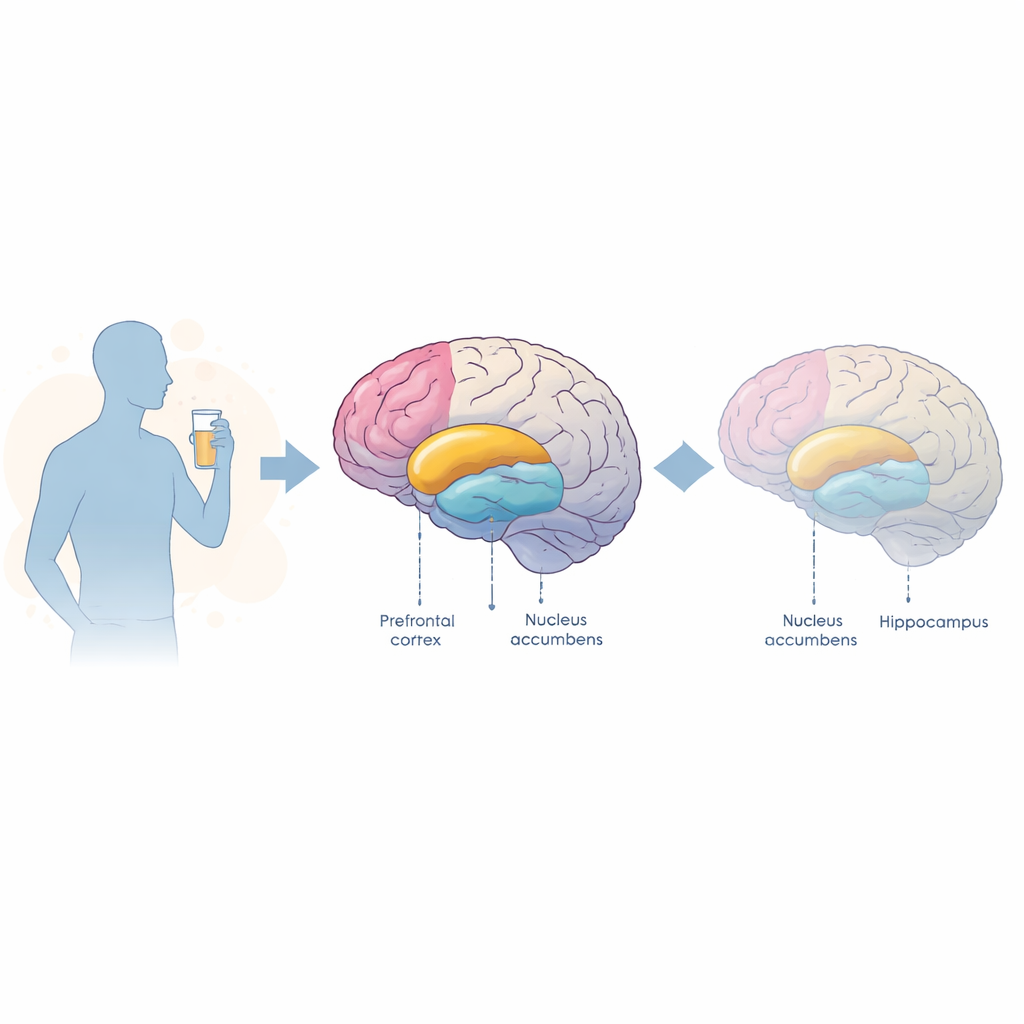
Eine hormonelle Verbindung zwischen Darm und Gehirn
Im Zentrum der Studie steht der Glucagon-like Peptid-1-Rezeptor, kurz GLP-1R, der normalerweise auf Signale aus dem Darm reagiert und Appetit, Stoffwechsel und Gehirnaktivität mitsteuert. GLP-1R ist im ganzen Gehirn verteilt, einschließlich Regionen, die Vergnügen, Motivation und Gedächtnis verarbeiten. Frühere Arbeiten an Tieren und Menschen legten nahe, dass Wirkstoffe, die diesen Rezeptor aktivieren, den Alkoholkonsum und das Verlangen reduzieren können, und dass genetische Unterschiede im GLP-1R-Gen mit starkem Trinken verbunden sind. Unklar war jedoch, ob langfristiger Alkoholkonsum selbst die Menge dieses Rezeptors im Gehirn verändert und wie solche Veränderungen mit anderen an Sucht beteiligten Molekülen zusammenhängen könnten.
Untersuchung von Gehirnen von Mäusen und Menschen
Um diese Fragen zu beantworten, verfolgte das Team einen zweigleisigen Ansatz. Zuerst erhielten männliche Mäuse sechs Wochen lang freiwillig Alkohol in einem Zwei-Flaschen-Setup, bei dem die Tiere zwischen Wasser und einer schrittweise stärkeren Alkohollösung wählen konnten. Nach dieser langen Exposition sezierten die Wissenschaftler drei Hirnregionen sorgfältig: den präfrontalen Kortex, der bei Planung und Selbstkontrolle hilft; den Nucleus accumbens, ein zentrales Belohnungszentrum; und den Hippocampus, der für Lernen und Gedächtnis entscheidend ist. Sie maßen, wie viel GLP-1R-Genaktivität in jedem Bereich verblieb, zusammen mit zwei weiteren wichtigen Markern: dem Gen für den Mu-Opioid-Rezeptor, das die angenehmen und motivierenden Effekte von Alkohol mitprägt, und dem Gen für das brain-derived neurotrophic factor (BDNF), ein wachstumsförderndes Protein, das für gesunde Schaltkreise und Kognition wichtig ist.
Konsequente molekulare Veränderungen über Arten hinweg
Der zweite Teil der Studie untersuchte postmortale Hirnproben von 18 Männern mit Alkoholgebrauchsstörung und 18 vergleichbaren Männern ohne diese Störung. Dieselben drei Hirnregionen wurden analysiert. Sorgfältige Qualitätsprüfungen stellten sicher, dass die RNA in diesen Geweben noch intakt genug für verlässliche Messungen war. Sowohl bei Mäusen als auch bei Menschen zeigte sich ein auffallend ähnliches Muster: Die GLP-1R-Genexpression war in allen drei Regionen bei denjenigen mit langfristiger Alkoholexposition signifikant niedriger. Zusätzlich war das Mu-Opioid-Rezeptor-Gen im Nucleus accumbens vermindert und BDNF im Hippocampus reduziert, ebenfalls in beiden Spezies. Diese Veränderungen korrelierten nicht wesentlich mit Alter, Körpergewicht, Rauchen, Gehirn-pH oder der Dauer des Trinkens, was darauf hindeutet, dass es sich um robuste Merkmale starken Alkoholkonsums handelt und nicht um Nebenwirkungen anderer Faktoren.
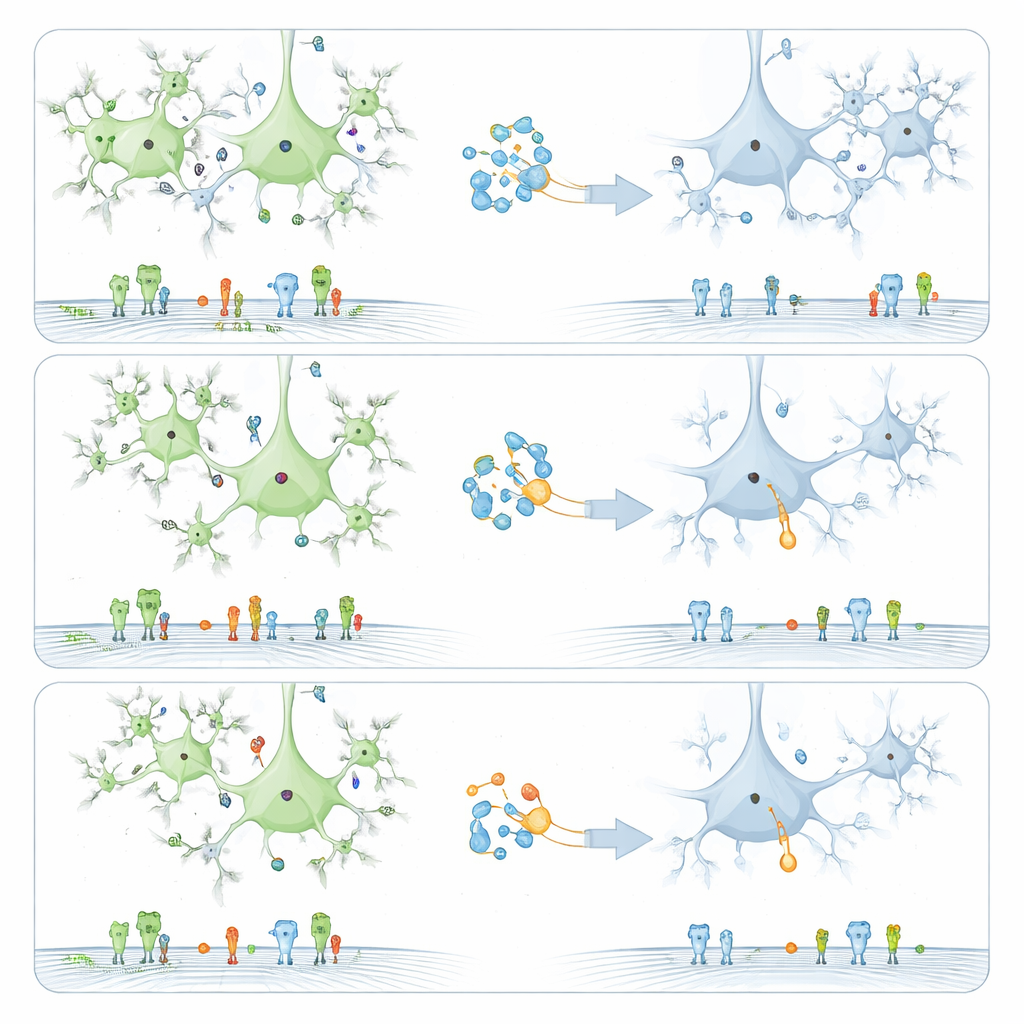
Was diese Veränderungen für das Gehirn bedeuten könnten
Der koordinierte Rückgang von GLP-1R, Mu-Opioid-Rezeptor und BDNF deutet auf eine weitreichende Schwächung von Systemen hin, die normalerweise Belohnungssignale regulieren und gesunde Gehirnstruktur und -funktion unterstützen. In den Belohnungszentren könnten weniger GLP-1- und Mu-Opioid-Rezeptoren die Fähigkeit des Gehirns dämpfen, die angenehmen und aversiven Effekte von Alkohol richtig auszugleichen, was möglicherweise zwanghaftes Verhalten begünstigt. Im Hippocampus und im präfrontalen Kortex könnten reduzierte GLP-1R- und BDNF-Spiegel zu den kognitiven Problemen und der schlechten Entscheidungsfindung beitragen, die häufig bei Menschen mit Alkoholabhängigkeit beobachtet werden. Die Autorinnen und Autoren fanden außerdem Hinweise darauf, dass bei Personen ohne Alkoholprobleme GLP-1R-Spiegel in einigen Regionen mit BDNF-Spiegeln in anderen Regionen verknüpft sind und dass diese Beziehungen bei Alkoholgebrauchsstörung gestört sind, was auf eine beeinträchtigte Kommunikation zwischen Hirnarealen hinweist.
Blick auf neue Werkzeuge und Behandlungen
Insgesamt zeigt die Studie, dass chronischer Alkoholkonsum bei Mäusen und Menschen mit einem konsistenten Rückgang von GLP-1R einhergeht, zusammen mit wichtigen belohnungs- und wachstumsbezogenen Molekülen in Hirnregionen, die das Verlangen nach Alkohol und die daraus resultierenden Denkstörungen vermitteln. Für eine allgemeine Leserschaft lautet die Kernaussage: Starkes Trinken „verschleißt" das Gehirn nicht einfach allgemein; es hinterlässt einen spezifischen molekularen Fingerabdruck, der nachweisbar und wichtig ist, weil er möglicherweise reversibel ist. Da GLP-1R bereits ein Arzneimittelziel bei Diabetes und Fettleibigkeit ist, untermauern diese Befunde die Idee, dass solche Medikamente zur Behandlung der Alkoholgebrauchsstörung umfunktioniert oder verfeinert werden könnten und dass GLP-1R selbst letztlich als Biomarker dienen könnte, um Risiko zu identifizieren, den Krankheitsverlauf zu verfolgen oder die Therapieantwort zu überwachen.
Zitation: Torregrosa, A.B., García-Gutiérrez, M.S., Ortuño-Miquel, S. et al. Effects of chronic ethanol consumption on brain GLP-1R gene expression in mice and humans. Transl Psychiatry 16, 123 (2026). https://doi.org/10.1038/s41398-026-03838-5
Schlüsselwörter: Alkoholgebrauchsstörung, GLP-1-Rezeptor, Belohnungssystem des Gehirns, Hippocampus und Gedächtnis, Mu-Opioid und BDNF