Clear Sky Science · de
Frühe funktionelle Veränderungen und Plasma-GFAP in schwedischen Familien mit autosomal-dominanten Alzheimer‑Mutationen
Warum diese Studie für Familien relevant ist
Alzheimer scheint oft plötzlich aufzutreten, in Wirklichkeit aber entwickeln sich schädliche Veränderungen im Gehirn über viele Jahre unbemerkt. In seltenen Familien mit vererbten („autosomal-dominanten“) Alzheimer‑Mutationen können Forschende abschätzen, wann Symptome voraussichtlich beginnen, und diese frühen Veränderungen beobachten. Diese Studie begleitete schwedische Familien mit solchen Mutationen, um zu verstehen, wie sich die Gehirnenergieverwertung, kognitive Fähigkeiten und ein Blutmarker für Gehirnstützzellen (GFAP) lange vor dem Auftreten von Gedächtnisproblemen verändern – und wie sich diese Veränderungen zwischen den Genen unterscheiden.
Der Krankheitsuhr in Hochrisikofamilien folgen
Da Menschen mit autosomal-dominanter Alzheimer‑Krankheit (ADAD) typischerweise in einem recht vorhersehbaren Alter Symptome entwickeln, können Forschende die „geschätzten Jahre bis zum Symptombeginn“ (EYO) berechnen — wie viele Jahre jemand vor oder nach dem erwarteten Auftreten erster Krankheitszeichen steht. Das Team untersuchte 45 Erwachsene aus schwedischen Familien mit APP- oder PSEN1‑Genmutationen sowie Verwandte ohne Mutation. Über im Mittel mehr als sieben Jahre unterzogen sich die Teilnehmenden Hirnscans, die den Glukoseverbrauch des Gehirns messen (FDG‑PET), ausführlichen Gedächtnis‑ und Denktests und bei einer Untergruppe Blutuntersuchungen für GFAP, ein Protein, das freigesetzt wird, wenn astrozytäre Stützzellen reaktiv werden. Dieses Design ermöglichte es den Forschern, verschiedene biologische Veränderungen entlang einer gemeinsamen Krankheitszeitachse anzuordnen, statt nur Personen zu einem einzigen Zeitpunkt zu vergleichen.
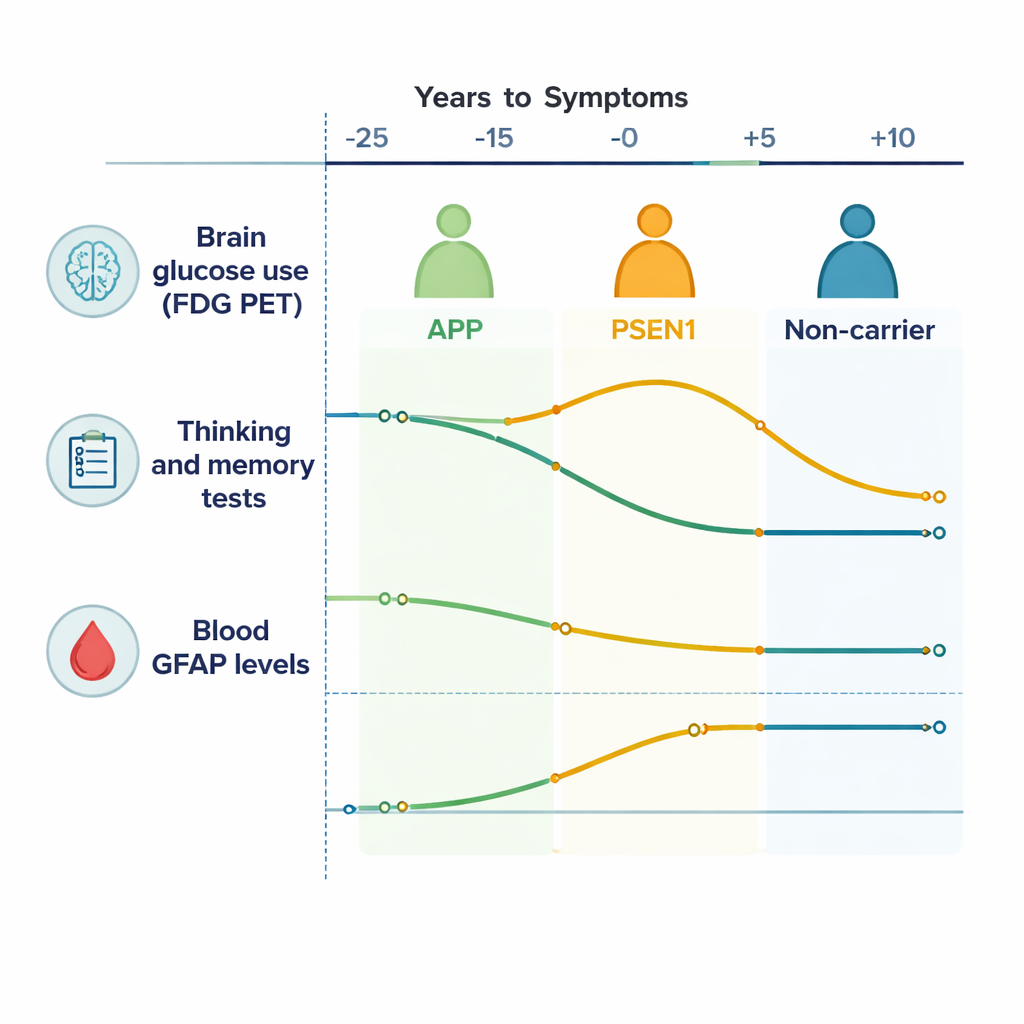
Verfolgung von Gehirnenergie und Kognition über die Zeit
In der Großhirnrinde zeigten Menschen mit Alzheimer‑Mutationen im Vergleich zu nicht‑mutierten Familienmitgliedern einen allmählichen Rückgang des FDG‑PET‑Signals, was bedeutet, dass ihr Gehirn im Laufe der Zeit weniger Zucker verbrauchte — ein Zeichen für nachlassende Gehirnzellenfunktion. Subkortikale Regionen tief im Gehirn, insbesondere Caudatus und Thalamus, zeigten ebenfalls abnehmende Aktivität, vor allem bei Personen mit APP‑Mutationen. Denk‑ und Gedächtnistests verschlechterten sich in mehreren Bereichen, darunter episodisches Gedächtnis und geistige Flexibilität, beginnend etwa 10–15 Jahre vor dem erwarteten Symptombeginn. Anders gesagt: Auch wenn sich Betroffene im Alltag noch normal fühlten und funktionierten, zeigten empfindliche Tests und Scans, dass ihre Gehirne bereits weniger effizient arbeiteten.
Unterschiedliche Muster bei verschiedenen Alzheimer‑Genen
Eine wichtige Erkenntnis war, dass die beiden Hauptmutationsgruppen — APP und PSEN1 — nicht identische Verläufe zeigten. Bei PSEN1‑Trägern beobachteten die Forschenden eine frühe Phase, etwa 20 bis 10 Jahre vor dem erwarteten Symptombeginn, in der Teile des Gehirns ungewöhnlich hohen Glukoseverbrauch aufwiesen („Hypermetabolismus“), begleitet von besseren Testergebnissen, bevor später ein Abfall folgte. Dies deutet auf eine vorübergehende Kompensationsphase hin, in der das Gehirn und seine Stützzellen die Aktivität erhöhen, um mit zunehmenden Schäden fertigzuwerden. APP‑Träger zeigten demgegenüber einen eher geradlinigen, allmählichen Abfall des Gehirnmetabolismus ohne diesen frühen Anstieg. Diese gen‑spezifischen Muster legen nahe, dass „Alzheimer‑Krankheit“ nicht eine einzige biologische Geschichte ist, selbst in vererbten Formen, sondern eine Familie verwandter Prozesse, die je nach zugrunde liegender Mutation unterschiedlich ablaufen.
Was ein Bluttest über frühen Hirnstress verrät
GFAP, gemessen aus einer einfachen Blutprobe, bot Einblicke darin, wie Astrozyten auf frühe Alzheimer‑Veränderungen reagieren. GFAP‑Spiegel stiegen tendenziell stetig an, je näher Menschen ihrem erwarteten Symptombeginn kamen — bei Mutationsträgern wie auch bei Nicht‑Trägern —, aber die Zusammenhänge zwischen GFAP, Gehirnstoffwechsel und Kognition waren genabhängig. Bei APP‑Trägern war höheres GFAP mit sinkendem Glukoseverbrauch in tiefen Hirnregionen und mit schlechteren Ergebnissen in den meisten kognitiven Tests verknüpft, was darauf hindeutet, dass Astrozytenaktivierung eng mit frühem Schaden und Funktionsverlust verbunden ist. Bei PSEN1‑Trägern waren diese Zusammenhänge schwächer oder fehlten, was erneut auf unterschiedliche biologische Wege bis zum gleichen klinischen Endpunkt der Demenz hinweist.
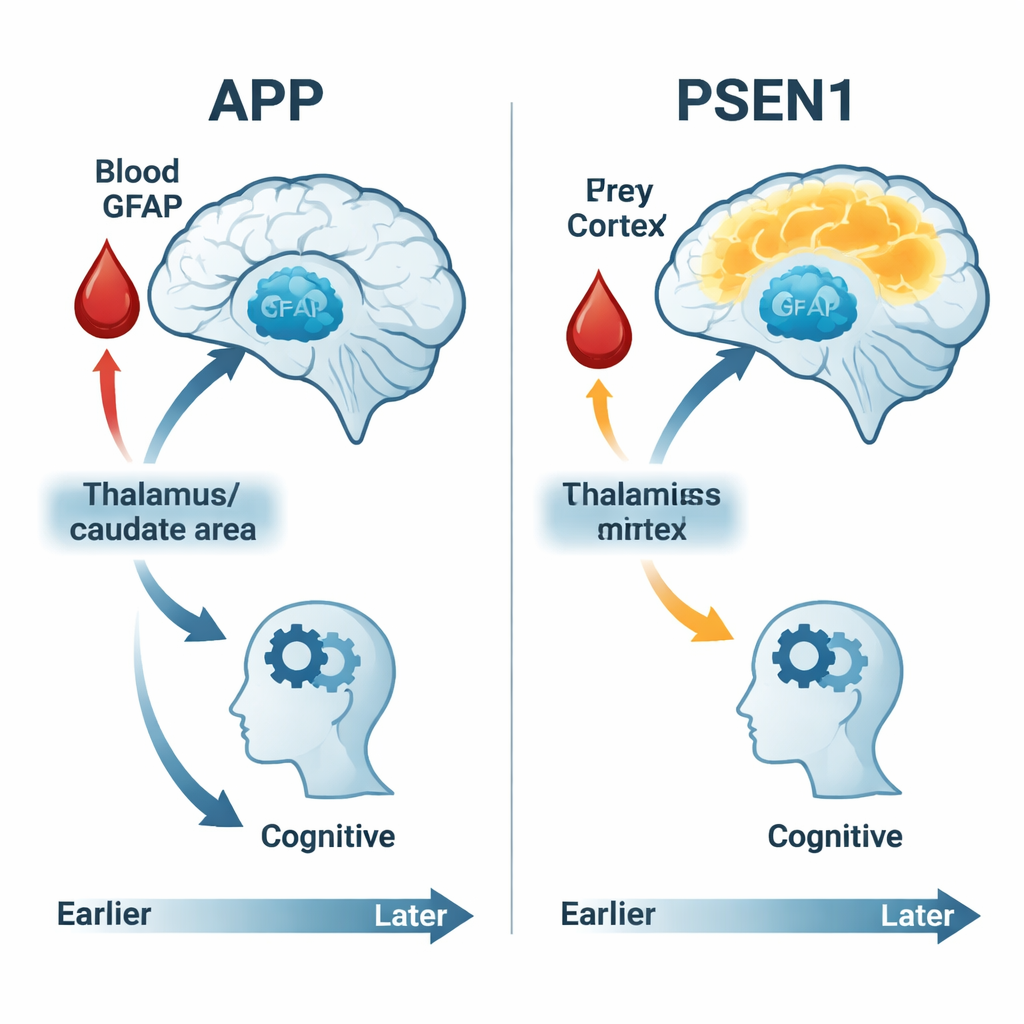
Implikationen für Früherkennung und Therapie
Für eine allgemein verständliche Leserschaft lautet die Hauptbotschaft: In diesen Hochrisikofamilien beginnen Alzheimer‑assoziierte Veränderungen Jahrzehnte vor offensichtlichem Gedächtnisverlust — und sie sehen nicht bei allen gleich aus. Hirnscans des Glukoseverbrauchs, feingranulare kognitive Tests und ein einzelner Blutmarker wie GFAP können zusammen zeigen, wann das Gehirn zu kämpfen beginnt und wie schnell dieser Prozess voranschreitet. Wichtig ist, dass Menschen mit unterschiedlichen genetischen Formen des Alzheimer unterschiedliche Abfolge von Veränderungen zeigen: Manche haben eine frühe überaktive Phase, andere einen stetigen Abfall, und der Blutmarker für Astrozytenstress ist in manchen Gruppen stärker mit Schäden verbunden als in anderen. Das Erkennen dieser unterschiedlichen Pfade kann helfen, zukünftige Medikamente und Studien besser auf die richtigen Personen zum richtigen Zeitpunkt zuzuschneiden, und unterstreicht das Potenzial von Bluttests wie GFAP, Alzheimer früher zu erkennen — bevor Symptome den Menschen ihre Selbstständigkeit rauben.
Zitation: Luckett, E.S., Zapater-Fajari, M., Almkvist, O. et al. Early functional changes and plasma GFAP in Swedish families with Autosomal Dominant Alzheimer’s disease mutations. Transl Psychiatry 16, 67 (2026). https://doi.org/10.1038/s41398-026-03829-6
Schlüsselwörter: autosomal-dominante Alzheimer‑Krankheit, GFAP Blut-Biomarker, Gehirn-Glukosestoffwechsel, Astrozyten und Neurodegeneration, früher Alzheimer‑Nachweis