Clear Sky Science · de
Konvergenz und Divergenz von Genen, informiert durch häufige und seltene Varianten bei Autismus-Spektrum-Störungen in gewebespezifischen Signalwegen und Gen-Netzwerken
Warum das genetische Puzzle des Autismus wichtig ist
Familien und Kliniker wissen seit langem, dass die Autismus-Spektrum-Störung (ASD) sehr unterschiedlich ausgeprägt ist: Manche Menschen benötigen lebenslange Unterstützung, während andere unabhängig leben, aber soziale Herausforderungen haben. Viel von dieser Vielfalt wird der Genetik zugeschrieben, doch das Risiko verteilt sich über Tausende von DNA-Veränderungen, die jeweils Gehirn und Körper in subtiler Weise beeinflussen. Diese Studie stellt eine einfache, aber wichtige Frage: Wie wirken seltene, starke Mutationen und die vielen häufigen, schwächeren DNA-Varianten in verschiedenen Geweben zusammen, um Autismus zu prägen — und was bedeutet das für das Verständnis und die Behandlung der Erkrankung?
Zwei Arten genetischer Hinweise
Forscher unterscheiden zwischen seltenen Varianten, die ein Gen stark stören können, aber bei relativ wenigen Menschen vorkommen, und häufigen Varianten, die in der Population verbreitet sind, meist jedoch nur geringe Effekte haben. Seltene Varianten waren in einzelnen Familien leichter mit Autismus zu verknüpfen, erklären aber nur einen kleinen Teil des gesamten genetischen Risikos. Häufige Varianten tragen zusammengenommen viel mehr zur erblichen Komponente von Autismus bei, doch die Wirkung jeder einzelnen ist winzig und leicht zu übersehen. Die Autorinnen und Autoren dieses Papiers wollten beide Signale integrieren und untersuchen, ob sie auf dieselben biologischen Systeme zulaufen oder auf unterschiedliche Körperregionen und verschiedene Krankheitsmechanismen hinweisen.
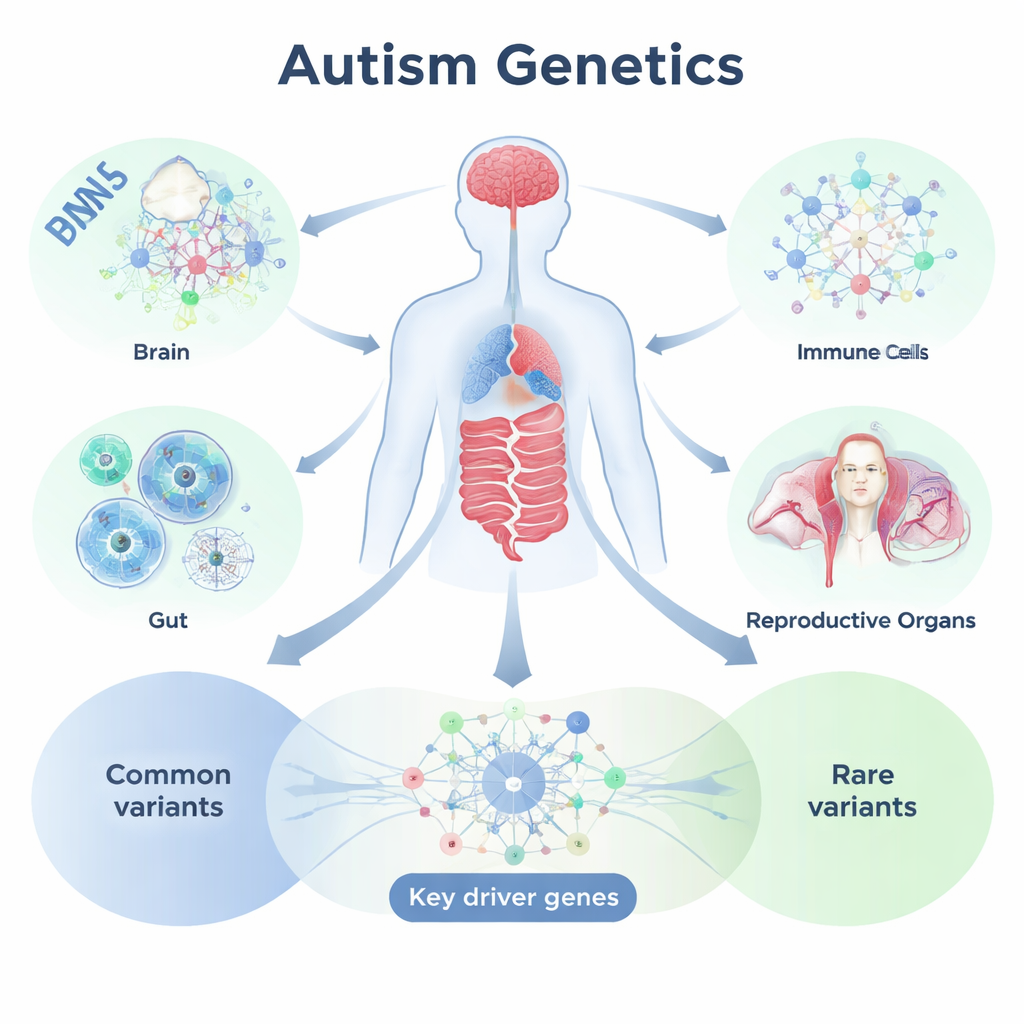
DNA-Signale auf Gewebe und Netzwerke abbilden
Um das zu untersuchen, nutzte das Team einen Analyse-Rahmen namens Mergeomics, der groß angelegte genetische Studien mit Informationen darüber kombiniert, wie Gene in spezifischen Geweben ein- und ausgeschaltet werden. Ausgangspunkt waren genomweite Assoziationsdaten zu mehr als neun Millionen häufiger DNA-Varianten von über 18.000 autistischen Personen und etwa 28.000 nicht-autistischen Kontrollen. Anschließend wurden diese Varianten auf Gene abgebildet, mithilfe detaillierter Referenzdaten zur Genaktivität in nahezu 50 Geweben, darunter viele Gehirnregionen sowie Verdauungs-, Immun-, Fortpflanzungs- und andere periphere Organe. Indem Gene zusammengefasst wurden, die im selben Gewebe gemeinsam exprimiert sind, und untersucht wurde, wie stark diese Gen-Gruppen mit autismus-assoziierten Varianten übereinstimmen, identifizierten die Forschenden gewebespezifische „Module“ und regulatorische Netzwerke, die für ASD bedeutsam zu sein scheinen.
Sowohl Gehirn als auch Körper tragen bei
Die Analyse bestätigte die zentrale Rolle des Gehirns — insbesondere Regionen wie den anterioren cingulären Kortex, die Amygdala, den frontalen Kortex, das Kleinhirn und weiterführende kortikale Bereiche, die an Emotion, sozialem Verhalten, Denken und Koordination beteiligt sind. Gen-Netzwerke in diesen Gehirnregionen waren reich an sowohl häufigen als auch seltenen autismusbezogenen Varianten und standen in Verbindung mit synaptischer Signalübertragung, Neuroentwicklung und immunologischer Kontrolle im Gehirn. Doch das Bild endete nicht am Schädel. Überraschenderweise enthielten viele periphere Gewebe, besonders des Verdauungs-, Immun-, endokrinen und reproduktiven Systems, ebenfalls Gen-Module, die stark durch autismus-assoziierte häufige Varianten informiert waren. Diese Module waren mit Prozessen assoziiert wie Immunantworten, Zellwachstum und -teilung, Energieproduktion, mRNA-Spleißen und einem wichtigen Steuerweg namens mTOR, die alle mit Gehirnentwicklung und Verhalten in Verbindung gebracht wurden.
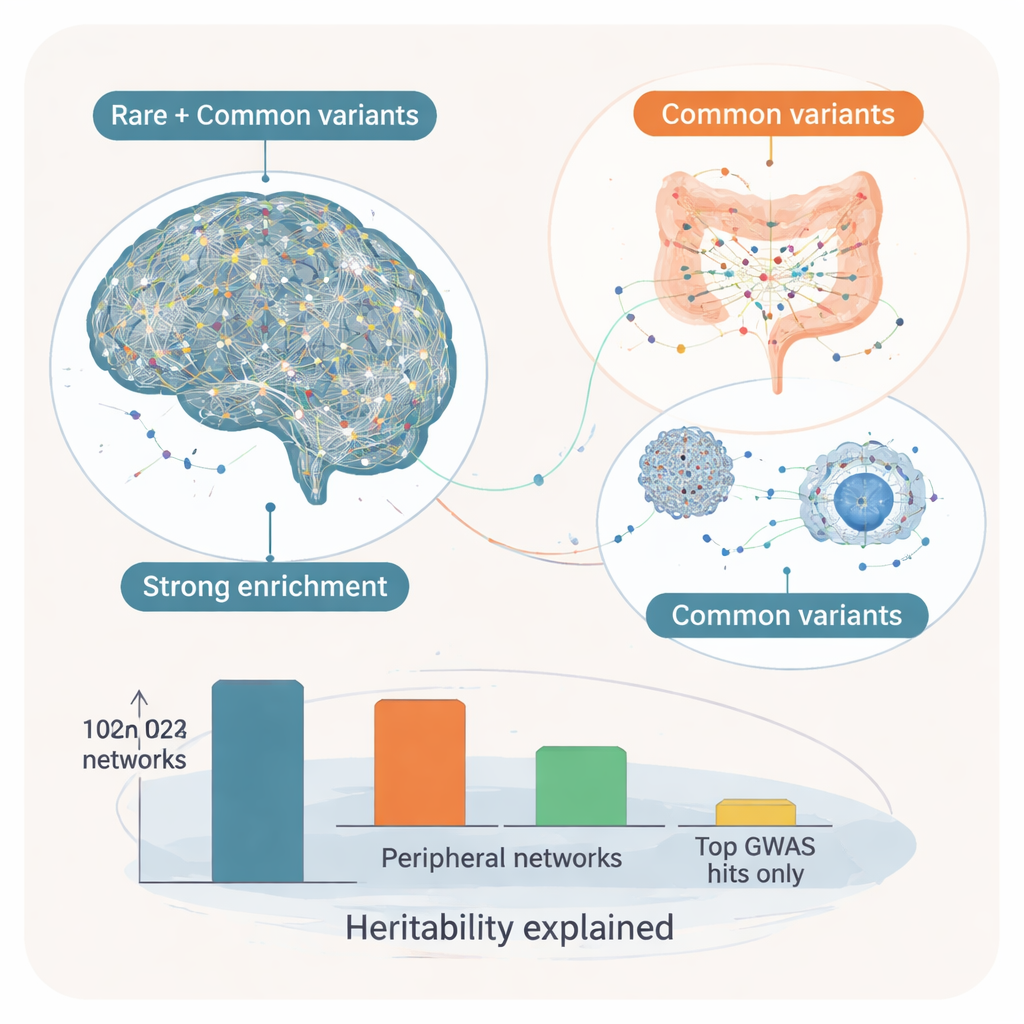
Schlüsselkontrollgene und die Kern–Modifikator-Idee
Indem die Forschenden diese Module in gerichtete genregulatorische Netzwerke einordneten, fragten sie als Nächstes, welche Gene an den Knotenpunkten sitzen — sogenannte „Key Drivers“, die viele andere Gene beeinflussen. In Gehirnnetzwerken zeigten diese Schlüsseltreiber eine starke Anreicherung seltener, hochwirksamer Autismus-Varianten ebenso wie häufiger Varianten, was darauf hindeutet, dass sie ein „Kern“-Set von Genen bilden, an dem beide Risikoarten zusammenlaufen. Beispiele sind SYT1, das die Neurotransmitterausschüttung an Synapsen mitsteuert, und ADD2, beteiligt an der Formgebung neuronaler Struktur und Konnektivität. Die umliegenden Netzwerke enthielten eine Mischung aus bekannten seltenen Autismusgenen und Zielgenen häufiger Varianten, die an synaptischer Kommunikation und neuronaler Erregbarkeit beteiligt sind. Im Gegensatz dazu wurden Schlüsseltreiber in peripheren Geweben, besonders im Verdauungs- und endokrinen Bereich, stärker allein von häufigen Varianten beeinflusst. Diese scheinen als „Modifikatoren“ zu wirken, die Immun-, Stoffwechsel- und Signalwege feinabstimmen und dadurch beeinflussen können, wie sich zentrale Gehirnverletzlichkeiten in Symptomen äußern.
Was das für Menschen und künftige Therapien bedeutet
Als die Autorinnen und Autoren schätzten, wie viel des erblichen Autismus-Risikos auf diese Netzwerke zurückgeführt werden kann, erklärten gehirnbasierte Module etwa 7 % der erblichen Komponente und periphere Module weitere 3 %; zusammen erfassen sie nahezu die gesamte häufige-Variant-Heritabilität, die in der ursprünglichen Studie beobachtet wurde — und weit mehr als der winzige Bruchteil, der nur durch die stärksten einzelnen DNA-Signale erklärt wird. Für Nicht-Spezialisten lautet die Schlussfolgerung, dass die Genetik des Autismus einem geschichteten Muster folgt: Seltene und häufige Varianten konvergieren auf ein Kern-Set von gehirnzentrierten Netzwerken, die für die Neuroentwicklung entscheidend sind, während weit verbreitete häufige Varianten in Darm-, Immun- und hormonellen Geweben wahrscheinlich den Verlauf und die Merkmale der Erkrankung modifizieren. Dieses Kern–Modifikator-Modell hilft zu erklären, warum Autismus von Person zu Person so unterschiedlich aussieht, und legt nahe, dass künftige Therapien nicht nur das Gehirn, sondern auch die breiteren Körpersysteme berücksichtigen sollten, die mit ihm interagieren.
Zitation: Gill, C., Zuo, Y., Ha, D.Sm. et al. Convergence and divergence of genes informed by common and rare variants of autism spectrum disorders in tissue-specific pathways and gene networks. Transl Psychiatry 16, 98 (2026). https://doi.org/10.1038/s41398-026-03824-x
Schlüsselwörter: Genetik von Autismus, seltene Varianten, häufige Varianten, Gehirnnetzwerke, Darm–Gehirn-Achse