Clear Sky Science · de
Histamin-H3-Rezeptor als Ziel für die Behandlung von Alkoholgebrauchsstörung: Die Vorhersagbarkeit von Tiermodellen für die klinische Übersetzung in der Arzneimittelentwicklung in Frage stellen
Warum diese Forschung für den Alltag wichtig ist
Alkoholgebrauchsstörung betrifft weltweit Millionen von Menschen, doch die derzeit verfügbaren Medikamente helfen nur einem Bruchteil der Betroffenen. Dieser Artikel verfolgt die gesamte Reise eines vielversprechenden neuen Arzneimittelkandidaten, BP1.3656B, von der Laborbank bis zu Studien am Menschen. Er zeigt, wie eine Idee, die bei Tieren hervorragend funktioniert, beim Menschen scheitern kann — und warum diese Lücke für alle wichtig ist, die auf bessere Behandlungen für problematischen Alkoholkonsum hoffen.
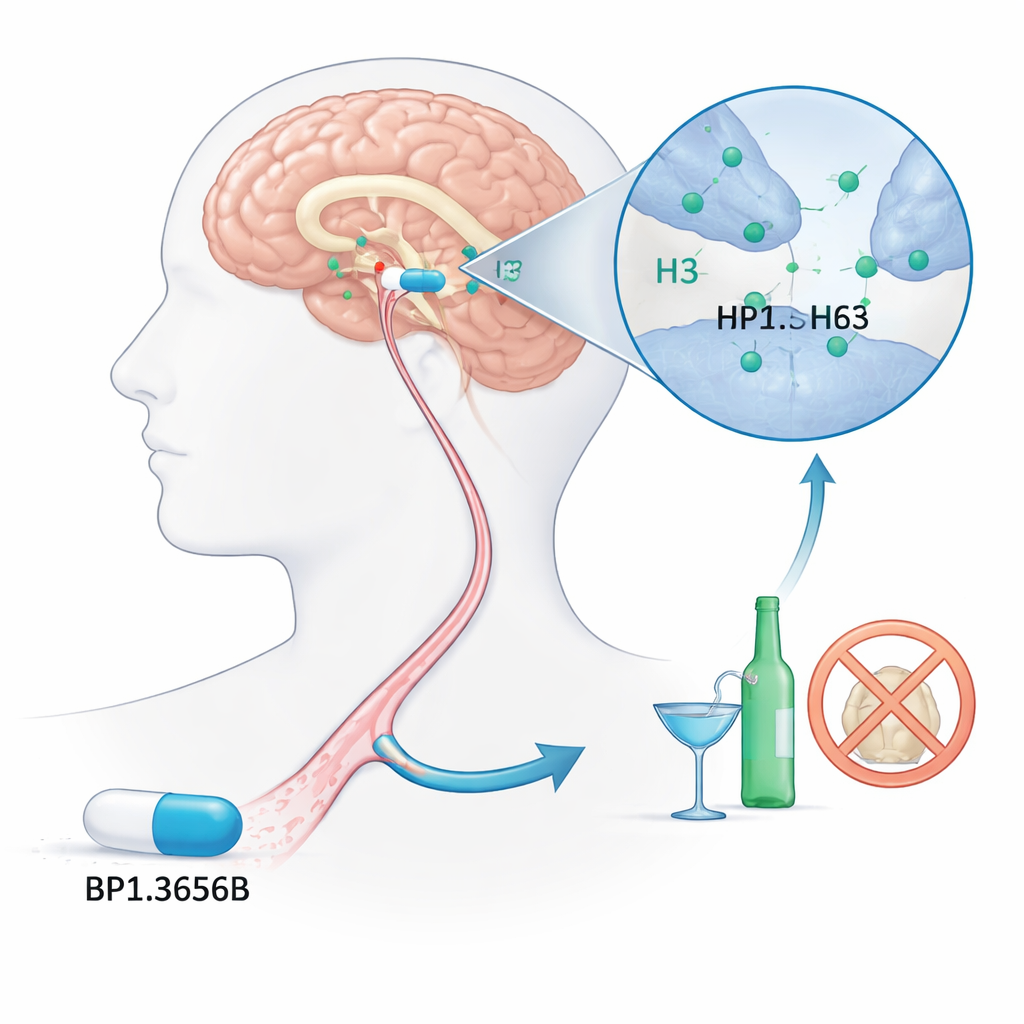
Ein neues Ziel im Gehirn für problematischen Alkoholkonsum
Die Forschenden konzentrierten sich auf einen weniger bekannten Schalter im Gehirn, den Histamin-H3-Rezeptor. Histamin ist vor allem für seine Rolle bei Allergien bekannt, im Gehirn jedoch reguliert es Wachheit und die Kommunikation zwischen Nervenzellen. Der H3-Rezeptor wirkt wie ein Dimmer, der die Freisetzung von Histamin und mehreren anderen Botenstoffen beeinflusst, die an Belohnung und Motivation beteiligt sind. Da Alkohol stark mit diesen Gehirnsystemen interagiert, vermuteten Wissenschaftler schon lange, dass die Blockade von H3-Rezeptoren das Verlangen zu trinken verringern könnte. BP1.3656B wurde als potenter H3-Blocker entwickelt, in der Hoffnung, den Sog von Alkohol auf die Belohnungsschaltkreise des Gehirns abzuschwächen.
Von der Chemie zu Erfolgsgeschichten in Tiermodellen
In frühen Tests zeigte BP1.3656B das Profil, von dem Arzneimittelentwickler träumen. Es band sehr stark und selektiv an den H3-Rezeptor, gelangte gut ins Gehirn und erschien in Standarduntersuchungen sicher. Bei Mäusen verringerte das Mittel den Aktivitätsschub, der typischerweise nach einer Alkoholgabe auftritt, und halbierte bis mäßig reduzierte binge‑ähnliches Trinken in einem „Drinking in the Dark“-Test. Bei Ratten, die das Drücken eines Hebels zum Erhalt von Alkohol erlernt hatten, senkte BP1.3656B deutlich die Trinkmenge und die Bereitschaft, für Alkohol zu arbeiten — sowohl bei einfach stark trinkenden Tieren als auch bei solchen mit körperlicher Abhängigkeit. Es dämpfte zudem rückfallähnliches Trinken und linderte angstbezogene Symptome im Zusammenhang mit Alkoholentzug. Zusammengenommen deuteten diese Ergebnisse darauf hin, dass das Mittel die Motivaton für Alkohol senken und helfen könnte, einen Rückfall in starken Konsum zu verhindern.
Frühe Tests am Menschen: Erreicht das Medikament sein Ziel?
Es folgten Phase‑I‑Studien an gesunden Freiwilligen. Einmalige und wiederholte Dosen bis zu 90 Mikrogramm wurden insgesamt gut vertragen, mit überwiegend milden schlafbezogenen Nebenwirkungen, die zu den wachheitsfördernden Eigenschaften von H3‑Blockern passen. Blutmessungen zeigten ein klares, vorhersagbares Muster von Aufnahme und Elimination des Wirkstoffs. Um sicherzugehen, dass er sein beabsichtigtes Ziel im lebenden menschlichen Gehirn trifft, nutzte das Team die Positronen-Emissions-Tomografie, eine Hirnbildgebung, die zeigen kann, wie viele Rezeptoren von einem Medikament besetzt werden. Schon relativ niedrige Dosen von BP1.3656B blockierten die Mehrheit der H3‑Rezeptoren in mehreren für Motivation und Belohnung wichtigen Hirnregionen und bestätigten damit, dass das Medikament biologisch das tat, wofür es entwickelt worden war.
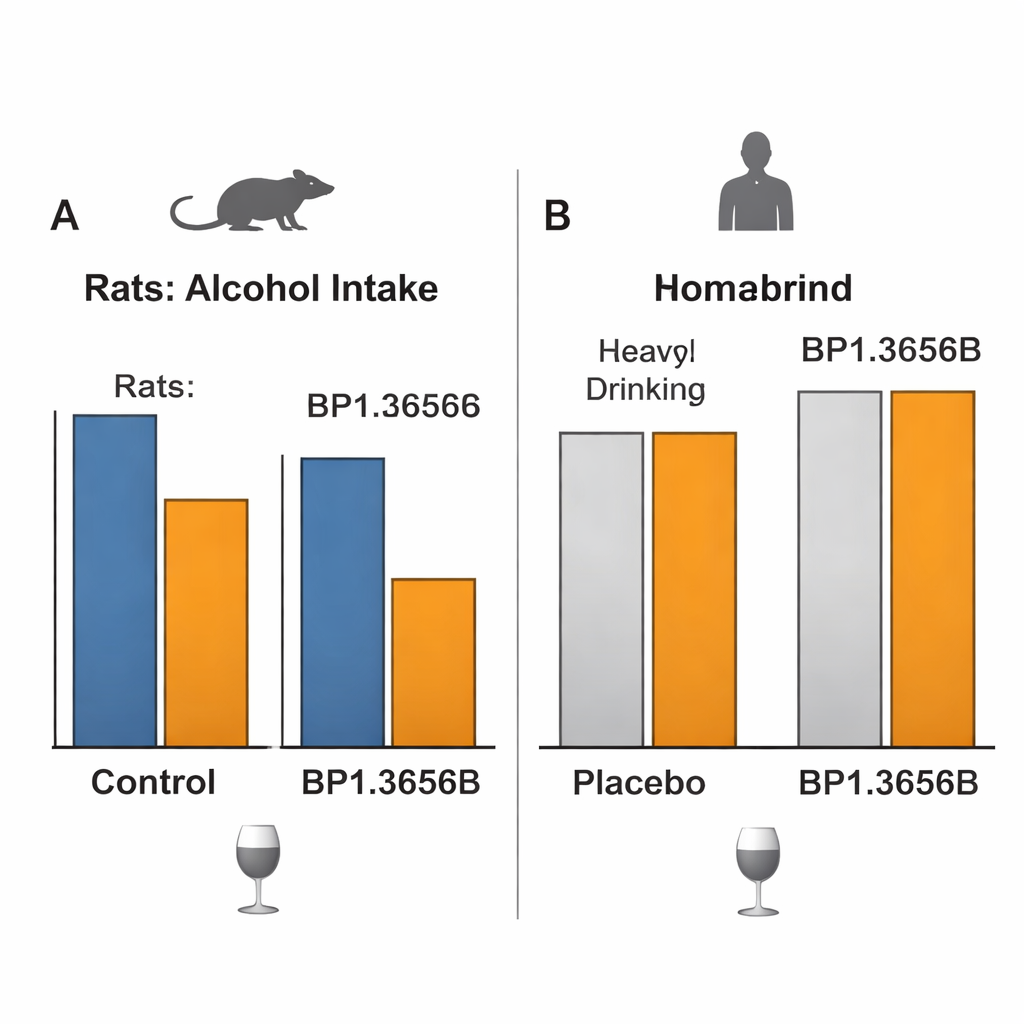
Wenn vielversprechende Tierergebnisse nicht auf den Menschen übertragbar sind
Die entscheidende Frage war, ob sich all das in bedeutsame Veränderungen des Trinkverhaltens bei Menschen mit Alkoholgebrauchsstörung übersetzt. In einer kontrollierten Laborsituation erhielten nicht‑behandlungssuchende Erwachsene mit Alkoholproblemen BP1.3656B oder Placebo und absolvierten dann Sitzungen, in denen sie durch das Drücken eines Knopfs intravenös Alkohol selbst verabreichen konnten — unter Bedingungen, die sowohl Genuss als auch Motivation messen sollten. Das Medikament hatte keinen erkennbaren Effekt darauf, wie viel Alkohol sie auswählten. In einer größeren, 12‑wöchigen multizentrischen Studie an behandlungssuchenden Patientinnen und Patienten wurden dann drei Tagesdosen von BP1.3656B gegen Placebo getestet. Alle Gruppen, einschließlich Placebo, reduzierten im Zeitverlauf deutlich die Anzahl starker Trinktage und die Gesamtalkoholaufnahme, doch das Medikament zeigte gegenüber Placebo bei keiner wichtigen Messgröße zu Trinkverhalten oder Verlangen einen Vorteil, trotz guter Sicherheit und klarer Zielbindung.
Was das für zukünftige Behandlungen bedeutet
Für eine lesende Öffentlichkeit ist die Quintessenz nüchtern, aber wichtig: Ein Wirkstoff, der in Zellen, Mäusen und Ratten exzellent wirkte — und nachweislich sein Ziel im menschlichen Gehirn erreichte — half den Menschen dennoch nicht, weniger zu trinken. Das bedeutet nicht, dass die Wissenschaft falsch war, wohl aber, wie unsicher es ist, menschliche Ergebnisse allein aus Tiermodellen vorherzusagen. Die Autorinnen und Autoren plädieren dafür, kleinere, frühe Studien am Menschen, die direkt die Auswirkung eines Medikaments auf Alkoholkonsum messen, routinemäßig einzusetzen, um die Entwicklung vor großen, teuren Studien besser zu „entrisiken“. Anders gesagt: Wir brauchen nicht nur neue Arzneimittelideen, sondern bessere Wege, um zu entscheiden, welche dieser Ideen tatsächlich eine Chance haben, Menschen mit Alkoholgebrauchsstörung zu helfen.
Zitation: Le Foll, B., Naassila, M., Jeanblanc, J. et al. Histamine H3 Receptor as a target for alcohol use disorder: challenging the predictability of animal models for clinical translation in drug development. Transl Psychiatry 16, 55 (2026). https://doi.org/10.1038/s41398-026-03807-y
Schlüsselwörter: Alkoholgebrauchsstörung, Histamin-H3-Rezeptor, BP1.3656B, Suchterkrankungsbehandlung, translationale Forschung