Clear Sky Science · de
Unterdrückung der mitochondrialen Energieproduktion durch ein photosynthetisches bakterielles Cupredoxin-Peptid hemmt das Tumorwachstum
Bakterien zu Krebsbekämpfern machen
Krebszellen sind energiehungrig. Sie verlassen sich auf winzige innere „Kraftwerke“, die Mitochondrien, um die Energie zu erzeugen, die sie zum Wachsen, Ausbreiten und zur Resistenz gegen Behandlungen benötigen. Diese Studie untersucht einen unerwarteten Verbündeten im Kampf gegen Krebs: ein kurzes Fragment eines Proteins, das ursprünglich in photosynthetischen Bakterien vorkommt. Die Forscher zeigen, dass dieses designte Peptid in Krebszellen eindringen, deren Energieversorgung an der Quelle lahmlegen und die Strahlentherapie deutlich wirksamer machen kann – während normale Zellen weitgehend geschont werden.
Ein winziges Peptid mit großer Aufgabe
Das Team begann mit einer früheren Entdeckung, dass ein bakterielles Protein namens Azurin das Tumorwachstum verlangsamen kann, indem es auf den bekannten Tumorsuppressor p53 wirkt. Anschließend suchten sie in Bakterien, die in und um menschliche Tumore leben, wobei sie sich auf photosynthetische Mikroben konzentrierten, die Licht zur Energiegewinnung nutzen. Diese Bakterien tragen eine verwandte Proteinfamilie, die Cupredoxine genannt wird. Durch den Vergleich ihrer Strukturen und ihrer Evolutionsgeschichte konzentrierten sich die Forscher auf ein Cupredoxin, Auracyanin B, und schnitten einen kurzen, 28 Aminosäuren langen Abschnitt heraus, den sie aurB nannten. Dieses Fragment ist wasserlöslich, kann Zellmembranen passieren und hat eine Form, die darauf hindeutete, dass es mit Schlüsselkomponenten der Energieproduktion innerhalb der Zellen interagieren könnte.
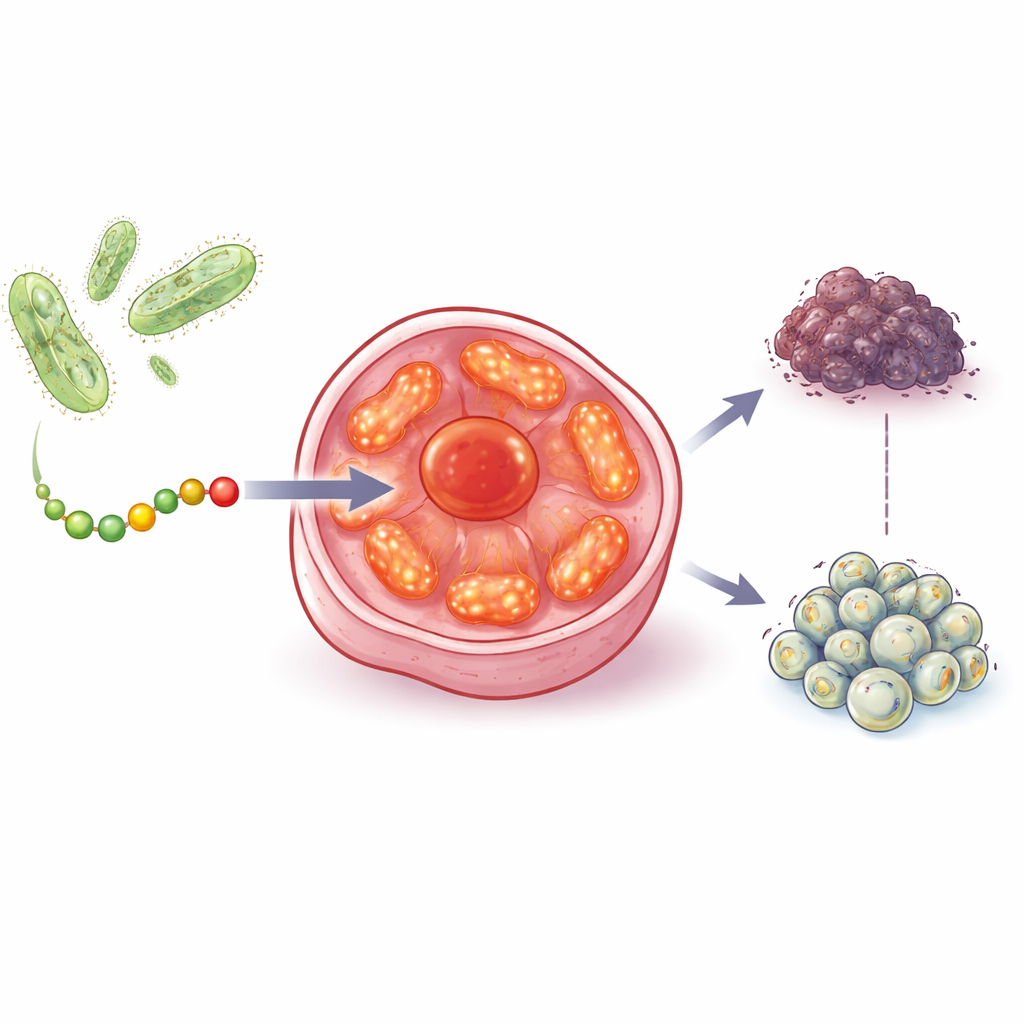
Die Kraftwerke des Krebses finden und treffen
In Labortests reduzierte aurB das Überleben von Brust-, Prostata-, Darm- und Eierstockkrebszelllinien, selbst wenn diese Zellen kein funktionierendes p53 oder keine Hormonrezeptoren aufwiesen, die viele aktuelle Medikamente benötigen. Wichtig ist, dass aurB deutlich schwächere Effekte auf normale Prostata-, Herz- und Muskelzellen hatte, obwohl diese gesunden Zellen reich an Mitochondrien sind. Bildgebende Experimente zeigten, dass aurB bevorzugt in Krebszellen gelangte und sich dann in deren Mitochondrien anreicherte. Elektronenmikroskopie, bei der aurB an winzige Goldstäbchen als visuellen Marker gekoppelt wurde, bestätigte, dass das Peptid tatsächlich innerhalb dieser Organellen akkumulierte.
Die Energiezufuhr kappen
Einmal in den Mitochondrien angekommen, band aurB an eine spezifische Komponente der ATP-Synthase – der molekularen Turbine, die ATP, die Hauptenergieeinheit der Zelle, herstellt. Biochemische Pull-down-Experimente und Massenspektrometrie identifizierten diesen Partner als ATP5C, einen Teil des zentralen Kerns des Enzyms. Messungen mittels Oberflächenplasmonenresonanz zeigten, dass aurB mit moderater Stärke und langsamer Dissoziation an ATP5C bindet, was auf eine stabile Interaktion hindeutet. Funktionelle Tests enthüllten anschließend die Folgen dieser Bindung: aurB reduzierte die mitochondrialen ATP-Spiegel in Prostatakrebszellen deutlich, verlangsamte deren Sauerstoffverbrauchsrate und blockierte sowohl die Atmung als auch den Backup-Weg der Glykolyse. Als die Energieproduktion zusammenbrach, zeigten die Krebszellen typische Kennzeichen des programmierten Zelltods, vermittelt durch Caspase-3, ein zentrales Exekutorenenzym.
Tumore blockieren und Strahlung verstärken
Die Forscher testeten aurB anschließend in Mausmodellen aggressiven Prostatakrebses. Bei Tieren mit menschlichen Prostatatumoren unter der Haut führten regelmäßige Injektionen von aurB zu einer etwa zwei Dritteligen Verkleinerung des Tumorwachstums, vergleichbar mit oder besser als das Chemotherapeutikum Paclitaxel, jedoch ohne offensichtlichen Gewichtsverlust oder Hinweis auf Leid. Tumorproben aus behandelten Mäusen enthielten weniger teilende Zellen und deutlich mehr sterbende Zellen. In einem zweiten Modell, das Knochenmetastasen nachahmt – ein häufiger und tödlicher Ort für die Ausbreitung von Prostatakrebs – verlangsamte aurB alleine das Tumorwachstum im Bein und verringerte die Anzahl der Lungenmetastasen. In Kombination mit einer moderaten Strahlendosis war der Effekt jedoch dramatisch: Tumore im behandelten Bein waren nahezu ausgelöscht, und die Lungenmetastasen reduzierten sich im Vergleich zu Kontrollen um mehr als 90 Prozent.
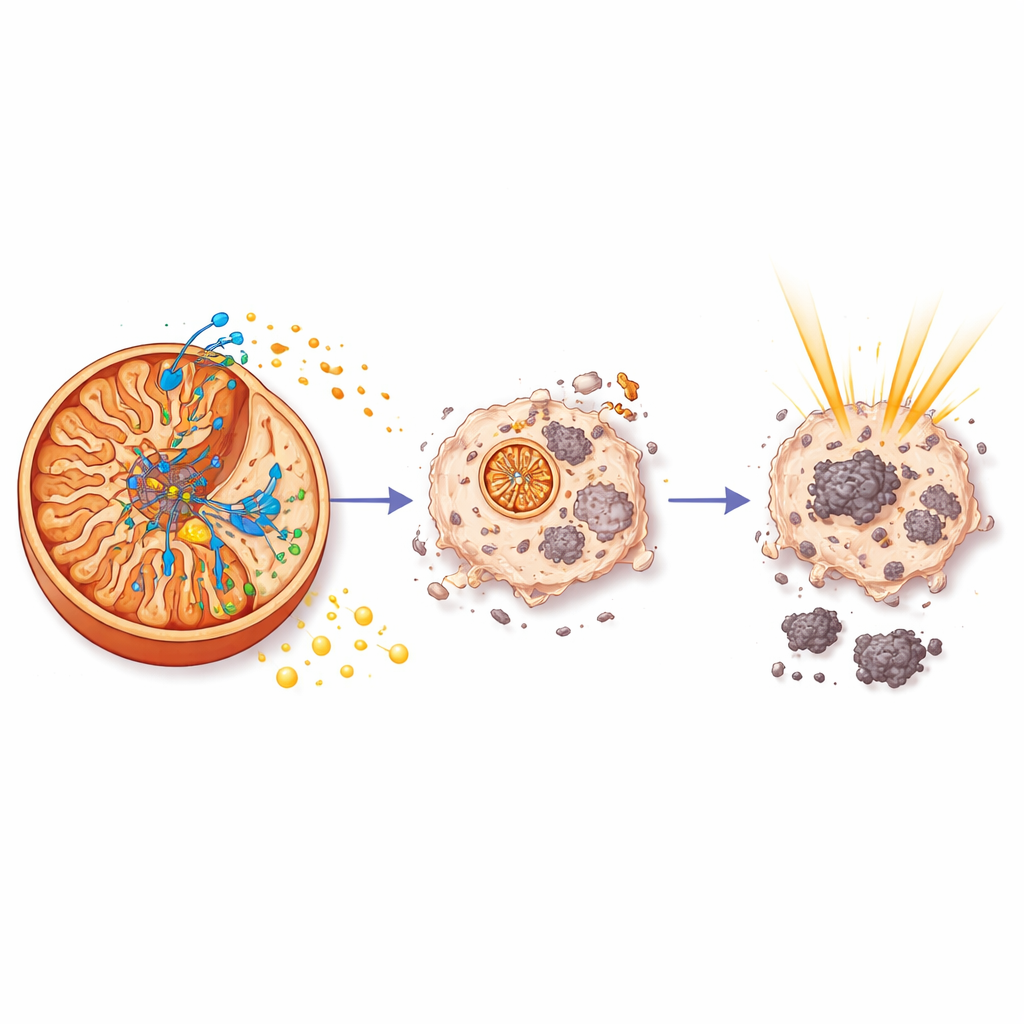
Warum Energie für Strahlung wichtig ist
Um zu verstehen, warum aurB die Strahlentherapie wirksamer macht, untersuchte das Team die Genaktivität in Tumoren behandelter Mäuse. Sie fanden, dass aurB, im Gegensatz zur Strahlung allein, ein Netzwerk von Genen dämpfte, das von HIF-1 kontrolliert wird – einem Masterregulator, der Krebszellen hilft, sich an niedrige Sauerstoffbedingungen anzupassen und die Resistenz gegen Therapien fördert. Unter den energiearmen Bedingungen, die aurB erzeugte, wurden zentrale Wachstums- und Überlebenswege, die von PI3K und c-Myc gesteuert werden, heruntergefahren, und die glykolytischen Mechanismen, die Tumoren das Überleben in rauen Umgebungen ermöglichen, wurden ebenfalls unterdrückt. Im Kern schob aurB die Krebszellen durch die Sabotage der ATP-Produktion direkt an der mitochondrialen Turbine in eine Energiekrise, die sie deutlich verletzlicher für Strahlenschäden machte.
Eine neue Klasse präziser Energieblocker
Diese Arbeit stellt eine neue Strategie für die Krebstherapie vor: die Entwicklung kleiner, von Bakterien inspirierter Peptide, die gezielt mitochondriale Energiesysteme ansteuern, die in Tumoren verändert sind. AurB, abgeleitet von einem photosynthetischen bakteriellen Protein, zielt selektiv auf eine Komponente der ATP-Synthase, die in Krebsarten wie Prostata-, Brust-, Eierstock- und Hirntumoren oft überaktiv ist. Indem es Krebszellen direkt der Energie beraubt und ihre Abwehrkräfte, insbesondere gegen Strahlung, schwächt, könnten solche Peptide bestehende Behandlungen ergänzen und Optionen bieten, wo immunbasierte Ansätze versagen. Obwohl noch viel Arbeit nötig ist, bevor dieses Konzept klinische Anwendung findet, zeigt die Studie, dass uralte bakterielle Energieproteine in moderne, hochspezifische Antikrebswerkzeuge umgewidmet werden können.
Zitation: Naffouje, S.A., Tran, D.B., Rademacher, D.J. et al. Suppression of mitochondrial energy production by a photosynthetic bacterial cupredoxin peptide inhibits tumor growth. Sig Transduct Target Ther 11, 124 (2026). https://doi.org/10.1038/s41392-026-02703-7
Schlüsselwörter: mitochondriale ATP-Synthase, Krebsstoffwechsel, therapeutische Peptide, Prostatakrebs, Strahlungssensibilisierung