Clear Sky Science · de
Spi-1-Protoonkogen reguliert mRNA-Hypertranskription und maligne Progression bei Kopf‑und‑Hals‑Krebs
Warum diese Krebsstudie wichtig ist
Kopf‑und‑Hals‑Tumoren sind häufig und oft tödlich, zum Teil weil viele Tumoren selbst nach aggressiver Behandlung weiterwachsen, streuen und wiederkehren. Diese Studie stellt eine scheinbar einfache Frage mit weitreichenden Folgen: Was passiert, wenn Krebszellen die Lautstärke ihrer gesamten Genaktivität gleichzeitig aufdrehen und ungewöhnlich große Mengen an messenger‑RNA (mRNA) produzieren, die Moleküle, die die Proteinproduktion steuern? Indem die Autoren einen einzelnen Kontrollschalter identifizieren, der diesen überaktiven Zustand befeuert, decken sie eine potenzielle Schwachstelle in einigen der gefährlichsten Kopf‑und‑Hals‑Tumoren auf.
Zellen, die im Schnellvorlauf leben
Jede Zelle braucht mRNA, um Proteine zu bauen, aber Krebszellen verhalten sich oft wie Fabriken im Überdrehen. Die Forschenden konzentrierten sich auf die „mRNA‑Hypertranskription“, einen Zustand, in dem Zellen global die Produktion protein‑kodierender Botschaften steigern, statt nur einige wenige krebsrelevante Gene. Mit Einzelzellsequenzierung an mehr als 100.000 Zellen von 12 Patientinnen und Patienten zählten sie mRNA‑Moleküle Zelle für Zelle. Tumorzellen mit der höchsten Gesamt‑mRNA‑Produktion waren weniger ausgereift, identitätsmäßig flexibler und stark mit aktiven Signalwegen ausgestattet, die Wachstum, Stressresistenz und Migration unterstützen. Bei Ausweitung der Analyse auf eine große öffentliche Krebsdatenbank hatten Patientinnen und Patienten, deren Tumoren diesen Hochleistungszustand zeigten, deutlich schlechteres Überleben — selbst nach Berücksichtigung von Faktoren wie Tumorstadium und Infektion mit humanem Papillomavirus. 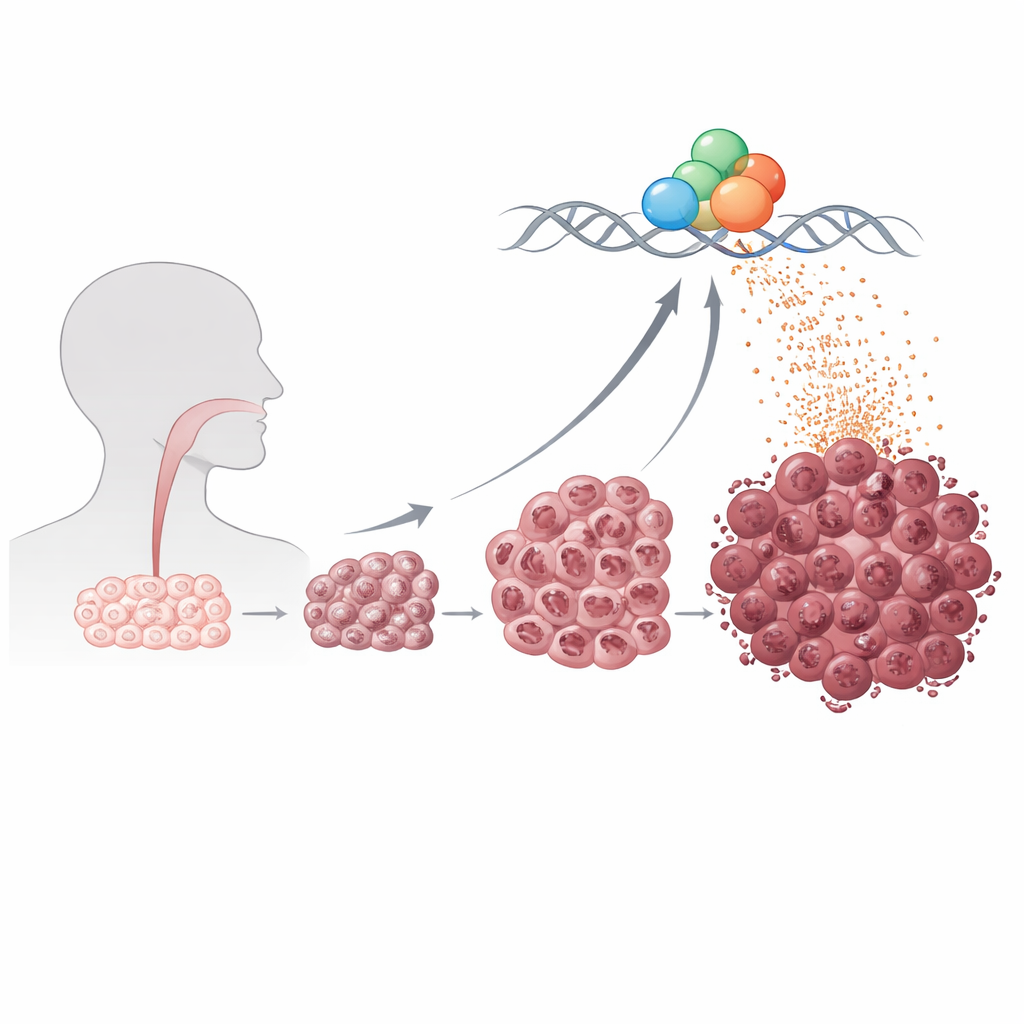
Ein Hauptschalter namens SPI1
Um zu verstehen, was diese hyperaktive Nachrichtenproduktion antreibt, suchte das Team nach Transkriptionsfaktoren — Proteinen, die an DNA binden und steuern, welche Gene ein‑ oder ausgeschaltet werden —, die in Hochleistungs‑Tumorzellen besonders aktiv waren. Einer stach heraus: SPI1, auch bekannt als PU.1, bisher vor allem mit Blutkrebserkrankungen in Verbindung gebracht. In Kopf‑und‑Hals‑Tumoren stieg die SPI1‑Aktivität im Gleichschritt mit den Gesamt‑mRNA‑Spiegeln, sowohl in Patientenproben als auch in Tumorzelllinien. Tumoren mit höherer SPI1‑Aktivität waren reich an krebsfördernden Signalwegen und mit schlechteren Patientenverläufen verknüpft. Innerhalb einzelner Tumoren waren es dieselben Zellen mit starken SPI1‑Signalen, die die intensivste mRNA‑Produktion zeigten, was auf eine direkte Verbindung zwischen diesem Faktor und dem überdrehten Zustand hindeutet.
SPI1 im Labor hoch- und runterregeln
Die Autoren fragten dann, ob SPI1 nur ein Begleiter aggressiver Erkrankung ist oder sie tatsächlich mitverursacht. In kultivierten Kopf‑und‑Hals‑Krebszellen, die natürlicherweise viel SPI1 produzieren, verwendeten sie genetische Werkzeuge, um das Protein zu drosseln. Diese Zellen wuchsen langsamer, bildeten weniger Kolonien, migrierten und invasierten weniger und zeigten stärkere Anzeichen programmierter Zellsterblichkeit. Wurden diese geschwächten Zellen in Mäuse implantiert, entstanden kleinere Tumoren, die langsamer wuchsen und weniger teilende, aber mehr sterbende Zellen enthielten. Das umgekehrte Experiment bestätigte die Beobachtungen: Das Hochregulieren von SPI1 in Zellen mit niedriger Expression beschleunigte Wachstum und Invasion in Kultur und führte in Tieren zu größeren, schneller wachsenden Tumoren.
Wie SPI1 die Genproduktion auf Touren bringt
Um den Einfluss von SPI1 auf die Genaktivität selbst zu messen, verfolgte das Team neu hergestellte RNA mit einem chemischen Marker und quantifizierte direkt die gereinigte mRNA pro Zelle. Die Reduktion von SPI1 verringerte sowohl die Synthese neuer RNA als auch die Gesamt‑mRNA, während das Erzwingen höherer SPI1‑Level sie erhöhte. Mit Systemen, die SPI1 rasch an‑ und ausschalten konnten, zeigten sie, dass die mRNA‑Produktion innerhalb von Stunden anstieg, was eine zeitabhängige Verstärkung offenbart. Genomweite Bindungsexperimente zeigten ferner, dass SPI1 sich an Tausenden von Genstartstellen lokalisiert und als breiter Aktivator wirkt, insbesondere für Wege, die mit Energieverbrauch, Zellbewegung und Stressreaktionen verknüpft sind. Zusammengenommen zeichnen diese Befunde SPI1 als Masterregulator, der Krebszellen in einen Hypertranskriptionszustand treibt, statt nur einige isolierte Gene zu verändern. 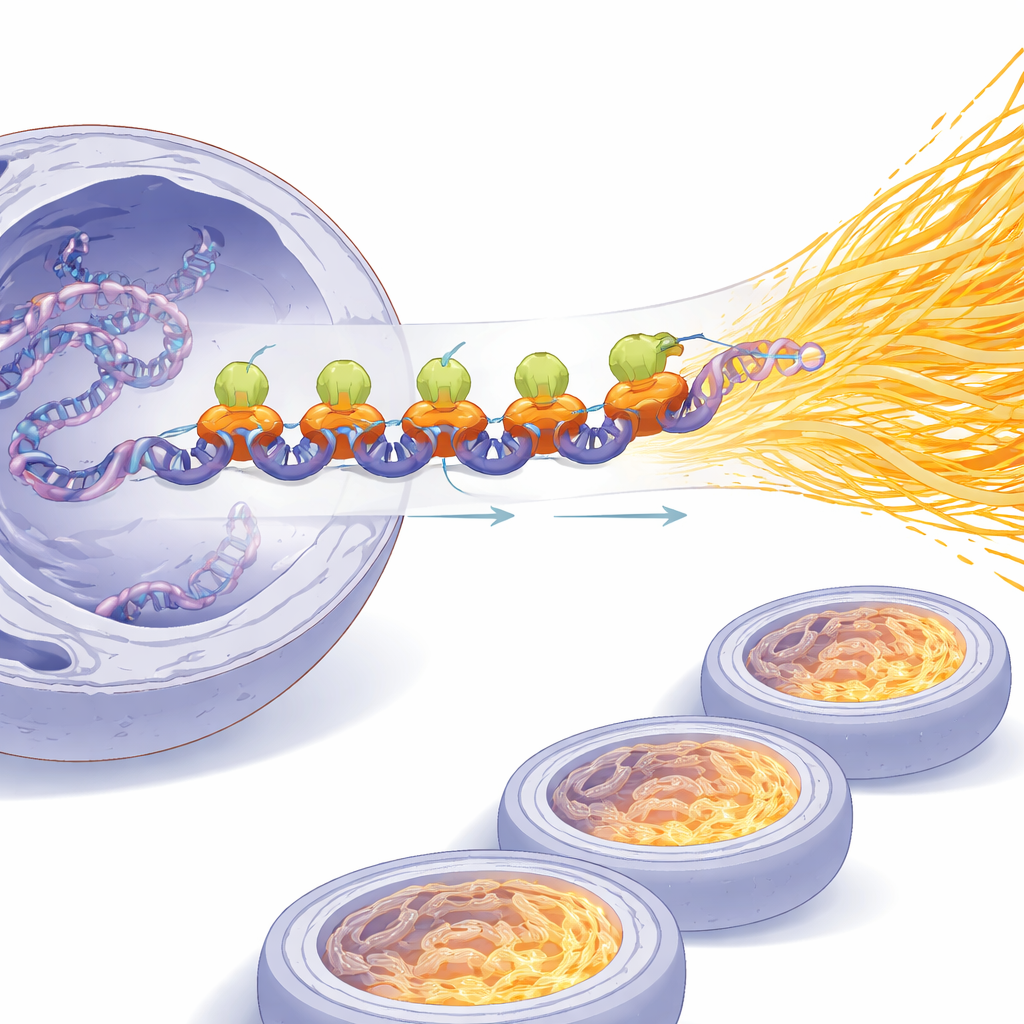
Was das für Patienten bedeutet
Schließlich untersuchten die Forschenden Tumorproben aus zwei unabhängigen Patientengruppen, die an einem einzigen Krankenhaus behandelt worden waren. Sowohl bei Kehlkopf‑ als auch bei Hypopharynxkarzinomen waren die SPI1‑Proteinlevel im Tumorgewebe deutlich höher als im umgebenden Normalgewebe. Patientinnen und Patienten, deren Tumoren mehr SPI1 enthielten, hatten eine kürzere Gesamtüberlebenszeit, und dieser Zusammenhang blieb bestehen, selbst nach Berücksichtigung gängiger klinischer Merkmale wie Stadium. Obwohl derzeit keine Medikamente direkt auf SPI1 abzielen, legt die Arbeit nahe, dass das Unterbrechen seiner Aktivität — oder der nachgeschalteten Transkriptionsmaschinerie, von der es abhängt — hohe Risiken bei Kopf‑und‑Hals‑Krebs verlangsamen oder eindämmen könnte. Einfache Worte: Die Studie zeigt, dass manche Tumoren besonders gefährlich werden, indem sie das globale "Gaspedal" der Genaktivität durchtreten, und dass SPI1 zu den Schlüsselfüßen gehört, die dieses Pedal herunterdrücken.
Zitation: Liu, Z., Qin, Z., Li, H. et al. Spi-1 proto-oncogene regulates mRNA hypertranscription and malignant progression in head and neck cancer. Sig Transduct Target Ther 11, 102 (2026). https://doi.org/10.1038/s41392-026-02669-6
Schlüsselwörter: Kopf‑und‑Hals‑Krebs, mRNA-Hypertranskription, SPI1-Transkriptionsfaktor, Tumorprogression, Krebs-Biomarker