Clear Sky Science · de
Cyclic Guanosinmonophosphat–Protein‑Kinase‑G‑Signalgebung mindert Verkalkung der Aortenklappe durch ULK1‑vermittelte Autophagie
Warum „Rost“ an der Herzklappe wichtig ist
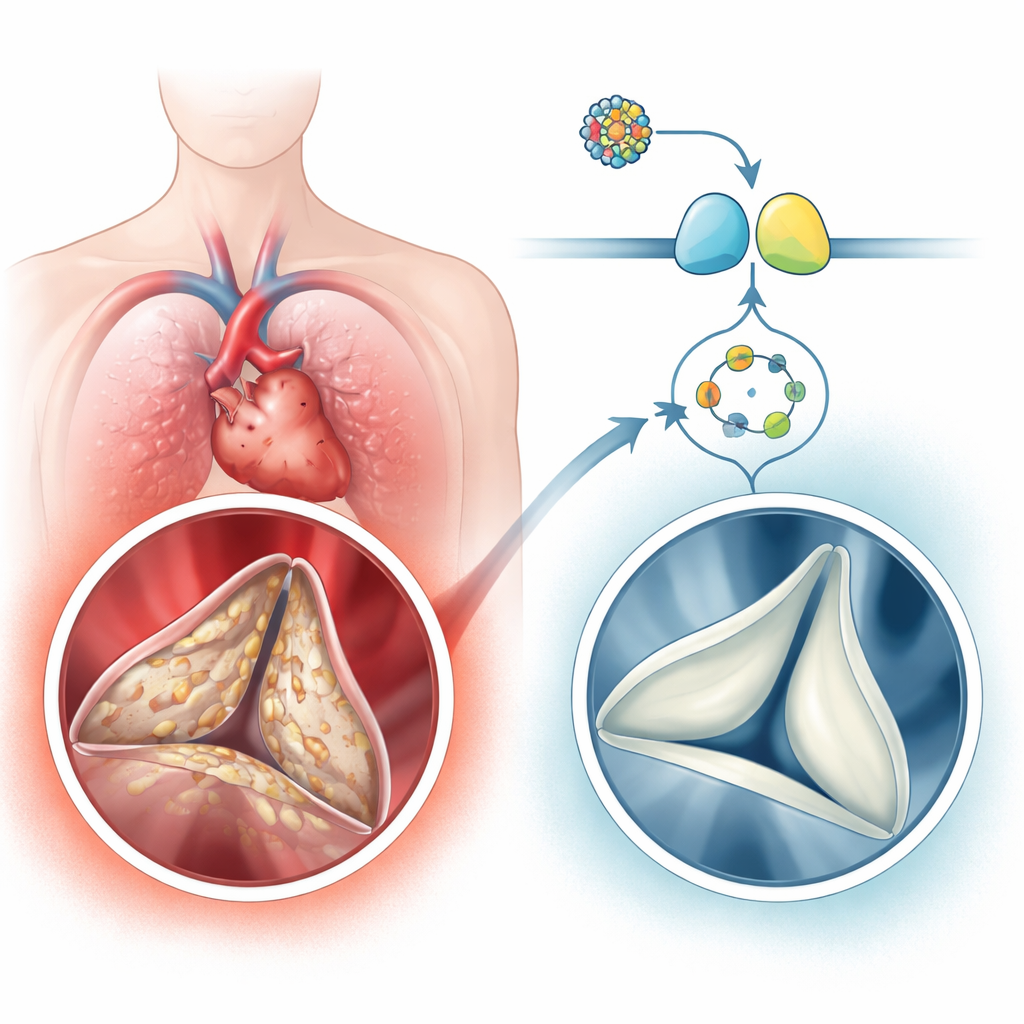
Mit zunehmendem Alter kann die Aortenklappe — das Hauptherzausflussventil — allmählich versteifen und sich mit Kalzium überziehen, ein Zustand, der als verkalkende Aortenklappenerkrankung bezeichnet wird. Dieses „Verhärten“ zwingt das Herz zu stärkerer Arbeit und kann zu Brustschmerzen, Ohnmacht, Herzinsuffizienz oder zum Bedarf an Klappenersatzoperationen führen. Derzeit gibt es kein Medikament, das diesen Prozess zuverlässig verlangsamt; Ärztinnen und Ärzte können nur abwarten, bis die Klappe stark geschädigt ist, und dann operieren. Diese Studie untersucht einen eingebauten zellulären Signalweg, der offenbar die Klappe vor Verkalkung schützt, und prüft ein modernes Herzinsuffizienz‑Medikament als möglichen Weg, diesen Schutz wieder zu aktivieren.
Ein häufiges, aber unterschätztes Herzproblem
Die verkalkende Aortenklappenerkrankung ist bei älteren Menschen überraschend verbreitet: Sie betrifft einige Prozent der über 65‑Jährigen und bis zu jeden zehnten der über 75‑Jährigen. Die Erkrankung ist nicht nur passiver „Verschleiß“. Vielmehr schalten die weichen Bindegewebszellen in der Klappe, die valvulären interstitiellen Zellen, in wundheilungs‑ und knochenähnliche Programme um. Sie legen zusätzliches Kollagen ab und lagern dann Kalzium ein, wodurch die ehemals flexiblen Segel zu steifen, steinähnlichen Klappen werden. Die Autoren analysierten menschliches Klappengewebe und große Genexpressionsdatensätze und fanden heraus, dass ein Signalweg rund um das kleine Molekül cGMP und dessen Partnerenzym Protein‑Kinase G (PKG) bei verkalkten Klappen durchgehend heruntergeregelt war, während Gene und Proteine, die mit Knochenbildung verknüpft sind, hochreguliert waren. Menschen mit starker Klappenverkalkung hatten auch niedrigere cGMP‑Spiegel im Blut, die mit dem Grad der Verengung und Obstruktion der Klappe korrelierten.
Ein schützendes Signal, das verschwindet
Um Ursache und Wirkung zu untersuchen, nutzte das Team Mäuse und kultivierte menschliche Klappenzellen. Mäuse, denen weniger PKG produziert werden konnte, entwickelten nach einer kontrollierten Verletzung der Aortenklappe dichtere, stärker verkalkte Klappensegel, und ihre Klappen zeigten höhere Spiegel eines Schlüsselproteins der Knochenbildung. In humanen Klappenzellen, die unter Bedingungen gezüchtet wurden, die Kalziumablagerungen begünstigen, beschleunigte das Herunterregeln von PKG mittels genetischer Werkzeuge diesen knochenähnlichen Umbau. Diese Ergebnisse deuten darauf hin, dass cGMP‑PKG‑Signalgebung normalerweise als Bremse gegen schädliche Zellumschaltungen in der Klappe wirkt — und wenn diese Bremse schwächer wird, beschleunigt die Verkalkung.
Ein Herzinsuffizienzmedikament neu nutzen
Die Forschenden fragten dann, ob das Anheben dieses Weges die Verkalkung verlangsamen oder umkehren könnte. Sie testeten drei Wirkstoffe, die auf unterschiedliche Weise cGMP erhöhen, darunter Vericiguat, ein zugelassenes Medikament für bestimmte Patientengruppen mit Herzinsuffizienz. In humanen Klappenzellen reduzierten alle drei Medikamente Kalziumablagerungen und Marker des knochenähnlichen Umbaus, wobei Vericiguat die stärkste Wirkung zeigte. Vericiguat verringerte außerdem die Verkalkung in kleinen Stücken menschlichen Klappengewebes, das außerhalb des Körpers am Leben gehalten wurde. In zwei Mausmodellen — einem durch cholesterinreiche Ernährung und einem durch mechanische Verletzung der Klappe — führte tägliche Vericiguat‑Behandlung zu dünneren, weniger verkalkten Klappensegeln und zu besserem Blutfluss über die Klappe, ohne die Pumpkraft des Herzens zu schwächen. Wurde PKG jedoch genetisch reduziert, verlor Vericiguat weitgehend seine Vorteile, was darauf hindeutet, dass PKG der zentrale nachgeschaltete Akteur ist.
Zelluläre Reinigung, gesündere Klappen
Tiefer gehend fanden die Forschenden, dass Vericiguat und PKG die winzigen Kraftwerke der Klappenzellen, die Mitochondrien, schützten. Unter verkalkenden Bedingungen häuften sich schädliche reaktive Sauerstoffspezies, die mitochondriale Membranpotenziale gingen verloren und es wurde weniger Energie erzeugt. Vericiguat stellte die mitochondriale Funktion wieder her und reduzierte oxidativen Stress. Umfangreiche Karten von Proteinen und Phosphatierungsstellen wiesen auf die Autophagie — das zelluläre Reinigungs‑ und Recyclingprogramm — hin. In verkalkten menschlichen Klappen zeigten mikroskopische Aufnahmen und Proteinmarker eine verringerte Bildung und Aktivität von Autophagosomen, den "Müllsäcken" der Autophagie. In Einzelzellanalysen wiesen mehrere Subtypen von Klappenzellen aus kranken Klappen eine breite Unterdrückung autophagiebezogener Programme auf. In kultivierten Zellen hob das Blockieren der Autophagie die schützende Wirkung der PKG‑Aktivierung auf, was nahelegt, dass PKG größtenteils durch Wiederbelebung dieses Reinigungsmechanismus wirkt.
Umschalten an einer molekularen Stelle
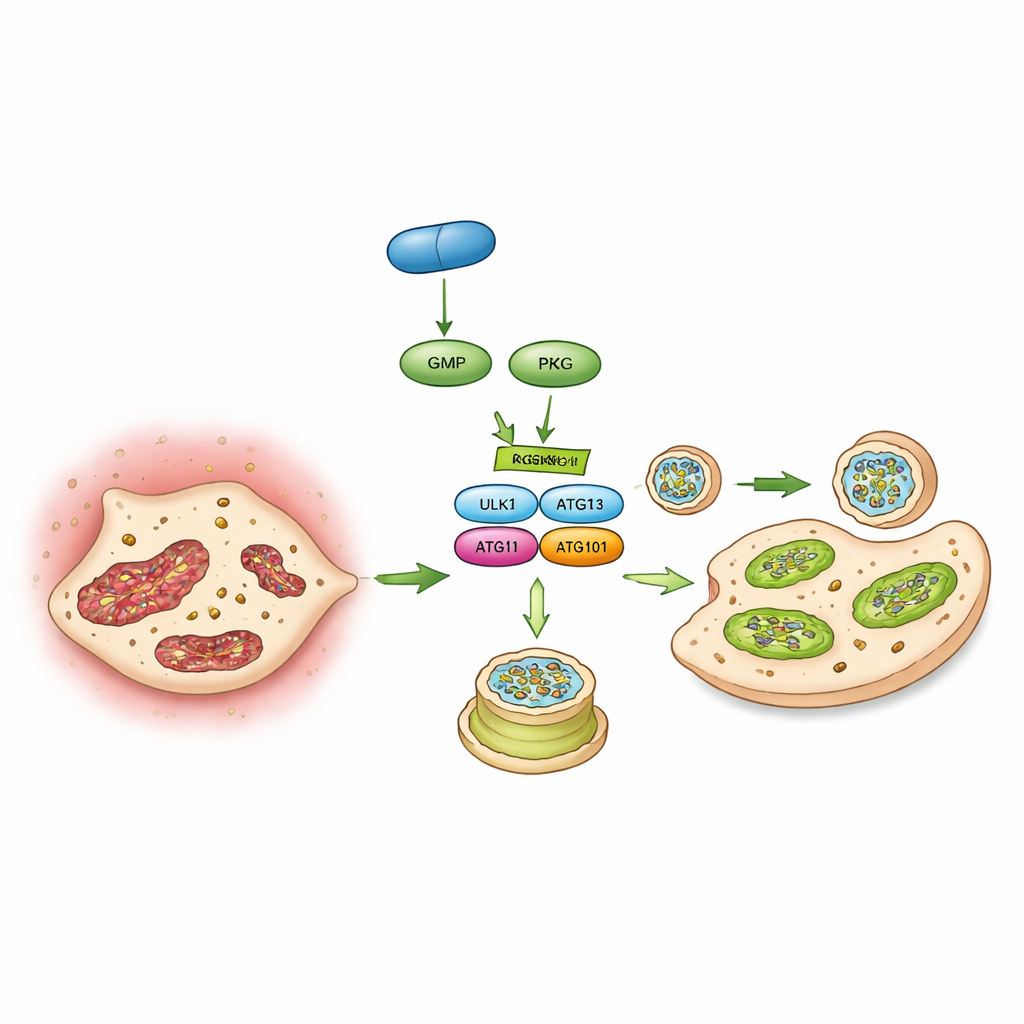
Schließlich identifizierten die Autoren einen spezifischen molekularen Schalter, der PKG mit der Autophagie verbindet: ein Protein namens ULK1, das den Start der Autophagosomenbildung einleitet. Mithilfe von Phosphoproteomik, Interaktionsstudien und Test‑Kinase‑Assays zeigten sie, dass PKG direkt eine Phosphatgruppe an ULK1 an einem bestimmten Ort anbringt (einer Aminosäure namens Serin 556). Wurde diese Stelle so verändert, dass sie nicht mehr modifiziert werden konnte, konnte PKG weder die Autophagie verstärken noch die Verkalkung in Klappenzellen blockieren. In Mäusen löschte die Expression dieses nicht ansprechbaren ULK1‑Mutanten in Klappenzellen ebenfalls die Schutzwirkung von Vericiguat aus. Zusammengenommen zeichnen diese Befunde eine Abfolge nach: Vericiguat stimuliert cGMP, das PKG aktiviert, das den ULK1‑Schalter umlegt, was die Autophagie wiederbelebt, die Mitochondrien erhält und verhindert, dass Klappenzellen zu knochenbildenden Zellen werden.
Was das für Patientinnen und Patienten bedeuten könnte
Diese Arbeit positioniert die cGMP–PKG–ULK1–Autophagie‑Achse als ein eingebautes Abwehrsystem gegen das „Rosten“ der Aortenklappe. Bei verkalkender Klappenerkrankung ist diese Verteidigung abgeschwächt, sodass Zellen Schäden akkumulieren und sich in Richtung eines knochenähnlichen Phänotyps entwickeln. Durch pharmakologisches Wiederherstellen des Signals mit einem bereits in der Herzinsuffizienztklinik eingesetzten Medikament verlangsamten die Forschenden die Verkalkung in mehreren experimentellen Modellen. Während klinische Studien am Menschen mit Klappenerkrankung notwendig sein werden, liefert die Studie eine klare, prüfbare Idee: Eine gezielte Stärkung dieses zellulären Reinigungswegs könnte eines Tages dazu beitragen, bei älteren Menschen mit Risiko für Aortenstenose das Fortschreiten zu verzögern oder den Bedarf an Klappenersatzoperationen zu verringern.
Zitation: Wang, Y., Xu, F., Song, C. et al. Cyclic guanosine monophosphate-protein kinase G signaling attenuates aortic valve calcification through ULK1-mediated autophagy. Sig Transduct Target Ther 11, 90 (2026). https://doi.org/10.1038/s41392-026-02624-5
Schlüsselwörter: verkalkende Aortenklappenerkrankung, cGMP‑PKG‑Signalgebung, Vericiguat, Autophagie, Herzklappenverkalkung