Clear Sky Science · de
Glukokortikoide erhöhen die Empfindlichkeit von klarzelligem Nierenzellkarzinom gegenüber HIF-2α-Inhibitoren durch Unterdrückung der H4K12-Laktylierung
Warum diese Studie zu Nierenkrebs wichtig ist
Das klarzellige Nierenkarzinom ist die häufigste und tödlichste Form von Nierenkrebs; viele Patientinnen und Patienten erleiden dennoch Rückfälle oder sprechen nicht auf die verfügbaren Medikamente an. Diese Studie legt eine verborgene „Abhängigkeit“ dieser Tumoren offen: Sie sind auf eine bestimmte Weise der Zuckerverbrennung angewiesen und nutzen das Abfallprodukt Laktat, um krebsfördernde Gene dauerhaft einzuschalten. Noch bedeutender ist, dass eine vertraute Medikamentenklasse – Glukokortikoide wie Dexamethason – umfunktioniert werden kann, um diese Abhängigkeit zu schwächen und ein neues zielgerichtetes Präparat, den HIF-2α-Inhibitor Belzutifan, wirksamer zu machen.
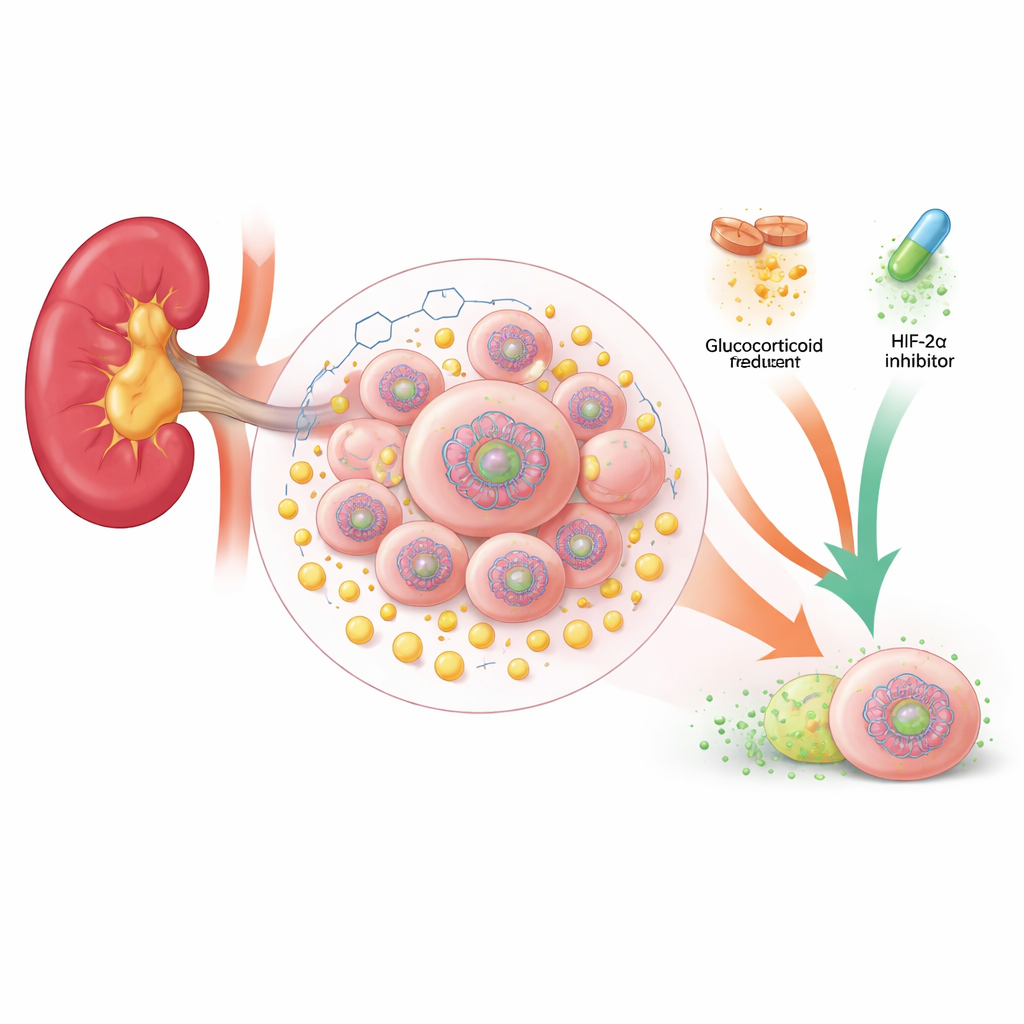
Eine zuckergetriebene Rückkopplung in Nierentumoren
Viele klarzellige Nierenkarzinome verlieren ein schützendes Schlüsselnogen namens VHL. Ohne VHL verhalten sich Zellen, als litten sie an Sauerstoffmangel, selbst wenn ausreichend Sauerstoff vorhanden ist. Sie verlagern ihren Stoffwechsel von der effizienten Energiegewinnung in den Mitochondrien hin zu einem schnellen, weniger sauberen Prozess, der Glykolyse, die viel Energie und große Mengen Laktat erzeugt. Die Autorinnen und Autoren fanden heraus, dass Laktat in VHL-defizienten Tumoren mehr ist als nur ein Abfallprodukt: Es gelangt in den Zellkern und markiert chemisch die Proteine, die die DNA verpacken. Insbesondere die Markierung H4K12-Laktylierung war in Patiententumoren auffällig erhöht und war mit größeren, aggressiveren Tumoren und schlechterem Überleben verbunden.
Wie Laktat krebsfördernde Gene dauerhaft anschaltet
Durch das Kartieren der Stellen, an denen diese laktatbasierte Markierung auf der DNA sitzt, entdeckte das Team, dass sie stark an den „Ein-/Ausschaltstellen“ (Promotoren) von Genen konzentriert ist, die Tumorwachstum und Zuckerstoffwechsel antreiben. Ein herausragendes Gen ist PGK1, ein Enzym, das die Glykolyse voranbringt und zur Laktatbildung beiträgt. In VHL-defizienten Zellen und Mausmodellen führten erhöhte PGK1-Werte zu mehr Laktat, was wiederum mehr H4K12-Laktylierung auf PGK1 und anderen Wachstumsgenen bewirkte. So entstand ein sich selbst verstärkender Kreislauf: PGK1 erhöht Laktat; Laktat dekoriert das Chromatin mit der H4K12-Markierung; diese Markierung hält PGK1 und andere tumorfördernde Gene hochaktiv und zwingt den Krebs in einen starren, hochglykolytischen Zustand.
Den Kreislauf mit vorhandenen Medikamenten durchbrechen
Die Forschenden fragten anschließend, ob zugelassene Medikamente diese Laktat–Chromatin-Rückkopplung dämpfen könnten. Ein Screening von 2.468 FDA-zugelassenen Verbindungen in Nierenkrebszellen förderte eine überraschende Trefferliste zutage: Mehrere Glukokortikoide reduzierten die H4K12-Markierung deutlich. Dexamethason war am wirksamsten und senkte die H4K12-Laktylierung bereits in niedrigen Dosen. Diese Hormone wirken über den Glukokortikoidrezeptor, ein Protein, das bei Anwesenheit des Medikaments in den Zellkern wandert und an DNA bindet. In den Krebszellen fiel das Binden des Glukokortikoidrezeptors an den Promotoren der Glykolysegene mit dem Verlust der H4K12-Markierung und einer reduzierten Aktivität von PGK1 und anderen zuckerverbrennenden Genen zusammen. Infolgedessen produzierten die Zellen weniger Laktat und wechselten wieder zu einem normaleren, sauerstoffabhängigen Stoffwechsel.
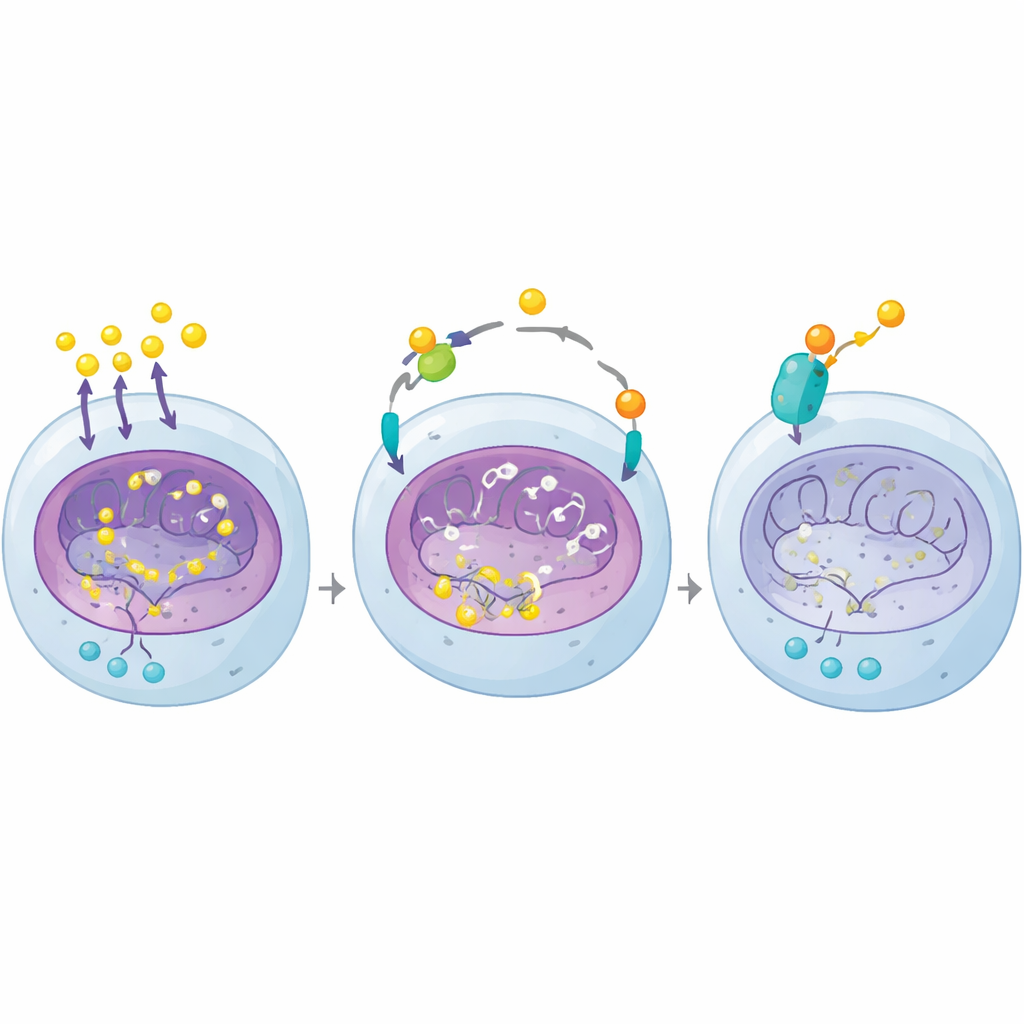
Ein zielgerichtetes Krebsmedikament wirksamer machen
Belzutifan, ein kürzlich zugelassener HIF-2α-Inhibitor, blockiert direkt einen der wichtigsten nachgelagerten Effektoreneffekte des VHL-Verlusts und hat bei Patientinnen und Patienten mit fortgeschrittenem klarzelligem Nierenkrebs Nutzen gezeigt. Die Ansprechraten sind jedoch unvollständig und oft von kurzer Dauer. Da Dexamethason das laktatgetriebene Chromatinprogramm des Krebses aus einem anderen Winkel angreift, prüften die Autoren die Kombination beider Medikamente in Mausmodellen. In Tumoren, die aus Zelllinien und Patientengewebe gewachsen waren, schrumpften VHL-defiziente Tumoren durch die Kombination aus Glukokortikoiden und Belzutifan deutlich stärker als durch eine der Behandlungen allein. Die Kombination verringerte die H4K12-Laktylierung und reduzierte die Spiegel wichtiger glycolytischer und nierenspezifischer Gene, die mit Tumorwachstum verknüpft sind, während in Tierversuchen normales Gewebe geschont blieb.
Was das für Patientinnen, Patienten und zukünftige Therapien bedeutet
Diese Arbeit zeigt, dass viele klarzellige Nierenkarzinome in einem Teufelskreis gefangen sind: Ein VHL-Defekt treibt einen zuckerhungrigen Stoffwechsel an, der Laktat erzeugt; dieses Laktat modifiziert chemisch das Chromatin und hält dieselben Wachstums- und Stoffwechselgene dauerhaft aktiv. Die Studie demonstriert, dass Glukokortikoide, bisher vor allem wegen ihrer entzündungshemmenden Wirkung eingesetzt, auch als gezielte epigenetische Wirkstoffe wirken können, die diesen laktatgetriebenen Kreislauf beruhigen und Tumoren für eine HIF-2α-Blockade empfindlicher machen. Sorgfältige klinische Prüfungen sind erforderlich – vor allem weil Glukokortikoide das Immunsystem unterdrücken können – doch die Ergebnisse deuten auf eine praktikable, auf den Mechanismus gestützte Kombinationsstrategie hin, die bestehende zielgerichtete Therapien für Menschen mit diesem schwer zu behandelnden Nierenkrebs wirksamer machen könnte.
Zitation: Zhang, K., He, L., Wang, Y. et al. Glucocorticoids elevate clear cell renal cell carcinoma sensitivity to HIF-2α inhibitors by suppressing H4K12 lactylation. Sig Transduct Target Ther 11, 117 (2026). https://doi.org/10.1038/s41392-026-02622-7
Schlüsselwörter: klarzelliges Nierenzellkarzinom, Tumorstoffwechsel, Histon-Laktylierung, Glukokortikoide, HIF-2α-Inhibitor Belzutifan