Clear Sky Science · de
Wirksamkeit und immunmodulatorische Wirkung von Claudin18.2-spezifischen, mit IL-7/XCL1 ausgestatteten CAR-T-Zellen bei Krebserkrankungen des Verdauungstrakts: präklinische und klinische Analyse
Das Immunsystem gegen Krebserkrankungen des Verdauungstrakts einsetzen
Magen- und Bauchspeicheldrüsenkrebs gehören zu den tödlichsten Tumoren, zum Teil weil sie häufig gegenüber Operation, Chemotherapie und Strahlentherapie resistent sind. Diese Studie untersucht einen neuen Ansatz, um diese Tumoren zu bekämpfen, indem die körpereigenen Immunzellen so verstärkt werden, dass sie in feste Tumoren eindringen, dort überleben und Verstärkung herbeirufen können. Durch die Umgestaltung krebsbekämpfender T‑Zellen, damit sie nützliche Immun‑Signale freisetzen, zielen die Forschenden nicht nur darauf ab, Tumoren direkt anzugreifen, sondern auch das übrige Immunsystem innerhalb der feindlichen Tumorumgebung zu aktivieren.
Warum solide Tumoren schwer zu behandeln sind
Moderne Zelltherapien, sogenannte CAR-T-Zellen, haben in Blutkrebserkrankungen dramatische Ergebnisse erzielt und einige Patienten geheilt, die keine anderen Optionen mehr hatten. Solide Tumoren wie jene des Verdauungstrakts stellen jedoch zusätzliche Hürden dar. Ihre Zellen variieren von Ort zu Ort, das Tumorinnere ist an Nährstoffen und Sauerstoff mangelhaft versorgt, und eine Mischung aus unterdrückenden Zellen und Signalmolekülen dämpft Immunangriffe. Frühere Generationen von CAR-T-Zellen konnten Zielmoleküle auf Zellen von Verdauungskrebs erkennen, scheiterten aber oft daran, sich in dieser harschen Umgebung zu vermehren, anzudauern und funktionsfähig zu bleiben, was ihre Wirksamkeit in der Praxis begrenzte.
Ein intelligenteres Design für gentechnisch veränderte T‑Zellen
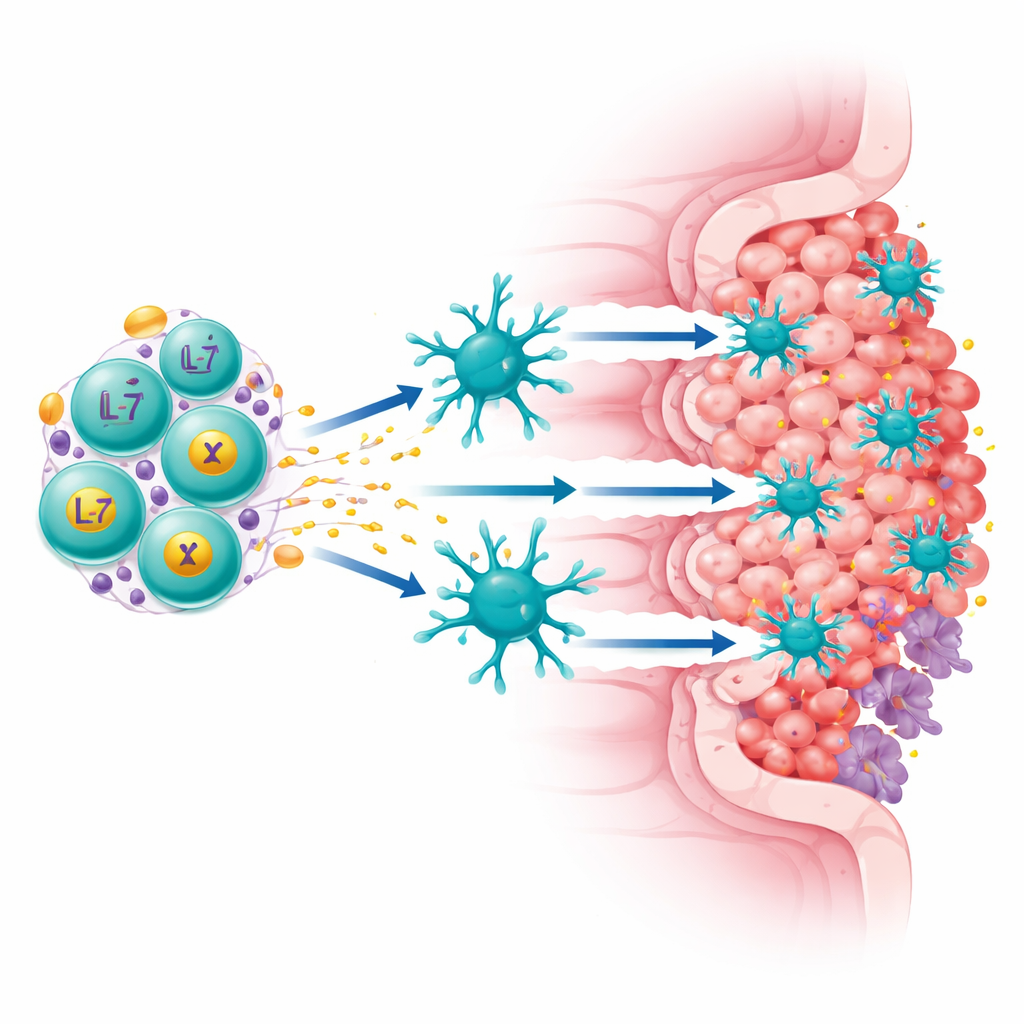
Das Team konzentrierte sich auf ein Protein namens Claudin18.2, das auf vielen Magen‑ und Bauchspeicheldrüsenkrebszellen in hohen Mengen vorkommt, in normalem Gewebe jedoch weitgehend fehlt. Sie entwickelten eine „vierte Generation“ von CAR-T-Zellen, die zwei Aufgaben gleichzeitig erfüllt: Sie erkennt Claudin18.2 auf Tumorzellen und setzt kontinuierlich zwei immunfördernde Faktoren frei, IL‑7 und XCL1. IL‑7 hilft T‑Zellen beim Überleben und fördert einen langlebigen, stammzellähnlichen Zustand, während XCL1 als Lockstoff wirkt und eine seltene, aber potente Art von Immunzellen anzieht, die cDC1 genannt werden und besonders gut darin sind, Killer‑T‑Zellen zu aktivieren. Diese aufgerüsteten Zellen, ExCAR‑T oder RD07 genannt, sind nicht nur dazu angelegt, das zu töten, was sie erkennen, sondern auch die immunologische Landschaft des Tumors umzugestalten.
Starke Tumorkontrolle in präklinischen Modellen
In Mausmodellen von Krebserkrankungen des Verdauungstrakts schnitten ExCAR‑T‑Zellen besser ab als konventionelle CAR-T-Zellen ohne IL‑7 und XCL1. Im Labor töteten die konstruierten Zellen mehr Krebszellen und enthielten mehr langlebige, gedächtnisähnliche T‑Zellen. Bei Tieren mit Claudin18.2-positiven Tumoren führten ExCAR‑T‑Behandlungen zu stärkeren Tumorrückbildungen und verlängertem Überleben im Vergleich zu Standard‑CAR‑T‑Zellen. Die verbesserten Zellen vermehrten sich im Blut besser und lösten eine breitere Immunantwort aus, einschließlich Signalen, die zusätzliche Immunzellen anlocken, während Faktoren, die mit Tumorprogression verbunden sind, reduziert wurden. Auffällig war, dass Mäuse, die durch ExCAR‑T geheilt wurden, einer erneuten Herausforderung mit Krebszellen ohne Claudin18.2‑Target widerstanden — ein Hinweis darauf, dass die Therapie ein dauerhaftes, tumorweites Immungedächtnis ausgelöst hatte und nicht nur eine enge Ein‑Ziel‑Antwort.
Erste Ergebnisse einer klinischen Studie bei Patienten
Ermutigt durch diese Daten starteten die Forschenden eine Erst‑in‑Mensch‑Studie mit RD07 bei 12 Personen mit fortgeschrittenem Magen‑, gastroösophagealem Übergangs‑ oder Bauchspeicheldrüsenkrebs, die bereits Standardtherapien erfolglos durchlaufen hatten. Nebenwirkungen waren insgesamt beherrschbar: Die schwerwiegendsten Probleme waren Blutzellabsenkungen infolge der prä‑Infusions‑Chemotherapie, und es traten nur milde Zytokinfreisetzungsreaktionen auf; schwerwiegende neurotoxische Ereignisse wurden nicht beobachtet. Von 10 auswertbaren Patienten zeigten 7 messbare Tumorverkleinerungen und 2 erreichten partielle Remissionen. Patienten mit moderat bis hoch exprimierendem Claudin18.2 sprachen besonders gut an: Jeder dieser Patienten erreichte mindestens eine Krankheitsstabilisierung, und einige lebten deutlich länger als erwartet. Bei diesen Ansprechern vermehrten sich die modifizierten T‑Zellen stärker im Blut, und die Blutspiegel von IL‑7 und XCL1 stiegen entsprechend dem Design der Therapie an.
Blick in die immunologische Nachbarschaft des Tumors
Um zu verstehen, wie RD07 beim Menschen wirkt, untersuchte das Team Tumorproben auf Einzelzell‑Ebene vor und nach der Behandlung. Sie beobachteten, dass der Anteil Claudin18.2‑positiver Krebszellen bei ansprechenden Patienten sank, was bestätigt, dass die Therapie ihr vorgesehenes Ziel traf. Gleichzeitig stieg die Vielfalt der T‑Zellklone an, einschließlich aktiver Killerzellen und geweberesidenter Gedächtniszellen, was darauf hindeutet, dass der Körper eine breitere Immunoffensive startete. Spezialisierte dendritische Zellen zeigten Zeichen gesteigerter Aktivität und stärkere Interaktionen mit proliferierenden T‑Zellen, was mit der Rekrutierung durch XCL1 übereinstimmt. Bildgebende Untersuchungen eines Tumorschnitts eines Patienten zeigten nach der Behandlung weniger Tumor‑ und suppressive myeloide Zellen, dafür mehr T‑ und B‑Zellen und eine Umstrukturierung des Gewebes in immunreichere Zonen — Kennzeichen einer „wärmeren“, stärker entzündeten Mikroumgebung.
Was das für die zukünftige Krebsbehandlung bedeuten könnte
Insgesamt deuten die präklinischen und frühen klinischen Befunde darauf hin, dass RD07 mehr leistet, als nur ein weiteres zielgerichtetes Medikament zum Arsenal gegen Krebs hinzuzufügen. Durch die Kombination von Tumorerkennung mit eingebauter immunologischer Unterstützung können diese gentechnisch veränderten T‑Zellen länger überleben, wichtige Partnerzellen rekrutieren und das körpereigene Immunsystem darin schulen, den Tumor unter Kontrolle zu halten — selbst wenn das ursprüngliche Ziel verloren geht. Obwohl die Studie klein war und an stark vorbehandelten Patienten durchgeführt wurde, sind die konsistente Tumorverkleinerung, die akzeptable Sicherheit und die tiefgreifende immunologische Umgestaltung vielversprechend. Bestätigen größere Studien diese Ergebnisse, könnte dieser Ansatz ein neues Kapitel in der Behandlung von Krebserkrankungen des Verdauungstrakts aufschlagen, in dem das Stärken des immunologischen Ökosystems im Tumor ebenso wichtig wird wie der direkte Angriff auf Krebszellen.
Zitation: Zhao, X., Liu, J., Zhang, Z. et al. Efficacy and immunomodulatory effect of Claudin18.2-specific IL-7/XCL1 armored CAR-T cells in digestive tract cancer: preclinical and clinical analysis. Sig Transduct Target Ther 11, 87 (2026). https://doi.org/10.1038/s41392-026-02621-8
Schlüsselwörter: CAR-T-Zelltherapie, Krebs des Verdauungstrakts, Tumormikroumgebung, Claudin18.2, Immuntherapie