Clear Sky Science · de
Visinin-ähnliches Protein 1 stört die Kalzium-Homöostase und fördert Vorhofflimmern in menschlichen und tierischen Modellen
Warum diese Geschichte zum Herzrhythmus wichtig ist
Vorhofflimmern ist eine häufige Herzrhythmusstörung, die das Risiko für Schlaganfall und Herzinsuffizienz erhöht. Viele Menschen leben damit, doch Ärztinnen und Ärzte haben nach wie vor Schwierigkeiten, das Auftreten zu verhindern oder Rückfälle nach einer Behandlung zu vermeiden. Diese Studie entdeckt ein bislang wenig beachtetes Protein in Herzmuskelzellen, genannt VILIP-1, das wie ein fehlerhafter Kalzium-Schalter wirkt und Vorhofflimmern bei Menschen und Tieren antreibt. Indem die Studie diesen Schalter identifiziert und zeigt, dass bereits verfügbare Medikamente ihn abschwächen können, eröffnet sie einen neuen Weg zu sichereren, gezielteren Therapien.
Ein genauerer Blick auf einen chaotischen Herzschlag
In einem gesunden Herzen breiten sich elektrische Wellen geordnet durch die oberen Herzkammern, die Vorhöfe, aus und steuern jeden Herzschlag. Diese Ordnung hängt stark von Kalzium ab, einem geladenen Mineral, das in Herzzellen ein- und ausströmt, um Kontraktion und Entspannung zu koordinieren. Beim Vorhofflimmern gerät dieser Kalziumverkehr aus dem Ruder: vermehrte Lecks und Schwankungen der Kalziumspiegel lösen fehlgeleitete elektrische Signale aus, die sich zu schnellen, unregelmäßigen Rhythmen auswachsen können. Ärztinnen und Ärzte wissen seit Jahren, dass eine Fehlregulation von Kalzium zentral für diese Störung ist, doch die auslösenden Faktoren sind bislang unklar geblieben.
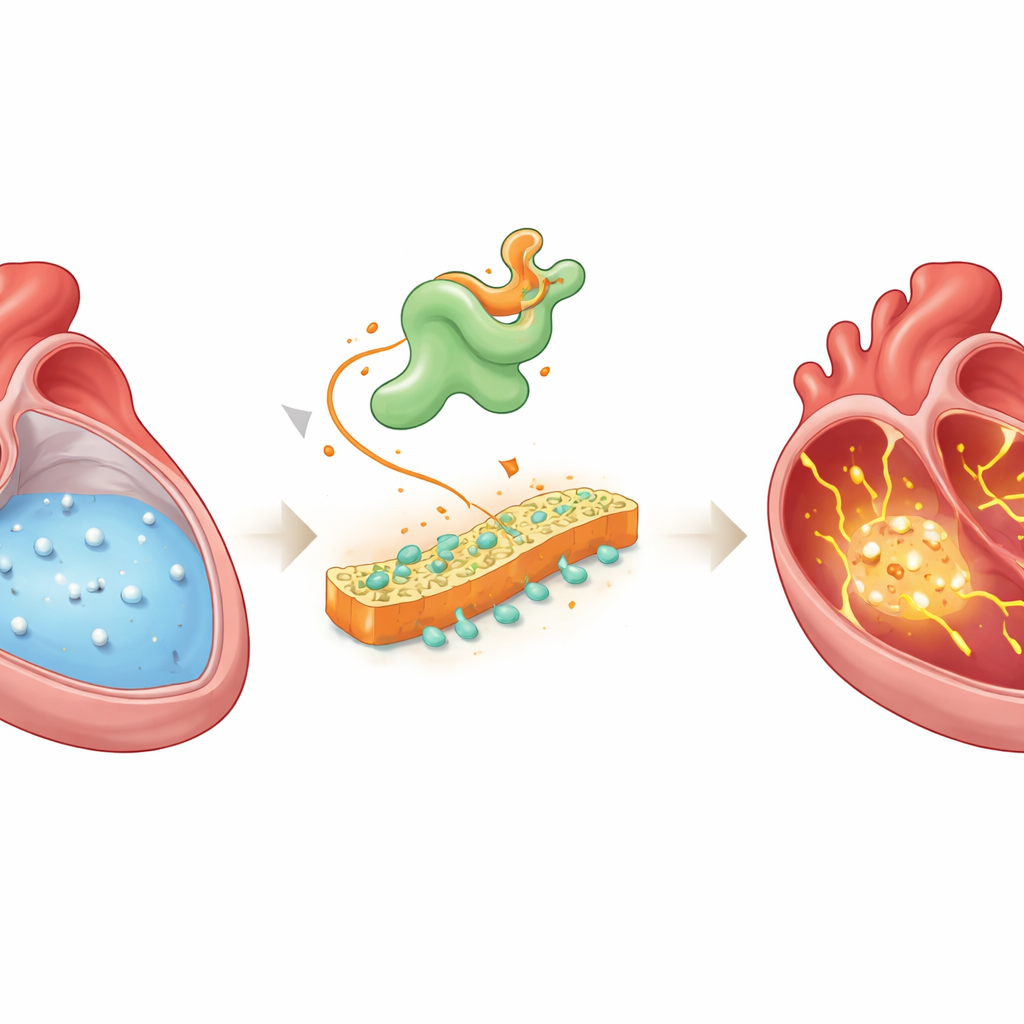
Ein versteckter Übeltäter wird gefunden
Die Forschenden kombinierten mehrere fortschrittliche Ansätze, um Moleküle zu suchen, die gestörtes Kalziumhandling mit Vorhofflimmern verknüpfen. Sie zeichneten Kalziumsignale Hunderter einzelner Vorhofzellen von Ratten mit tachykardieinduziertem Vorhofflimmern auf und sequenzierten dann die gesamte aktive Genexpression derselben Zellen. Außerdem verglichen sie Genaktivität in Vorhofgewebe von Patientinnen und Patienten mit Vorhofflimmern mit der von Personen mit normalem Rhythmus. Als sie diese Datensätze überlagerten und verfolgten, wie sich Zellen auf dem Weg vom gesunden zum erkrankten Zustand veränderten, stach ein Gen wiederholt hervor: Vsnl1, das das Protein VILIP-1 produziert, ein Kalzium-sensitives Molekül, das bisher vor allem im Gehirn und in der Bauchspeicheldrüse untersucht worden war, nicht im Herzen.
Wie VILIP-1 das Kalziumgleichgewicht stört
In Vorhofgewebe von Patienten und Tiermodellen waren die VILIP-1-Spiegel deutlich erhöht, und das Protein war an der Zelloberfläche konzentriert. Um zu prüfen, ob diese Veränderung bloßer Begleiterscheinung oder Treiber ist, veranlasste das Team in Mäusen eine gesteigerte Produktion von VILIP-1 in Vorhofzellen. Diese Mäuse zeigten keine offensichtlichen strukturellen Schäden am Herzen, doch ihre Vorhöfe ließen sich durch elektrische Stimulation wesentlich leichter in Vorhofflimmern überführen. Detaillierte elektrische Aufzeichnungen zeigten vermehrt verzögerte Nachdepolarisierungen—abnorme Auslenkungen nach jedem Schlag—und Schlag-zu-Schlag-Variationen in der Aktionspotenzialform, klassische Zeichen instabiler elektrischer Aktivität, die mit Kalziumüberladung verbunden sind. Hochauflösende Kalziumbildgebung bestätigte häufige spontane Kalziumwellen und erschöpfte interne Kalziumspeicher, was auf schwere Lecks innerhalb der Zellen hinweist.
Der kritische Partner an der Zelloberfläche
Um zu verstehen, wie VILIP-1 diese Störung verursacht, kartierten die Wissenschaftlerinnen und Wissenschaftler, welche Proteine in Herzmuskelzellen mit ihm interagieren. Mithilfe zweier komplementärer Methoden—dem Herausziehen von Bindungspartnern aus Vorhofgewebe und dem Markieren benachbarter Proteine durch eine „Biotin-Hülle“ in lebenden Zellen—fanden sie NCX-1, den hauptsächlichen Natrium–Kalzium-Austauscher in der Membran der Herzoberfläche. Dieser Austauscher hilft normalerweise, Kalzium gegen Natrium auszuleiten, kann aber unter bestimmten Bedingungen umkehren und Kalzium in die Zelle treiben. Die Studie zeigte, dass VILIP-1 physisch an NCX-1 bindet und die Anzahl der NCX-1-Moleküle in der Membran erhöht, ohne die Gesamtproduktion von NCX-1 zu steigern. Infolgedessen wurden die Austauscherströme größer, und die Blockade von NCX-1 mit einem selektiven Inhibitor reduzierte Kalziumwellen und erschwerte das Auslösen von Vorhofflimmern in Mäusen mit überschüssigem VILIP-1.
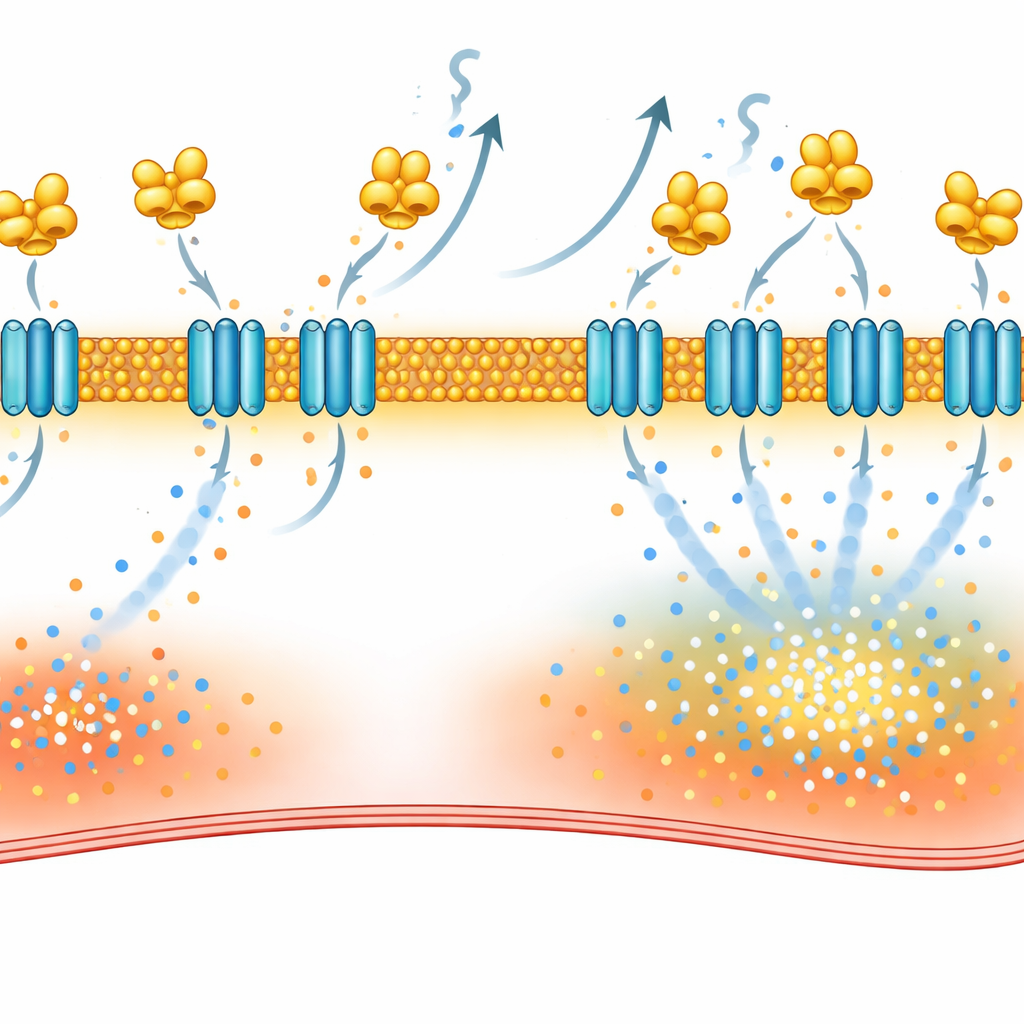
Den fehlerhaften Schalter mit vorhandenen Medikamenten abschalten
VILIP-1 verankert sich an Membranen durch einen fetthaltigen Anhängsel namens Myristat, der sichtbar wird, wenn Kalzium an das Protein bindet. Das Team verwendete Desloratadin, das zuvor gezeigt hatte, dass es diesen Verankerungsschritt stören kann, und fand heraus, dass es NCX-1 an der Zelloberfläche verringerte, die Austauscherströme normalisierte, Kalziumwellen reduzierte und Vorhofflimmer-Episoden in Rattenmodellen verringerte. Sie testeten auch Repaglinid, ein Diabetesmedikament, das dafür bekannt ist, verwandte Kalziumsensoren zu binden. Biophysikalische Tests bestätigten, dass Repaglinid direkt an VILIP-1 bindet. In stimulierten Ratten und in Vorhofgewebe von Patientinnen und Patienten mit Vorhofflimmern reduzierte Repaglinid NCX-1 in der Membran, beruhigte Kalziumleckagen in einzelnen Zellen und verringerte deutlich die Auslöseempfindlichkeit für Vorhofflimmern.
Was das für Menschen mit unregelmäßigem Herzschlag bedeutet
Insgesamt skizziert die Studie einen sich selbst verstärkenden Kreislauf: Steigende Kalziumwerte rekrutieren VILIP-1 an die Zelloberfläche, wo es NCX-1 verstärkt, was wiederum zu weiterer Kalziumüberladung führt und die Bühne für Vorhofflimmern bereitet. Indem man diesen Kreislauf auf der Ebene von VILIP-1 unterbricht—entweder durch Blockade seines fetthaltigen Ankers oder durch Bindung seines Kalzium-sensitiven Kerns—können vorhandene Medikamente ein stabileres Kalziumgleichgewicht wiederherstellen und die Anfälligkeit für Arrhythmien in menschlichem und tierischem Herzgewebe vermindern. Während weitere Arbeit nötig ist, um die Wirkstoffspezifität zu verfeinern und diese Strategien in größeren Tiermodellen und klinischen Studien zu prüfen, tritt VILIP-1 nun als vielversprechender neuer Ansatzpunkt zur Vorbeugung und Behandlung dieser weit verbreiteten und oft hartnäckigen Herzrhythmusstörung hervor.
Zitation: Xiong, K., Wang, G., Li, D. et al. Visinin-like protein 1 disrupts calcium homeostasis and promotes atrial fibrillation in human and rodent models. Sig Transduct Target Ther 11, 105 (2026). https://doi.org/10.1038/s41392-026-02615-6
Schlüsselwörter: Vorhofflimmern, Kalzium-Signalübertragung, Herzrhythmusstörung, Sodum-Kalzium-Austauscher, therapeutische Zielstrukturen