Clear Sky Science · de
SHR-A1811, ein neuartiges HER2‑zielgerichtetes Antikörper‑Wirkstoffkonjugat bei fortgeschrittenen soliden Tumoren (HORIZON‑X): eine globale Phase‑1‑Studie
Neue Hoffnung für Menschen mit ausgeschöpften Optionen
Für viele Menschen mit fortgeschrittenem Krebs hören Standardtherapien irgendwann auf zu wirken, sodass nur noch wenige sinnvolle Optionen bleiben. Diese Studie prüft eine neue Form einer zielgerichteten Krebstherapie namens SHR‑A1811 bei Patientinnen und Patienten, deren Tumoren zusätzliche Kopien oder Mutationen des Wachstumssignals HER2 aufweisen. Die Teilnehmenden hatten bereits mehrere Therapielinien durchlaufen. Die zentrale Frage war, ob dieses Prüfpräparat Tumoren langfristig verkleinern kann, ohne gefährliche Nebenwirkungen zu verursachen.
Eine intelligente Rakete gegen Krebszellen
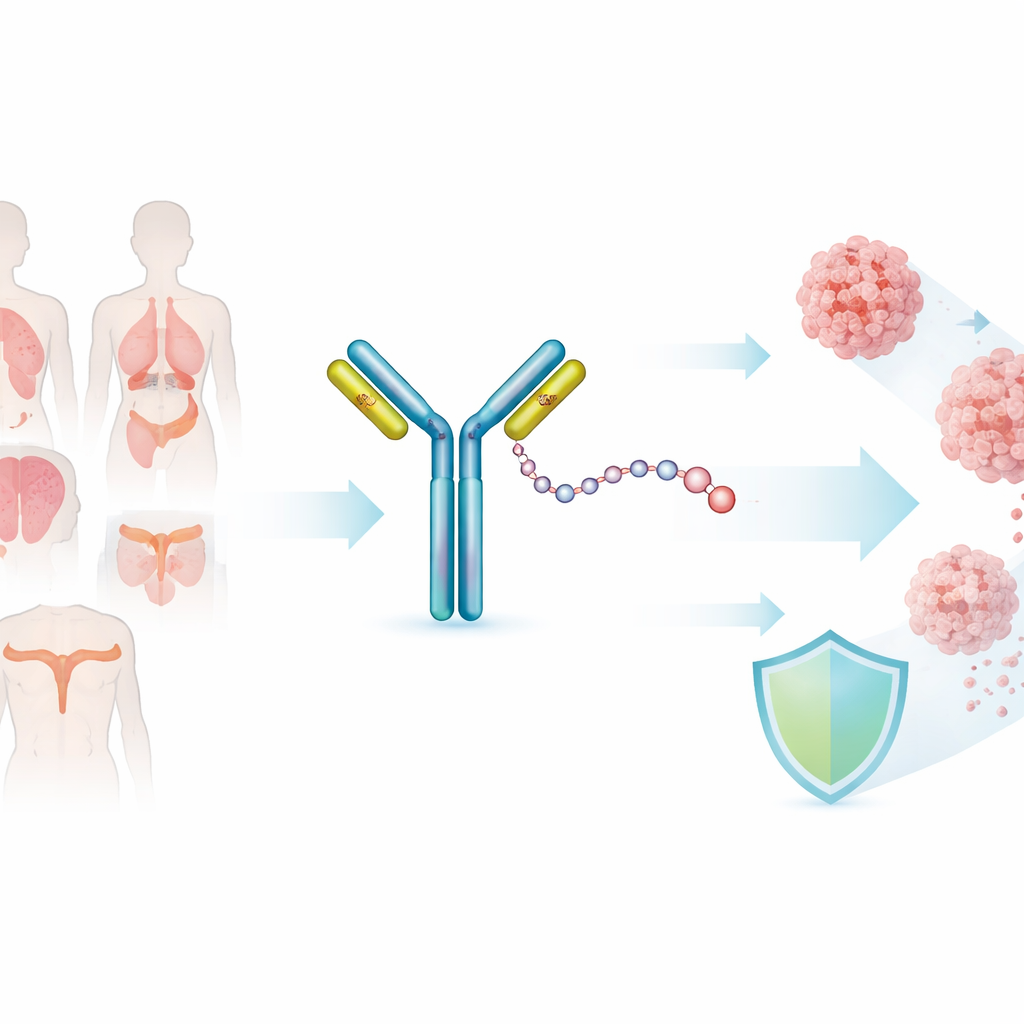
SHR‑A1811 gehört zu einer neueren Medikamentenklasse, den Antikörper‑Wirkstoff‑Konjugaten, die oft als „intelligente Raketen“ beschrieben werden. Ein Teil des Medikaments ist ein Antikörper, der HER2 erkennt, ein Protein, das auf einigen Krebszellen in hohen Mengen vorkommt. Der andere Teil ist ein sehr wirksames Chemotherapeutikum, das allein zu toxisch wäre. Ein spezieller chemischer Linker verbindet diese Komponenten. Die Idee ist, dass der Antikörper die toxische Nutzlast direkt an HER2‑markierte Tumorzellen bringt, wo sie innerhalb der Krebszelle freigesetzt wird und gesundes Gewebe weitgehend schont.
Wer die neue Behandlung erhielt
Diese globale Phase‑1‑Studie rekrutierte 396 erwachsene Patientinnen und Patienten mit fortgeschrittenen oder metastasierten soliden Tumoren an 38 Krankenhäusern. Alle Tumoren produzierten entweder zusätzliches HER2 oder trugen HER2‑Mutationen. Die Mehrheit hatte Brustkrebs, andere hatten Gallengangskarzinome, Blasen‑, Eierstock‑ und Gebärmutterkrebs, Kolon‑, Magen‑, Lungen‑, Pankreas‑ und weitere Tumoren. Im Durchschnitt hatten die Patientinnen und Patienten bereits drei bis vier vorherige Therapieschemata gegen die metastasierte Erkrankung erhalten, was auf schwer kontrollierbare Tumoren hinweist. SHR‑A1811 wurde als intravenöse Infusion alle drei Wochen in unterschiedlichen Dosen verabreicht, um eine geeignete Dosis zu finden und Sicherheit sowie frühe Anzeichen von Wirksamkeit zu beobachten.
Abwägung von Nebenwirkungen und Sicherheit
Fast alle Patientinnen und Patienten erlebten Nebenwirkungen, wie bei starken Krebsmedikamenten zu erwarten. Die häufigsten Probleme waren Abfälle der Blutwerte, einschließlich weißer und roter Blutkörperchen sowie Thrombozyten, was das Infektionsrisiko erhöhen und Müdigkeit oder Blutergüsse verursachen kann. Diese ließen sich meist durch Dosisanpassungen handhaben, und nur etwa eine von zehn Personen brach die Behandlung wegen Nebenwirkungen ab. Ein zentrales Sicherheitsrisiko bei ähnlichen Präparaten ist Vernarbung und Entzündung der Lungen, die lebensbedrohlich sein kann. In dieser Studie traten Lungenprobleme jeglicher Schwere bei nur 2,5 % der Patientinnen und Patienten auf, meist mild; nur eine Patientin bzw. ein Patient starb an dieser Komplikation bei der höchsten Dosis. Insgesamt blieb das Sicherheitsprofil über mehr als zwei Jahre Nachbeobachtung stabil, ohne neue oder unerwartete Risiken.
Schrumpfende Tumoren und anhaltende Kontrolle
Die Ergebnisse zur Tumorkontrolle waren für so stark vorbehandelte Patientengruppen bemerkenswert. Über alle Tumorarten hinweg sahen fast 60 % der Patientinnen und Patienten eine Tumorverkleinerung, bei einigen verschwand sichtbare Erkrankung vollständig in bildgebenden Verfahren. Bei HER2‑positivem Brustkrebs schrumpfte der Tumor bei etwa vier von fünf Patientinnen und Patienten, und die mediane Zeit bis zum Wiederauftreten des Wachstums betrug etwas mehr als zwei Jahre. Patientinnen und Patienten mit geringeren HER2‑Spiegeln im Brusttumor profitierten ebenfalls, mit einer medianen Krankheitskontrolle von nahezu einem Jahr. Für Nicht‑Brust‑Tumoren – darunter Gallengang, Blase, gynäkologische Tumoren, Kolorektal, Magen und Lunge – waren die Ansprechraten unterschiedlich, aber überwiegend ermutigend, viele Patientinnen und Patienten erzielten mehrere Monate zusätzliche Krankheitskontrolle. Wichtig ist, dass die Ansprecheffekte tendenziell anhielten: Unter denen, deren Tumoren schrumpften, behielten viele ihren Nutzen ein Jahr oder länger.
Erreichen von Tumoren mit kaum nachweisbarem Ziel
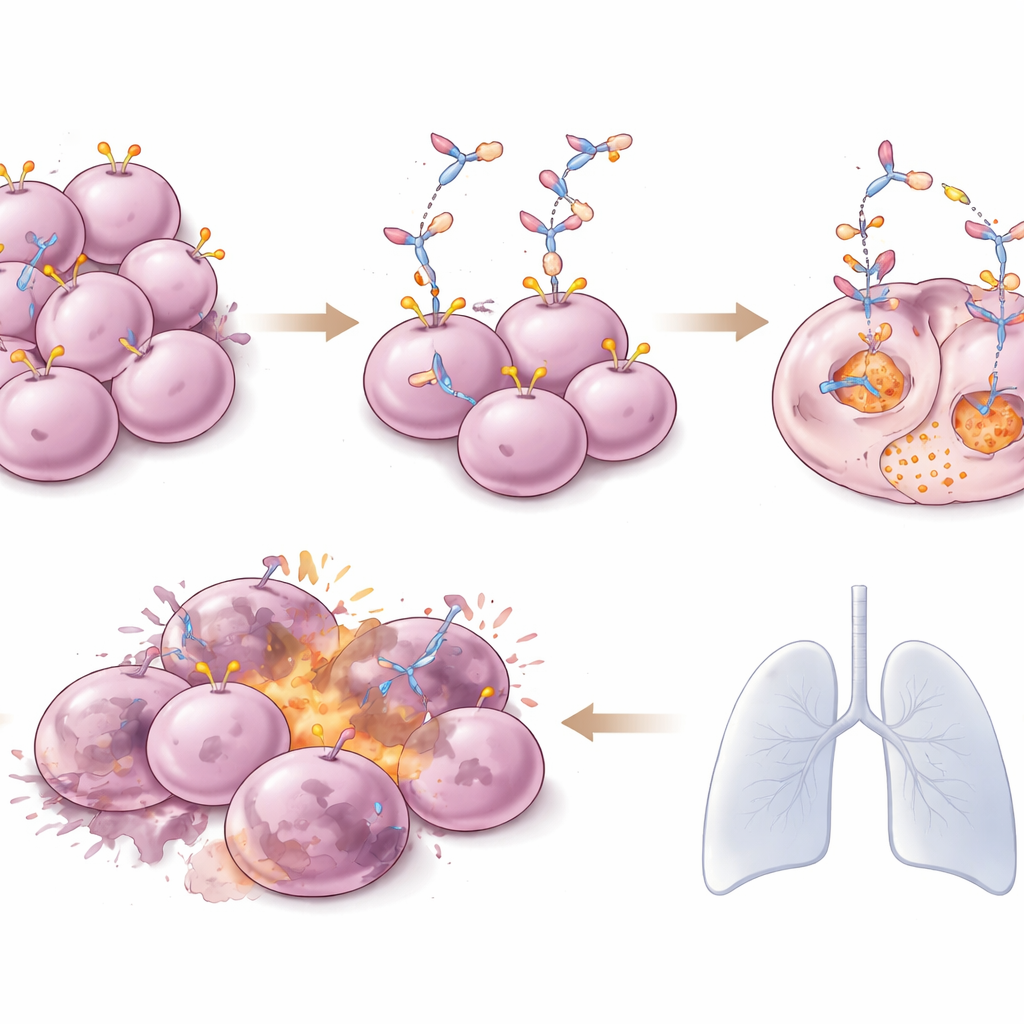
Ein interessantes Ergebnis war, dass SHR‑A1811 einigen Patientinnen und Patienten half, deren Tumoren nur sehr wenig nachweisbares HER2 aufwiesen – Werte, die traditionell als zu gering für eine HER2‑gerichtete Therapie gelten. In dieser Gruppe sah mehr als die Hälfte trotzdem Tumorverkleinerungen, und die Krankheitskontrolle hielt im Mittel etwa zehn Monate an. Laboruntersuchungen deuten darauf hin, dass dies dadurch möglich wird, dass die freigesetzte toxische Nutzlast in einer HER2‑markierten Zelle in benachbarte Krebszellen ohne viel HER2 eindringen kann – ein sogenannter „Bystander‑Effekt“. Das legt nahe, dass das Medikament potenziell einem breiteren Patientenkreis helfen könnte als die klassischen HER2‑Definitionen vermuten lassen.
Was das für Menschen mit fortgeschrittenem Krebs bedeutet
Insgesamt zeigt die Langzeitnachbeobachtung der HORIZON‑X‑Studie, dass SHR‑A1811 in vielen Patientinnen und Patienten mit bereits gegen mehrere Therapien resistenten HER2‑bezogenen Tumoren eine starke und anhaltende Tumorkontrolle erreichen kann, während schwere Nebenwirkungen – insbesondere Lungenschäden – relativ selten blieben. Auch wenn dies kein direkter Vergleichstest war, erscheinen die Ergebnisse mindestens vergleichbar mit einem bereits zugelassenen HER2‑gerichteten „intelligenten Raketen“‑Präparat und in puncto Sicherheit teils günstiger. Größere, randomisierte Studien sind weiterhin nötig, doch die bisherigen Daten deuten darauf hin, dass SHR‑A1811 eine wichtige neue Option für schwer behandelbare, HER2‑getriebene Krebserkrankungen werden könnte.
Zitation: Yao, H., Yan, M., Tong, Z. et al. SHR-A1811, a novel HER2-targeting antibody-drug conjugate, in advanced solid tumors (HORIZON-X): a global phase 1 trial. Sig Transduct Target Ther 11, 104 (2026). https://doi.org/10.1038/s41392-026-02612-9
Schlüsselwörter: HER2‑zielgerichtete Therapie, Antikörper‑Wirkstoff‑Konjugat, metastasiertes Mammakarzinom, solide Tumoren, klinische Studie