Clear Sky Science · de
M6A-modifizierte circArhgap26 mildert ischämisch‑reperfusionsbedingte Herzschädigung durch Unterdrückung der Palmitoylierung von Plakophilin‑1
Warum es wichtig ist, das Herz nach einem Herzinfarkt zu schützen
Wenn jemand einen Herzinfarkt hat, bemühen sich Ärztinnen und Ärzte, die verstopfte Arterie schnell wieder zu eröffnen und den Blutfluss wiederherzustellen. Dieser Rettungsschritt rettet Leben, hat aber auch eine Schattenseite: Das plötzliche Wiederkehren des Blutes kann das Herz zusätzlich schädigen, ein Problem, das als Ischämie‑Reperfusions‑Schädigung bekannt ist. Die hier zusammengefasste Studie untersucht einen unerwarteten natürlichen Schutzmechanismus in Herzmuskelzellen — ein zirkuläres RNA‑Molekül namens circArhgap26 — das hilft, den Herzmuskel vor dieser sekundären Schädigungswelle zu schützen. Zu verstehen, wie dieses winzige Molekül funktioniert, könnte Wege zu neuen Therapien und Bluttests für Menschen mit Herzerkrankungen eröffnen.
Ein verborgener Kreis im genetischen Text des Herzens
Die meisten von uns denken an Gene als gerade Stränge von DNA und RNA, aber Zellen produzieren auch ringförmige RNA‑Moleküle, sogenannte zirkuläre RNAs, die ungewöhnlich stabil sind und viele zelluläre Prozesse fein regulieren können. Die Forschenden durchsuchten Mäuseherzen nach zirkulären RNAs, die sich während einer Herzverletzung verändern, und konzentrierten sich auf eine, circArhgap26, deren Spiegel stark abfielen, wenn der Blutfluss unterbrochen und dann wiederhergestellt wurde. Sie bestätigten, dass diese zirkuläre RNA eine geschlossene Schleife bildet, hauptsächlich im zellulären Zytoplasma vorkommt und nicht als Vorlage zur Proteinproduktion dient. Stattdessen scheint sie als Regulator zu wirken, indem sie mit anderen Molekülen interagiert und beeinflusst, ob eine Herzmuskelzelle nach Stress überlebt oder stirbt. 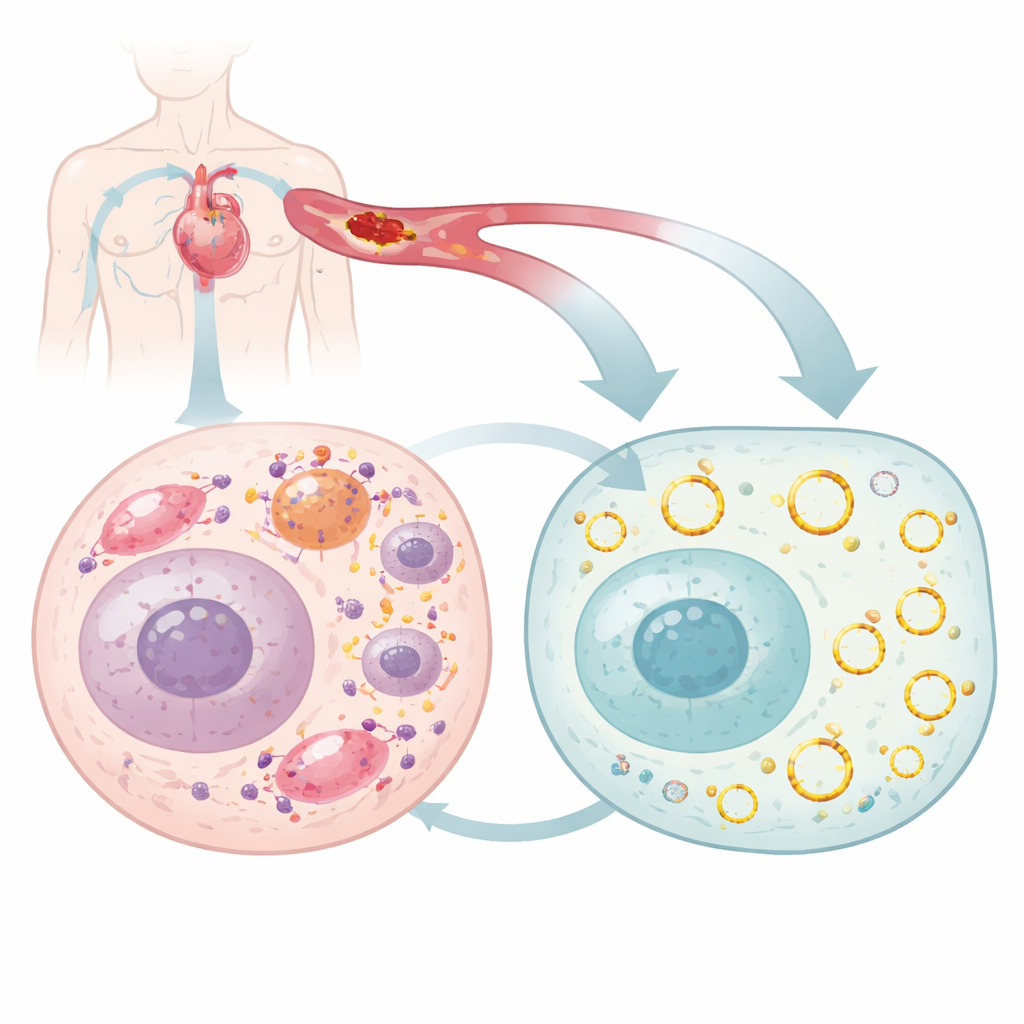
Belege dafür, dass die zirkuläre RNA das Herz schützt
Um zu untersuchen, was circArhgap26 tatsächlich bewirkt, erhöhten oder verringerten die Forschenden seine Konzentration in Mäuseherzen. Als sie ein Virus verwendeten, um circArhgap26 spezifisch in Herzmuskelzellen zu steigern, zeigten die Tiere, die einer vorübergehenden Blockade einer Koronararterie mit anschließender Wiederherstellung des Blutflusses unterzogen wurden, eine stärkere Pumpfunktion, kleinere geschädigte Bereiche und weniger sterbende Zellen. Klassische Marker für Verletzung im Blut und im Herzgewebe waren ebenfalls niedriger. Das Gegenteil zeigte sich, wenn die zirkuläre RNA stillgelegt wurde: Selbst ohne einen induzierten Herzinfarkt verschlechterte sich die Herzfunktion und die Zelltodrate stieg an; diese Probleme verschlimmerten sich, wenn Ischämie‑Reperfusion hinzukam. Ähnliche schützende Effekte traten in menschlichen herzähnlichen Zellen im Labor auf, was darauf hindeutet, dass der Mechanismus zwischen Maus und Mensch erhalten ist.
Ein schädlicher Partnerprotein bleibt in Schach
Bei tiefergehenden Untersuchungen fragten die Forschenden, wie circArhgap26 diesen Schutz vermittelt. Mit biochemischen Fangmethoden fanden sie, dass es direkt an ein Strukturprotein namens Plakophilin‑1 (PKP1) bindet, das beeinflussen kann, wie stark Zellen zusammenhalten und wie leicht sie programmierten Zelltod durchlaufen. In verletzten Herzen und gestressten Herzzellen stiegen die PKP1‑Spiegel und korrelierten mit stärkerer Schädigung. Das Stilllegen von PKP1 milderte Herzverletzung und Zelltod, während seine Überexpression die Schäden verschlimmerte. Als circArhgap26 erhöht wurde, sank die Menge an PKP1‑Protein, obwohl die Genaktivität unverändert blieb, was auf eine Regulation nach der RNA‑Phase hindeutet. Experimente zeigten, dass circArhgap26 den Abbau des PKP1‑Proteins beschleunigt, indem es einen Fettsäure‑Modifikationsprozess namens Palmitoylierung stört, der PKP1 normalerweise stabilisiert.
Ein molekulares Tauziehen um Todes‑Signale der Zelle
Die Palmitoylierung wird von einer Familiengruppe von Enzymen ausgeführt; eines davon, ZDHHC1, wurde gefunden, Fettsäuregruppen an PKP1 anzuhängen und es dadurch langlebiger zu machen. CircArhgap26 bindet an PKP1 in derselben Region, die auch von ZDHHC1 genutzt wird, und erzeugt so ein molekulares Tauziehen. Wenn die zirkuläre RNA gewinnt, erhält PKP1 weniger Fetttags, wird weniger stabil und schneller abgebaut. Das hat eine Folge: PKP1 fördert normalerweise die Produktion eines anderen Proteins, APAF1, indem es mit einem Kontrollabschnitt seiner RNA interagiert. APAF1 ist ein zentraler Bestandteil der Maschinerie, die die Aktivierung der Enzyme Caspase‑9 und Caspase‑3 auslöst, die als Ausführungswerkzeuge des programmierten Zelltods fungieren. Mit weniger stabilem PKP1 fällt die APAF1‑Proteinproduktion, die Todes‑Signal‑Kaskade wird abgeschwächt, und Herzzellen überleben die Belastung durch wiederhergestellten Blutfluss eher. 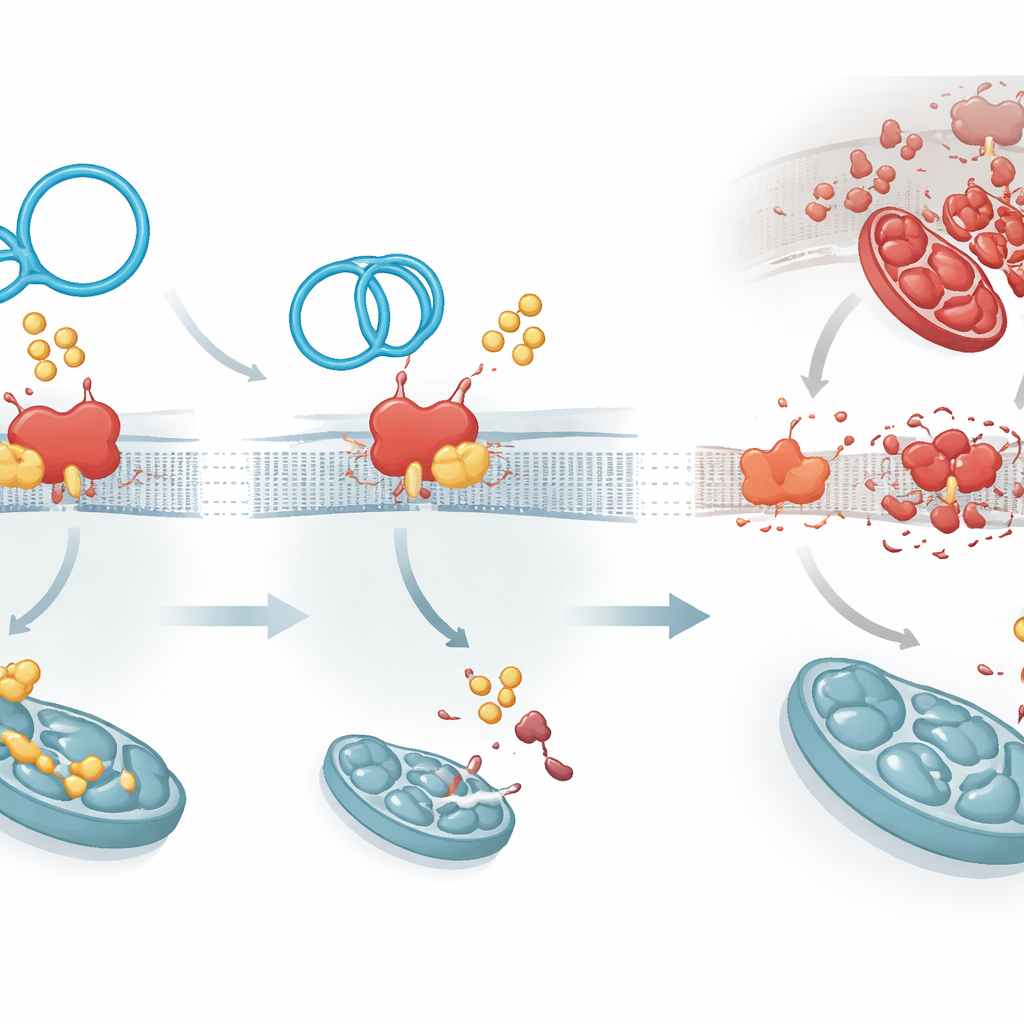
Feinabstimmung des Kreises und seine Perspektive für Patienten
Die Studie zeigt außerdem, wie circArhgap26 selbst während einer Schädigung heruntergeregelt wird. Eine häufige chemische Markierung auf RNA, genannt m6A, sammelt sich auf dieser zirkulären RNA in gestressten Herzen an. Ein Leserprotein namens YTHDF2 erkennt diese Markierung und fördert den Abbau von circArhgap26, wodurch der natürliche Schutz des Herzens gerade dann geschwächt wird, wenn er am dringendsten gebraucht wird. Wichtig ist, dass die menschliche Version dieser zirkulären RNA der Mausversion sehr ähnlich ist und im Blut von Patientinnen und Patienten, die sich einer arteriellen Wiedereröffnungsprozedur unterziehen, deutlich niedriger ist als bei gesunden Freiwilligen. Zusammen deuten diese Befunde darauf hin, dass die Wiederherstellung oder das Nachahmen von circArhgap26 sowohl als blutbasierter Risikomarker als auch als neuartige Therapie dienen könnte. In einfachen Worten enthüllt die Arbeit ein kleines zirkuläres Molekül, das als Wächter gegen Reperfusionsschäden wirkt, indem es eine tödliche Kettenreaktion in Herzzellen entschärft.
Zitation: Zhang, My., Ji, Dn., Qi, Wy. et al. M6A-modified circArhgap26 attenuates cardiac ischemia‒reperfusion injury by suppressing plakophilin-1 palmitoylation. Sig Transduct Target Ther 11, 99 (2026). https://doi.org/10.1038/s41392-026-02609-4
Schlüsselwörter: Ischämie‑Reperfusions‑Schädigung, zirkuläre RNA, Herzinfarkt, Kardiomyozyten‑Apoptose, RNA‑basierte Therapie