Clear Sky Science · de
Chemo-photothermische Synergie entfacht antitumorale Immunität über Ferroptose
Den Körperwärme und Licht in einen Krebsbekämpfer verwandeln
Chemotherapeutika können Tumoren verkleinern, gehen aber oft mit starken Nebenwirkungen einher und verhindern nicht zuverlässig ein Wiederauftreten des Krebses. Diese Studie untersucht einen neuen Weg, ein etabliertes Medikament, Docetaxel, wirksamer und gezielter zu machen, indem man es in winzige, hitzereagierende Partikel packt und mit nahinfrarotem Licht aktiviert. Ziel ist es nicht nur, Tumorzellen präziser zu töten, sondern auch das Immunsystem zu wecken, damit es den Krebs im ganzen Körper erkennt und verfolgt und zukünftige Rückfälle verhindert. 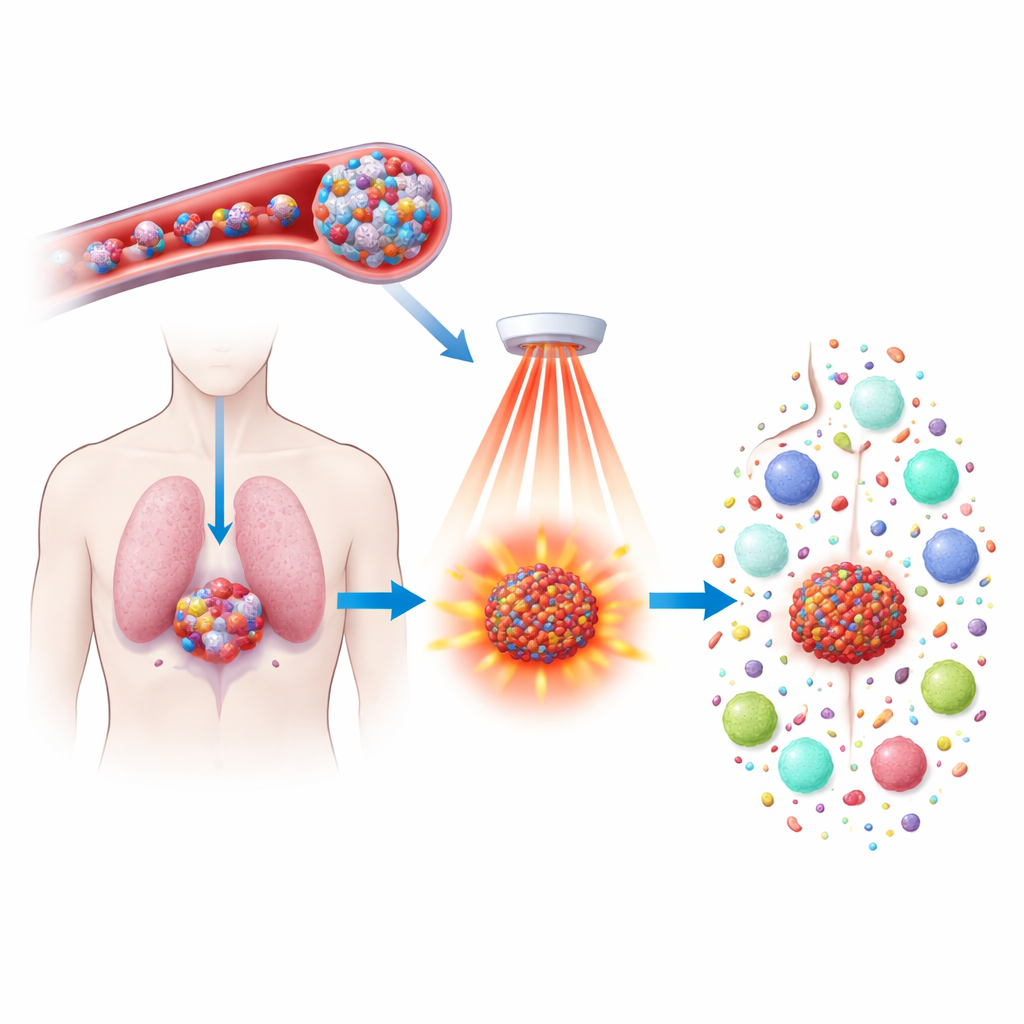
Kleine Kuriere, die wissen, wohin sie müssen
Die Forschenden entwickelten einen neuen Nanopartikeltyp aus einem Polymer, das Ferrocene enthält – ein eisenhaltiges Molekül, das stark mit Wasserstoffperoxid reagiert, einem Oxidans, das in Tumoren in höherer Konzentration vorkommt als in gesundem Gewebe. Diese Polymere setzen sich selbstständig zu wasserfreundlichen Kugeln zusammen, die sowohl Docetaxel als auch einen lichtabsorbierenden Farbstoff namens IR808 transportieren können. Einmal in den Blutkreislauf injiziert, sind die Partikel klein und stabil genug, um zu zirkulieren und in Tumoren zu gelangen; dort schwächen die undichten Blutgefäße und die hohen Wasserstoffperoxid‑Werte die Partikel und bewirken eine langsame Freisetzung ihres Wirkstoffs. Dieses Design konzentriert die Behandlung in den Tumoren und begrenzt gleichzeitig Schäden an gesunden Organen.
Licht nutzen, um lokale Schäden zu verstärken
Nahinfrarotes Licht, das Gewebe sicher durchdringen kann, wird auf die Tumorregion gerichtet. Das im Nanopartikel enthaltene IR808 absorbiert dieses Licht und wandelt es in Wärme um, während es zudem chemisch reaktive Sauerstoffspezies erzeugt. Die Kombination aus tumorproduziertem Wasserstoffperoxid und lichtgetriebenen Oxidantien lässt die Partikel schneller zerfallen und setzt die Arzneiladung genau dort frei, wo sie gebraucht wird. Gleichzeitig hilft das Eisen im Ferrocene‑Baustein, diese Oxidantien in besonders aggressive Formen umzuwandeln, die die fettigen Bestandteile von Zellmembranen angreifen. Dieser gezielte chemische und thermische Angriff erhöht die Abtötungswirkung deutlich im Vergleich zu Docetaxel oder Lichtbehandlung allein. 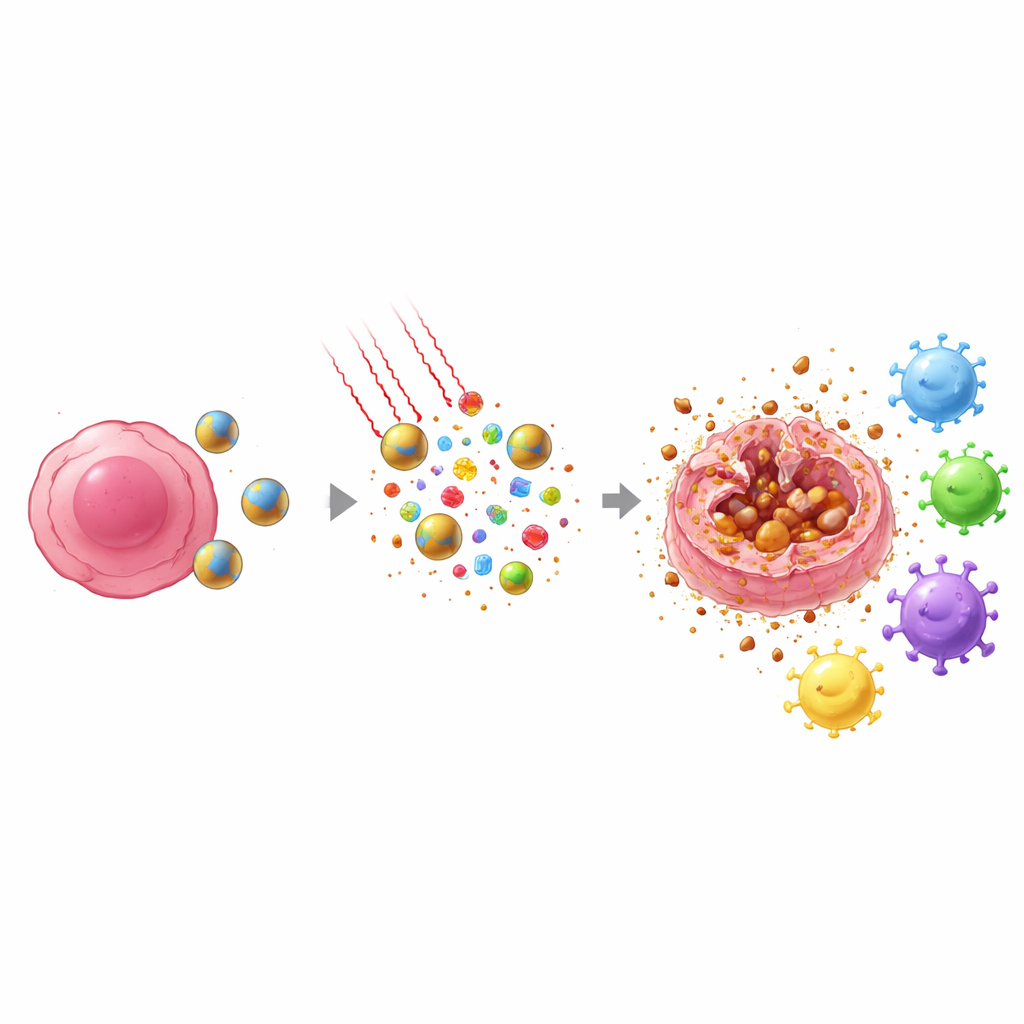
Ein kontrolliertes Brennen, das das Immunsystem alarmiert
Wichtig ist, dass die Art und Weise, wie Tumorzellen unter dieser Behandlung sterben, sich von gewöhnlicher Chemotherapie unterscheidet. Statt leise in geordnete Bruchstücke zu zerfallen, durchlaufen viele Zellen einen Prozess namens Ferroptose, eine Form des eisenvermittelten, membrane‑schädigenden Todes, bei dem die Außenmembran einreißt. Dabei geben die Zellen interne Alarmsignale und tumorspezifische Fragmente in ihre Umgebung ab. Gleichzeitig drängt Docetaxel ein wichtiges Kernprotein, HMGB1, an den Zellrand und bereitet dessen Freisetzung vor. Zusammengenommen erzeugen Hitze, Oxidantien und die Wirkung des Wirkstoffs eine Welle von Gefahren‑ und Antigensignalen, die benachbarte Immunwächter—dendritische Zellen—erkennen und zu den Lymphknoten transportieren können.
Vom lokalen Angriff zur Abwehr im ganzen Körper
In Maus‑Tumormodellen verkleinerte diese kombinierte chemo‑photothermische Behandlung nicht nur die direkt erhitzten Tumoren wirksamer als jede Einzelkomponente, sie veränderte auch die Immunlandschaft. In den Tumoren fanden sich mehr ausgereifte dendritische Zellen und größere Zahlen cytotoxischer T‑Zellen, sowohl im Tumor selbst als auch in den abführenden Lymphknoten. In einigen immunkompetenten Mäusen verschwanden die Primärtumoren bereits nach nur zwei Behandlungszyklen. Als die Forschenden später neue Tumore an entfernten Stellen oder in der gegenüberliegenden Flanke einpflanzten, wuchsen diese sekundären Herde langsamer oder wurden unterdrückt, was darauf hindeutet, dass die Tiere eine Form tumor‑spezifischen immunologischen Gedächtnisses entwickelt hatten. Die Zugabe eines checkpointblockierenden Antikörpers, der die Erschöpfung von T‑Zellen verhindert, verringerte Lungenmetastasen weiter und verlängerte das Überleben, was darauf hindeutet, dass diese lokale Behandlung mit modernen Immuntherapien kombinierbar ist.
Warum das für die zukünftige Krebsversorgung wichtig ist
Für Nichtfachleute ist die wichtigste Botschaft, dass dieser Ansatz Docetaxel von einem unspezifischen systemischen Gift zu einem Teil einer intelligenten, mehrstufigen Anti‑Krebs‑Strategie macht. Durch das Verpacken des Medikaments in lichtaktivierbare, eisenhaltige Nanopartikel, die auf die Chemie des Tumors reagieren, liefert die Therapie mehr Schaden innerhalb der Tumoren und schont gesundes Gewebe. Das spezielle Muster des ausgelösten Zelltods wirkt wie eine Impfung aus dem Tumor heraus und lehrt das Immunsystem, den Krebs zu erkennen und zu speichern. Wenn sich diese Ergebnisse auf den Menschen übertragen lassen, könnten solche chemo‑photothermischen Systeme resistente „kalte“ Tumoren in „heiße“ verwandeln, die deutlich besser auf immunbasierte Therapien ansprechen — was Rückfälle reduzieren und die langfristige Kontrolle verbessern könnte.
Zitation: Lin, J., Yang, H., Zou, Z. et al. Chemo-photothermal synergy ignites antitumor immunity via ferroptosis. Sig Transduct Target Ther 11, 98 (2026). https://doi.org/10.1038/s41392-026-02608-5
Schlüsselwörter: Krebsnanomedizin, photothermische Therapie, Ferroptose, Krebsimmuntherapie, Docetaxel‑Freisetzung