Clear Sky Science · de
DUSP6-Entfernung stellt die Fitness von CAR-T-Zellen wieder her, die durch den Verlust von Tumor‑CD58 beeinträchtigt sind, indem sie AP‑1‑Signalgebung belebt
Warum die Aufrüstung krebsbekämpfender Zellen wichtig ist
Genetisch veränderte Immunzellen, sogenannte CAR‑T‑Zellen, haben die Behandlung bestimmter Blutkrebserkrankungen revolutioniert, dennoch fallen viele Patienten zurück, weil ihre Tumoren Wege finden, Angriffen zu entgehen. Diese Studie enthüllt eine verborgene Schwachstelle mancher Tumoren, die CAR‑T‑Zellen still und heimlich von innen deaktiviert — und zeigt, wie eine präzise genetische Anpassung die Ausdauer, Energieversorgung und Wirksamkeit dieser Zellen wiederherstellen kann. Für Leser ist das ein Einblick, wie die nächste Generation zellbasierter Therapien beständiger und wirksamer für mehr Menschen werden könnte.
Ein fehlender Griff an den Tumorzellen
CAR‑T‑Zellen brauchen einen festen „Handschlag“ mit ihrem Ziel, um gut zu funktionieren. Viele Tumorzellen zeigen ein Oberflächenmolekül namens CD58, das als „Griff“ für Immunzellen dient und ihnen hilft, sich festzuhalten und eine enge Kontaktzone zu bilden. Frühere Arbeiten zeigten, dass CAR‑T‑Zellen Schwierigkeiten haben, diesen Kontakt zu formen, wenn Tumoren CD58 verlieren, und dadurch weniger effektiv werden. In dieser Studie stellten die Forschenden eine tiefergehende Frage: Über dieses mechanische Kontaktproblem hinaus — wie verändert der Verlust von CD58 die innere Biologie der CAR‑T‑Zellen, sodass ihre Leistungsfähigkeit über die Zeit gemindert wird?
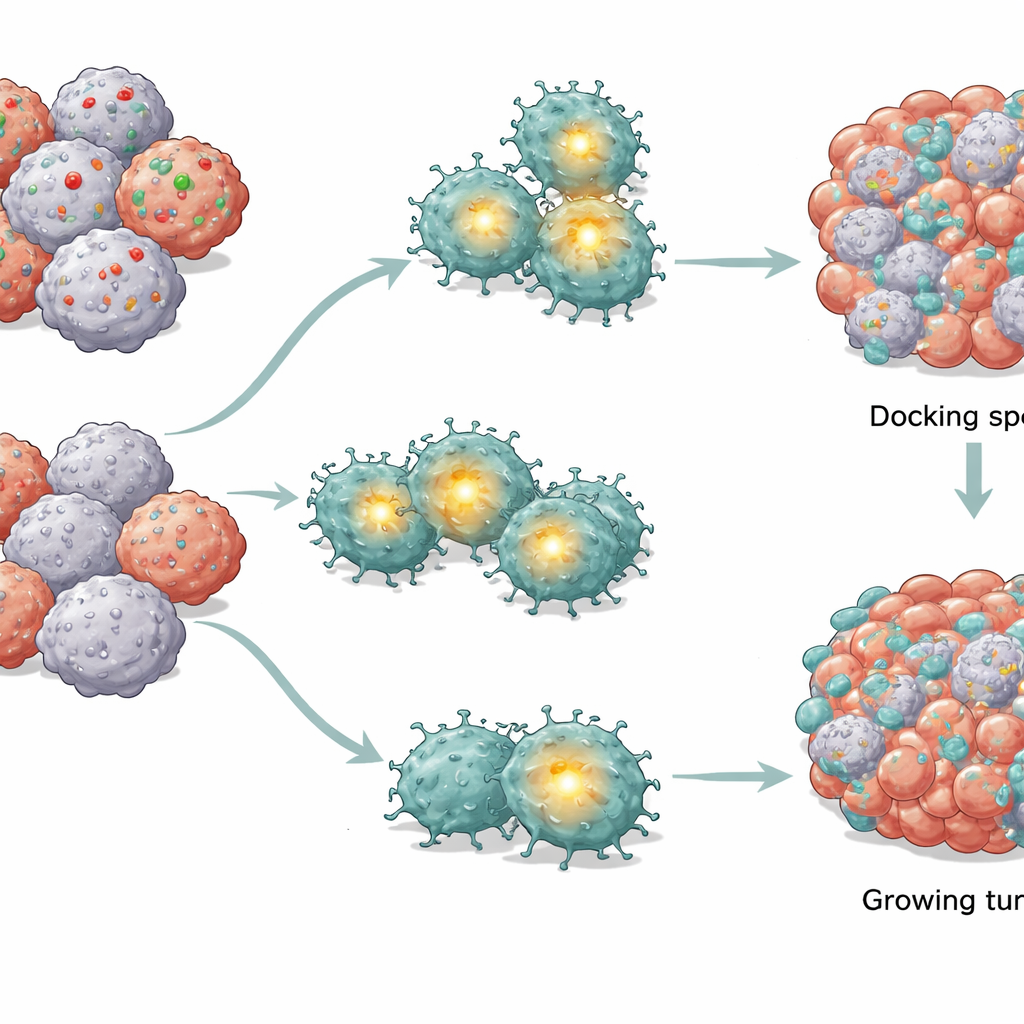
Kurzgeschlossene Signalwege in CAR‑T‑Zellen
Durch den Vergleich von CAR‑T‑Zellen, die normalen Tumoren ausgesetzt waren, mit solchen, die CD58‑defizienten Tumoren gegenüberstanden, fand das Team heraus, dass eine zentrale Steuerstelle in den T‑Zellen — genannt AP‑1 — selektiv geschwächt war, während andere wichtige Signalwege weitgehend intakt blieben. AP‑1 ist eine Gruppe von Proteinen, die Gene aktivieren, die an Aktivierung und Überleben beteiligt sind. Wenn die AP‑1‑Aktivität nachließ, zeigten CAR‑T‑Zellen typische Anzeichen einer internen Energiekrise: weniger und kleinere Mitochondrien (ihre Kraftwerke), verringerte Fähigkeit, Sauerstoff zu verbrauchen und Zucker zu nutzen, sowie ein Verlust der elektrischen Ladung über den Mitochondrienmembranen. Gleichzeitig häuften sich schädliche reaktive Sauerstoffmoleküle. Zusammengenommen trieben diese Veränderungen CAR‑T‑Zellen in ein Selbstzerstörungsprogramm, das auf Schäden in den eigenen Mitochondrien beruht — und das ohne externe Todesreize.
Eine innere Bremse ausschalten
Um zu verstehen, warum AP‑1 so gedämpft war, suchten die Forschenden stromaufwärts nach molekularen „Bremsen“, die überaktiv sein könnten. Sie fanden, dass CAR‑T‑Zellen, die mit CD58‑negativen Tumoren konfrontiert waren, mehrere Phosphatasen hochfuhren — Enzyme, die Signalwege abschalten — insbesondere eine namens DUSP6. Mit Medikamenten und anschließender präziser Genbearbeitung, um diese Enzyme zu blockieren, entdeckten sie, dass die Entfernung von DUSP6 die AP‑1‑Aktivität am stärksten wiederbelebte. DUSP6‑bearbeitete CAR‑T‑Zellen vermehrten sich besser, bildeten mehr Mitochondrien, verbrannten Energie effizienter, produzierten mehr krebszerstörende Moleküle und waren weniger anfällig für Apoptose, vor allem bei wiederholter Konfrontation mit CD58‑defizienten Tumorzellen.
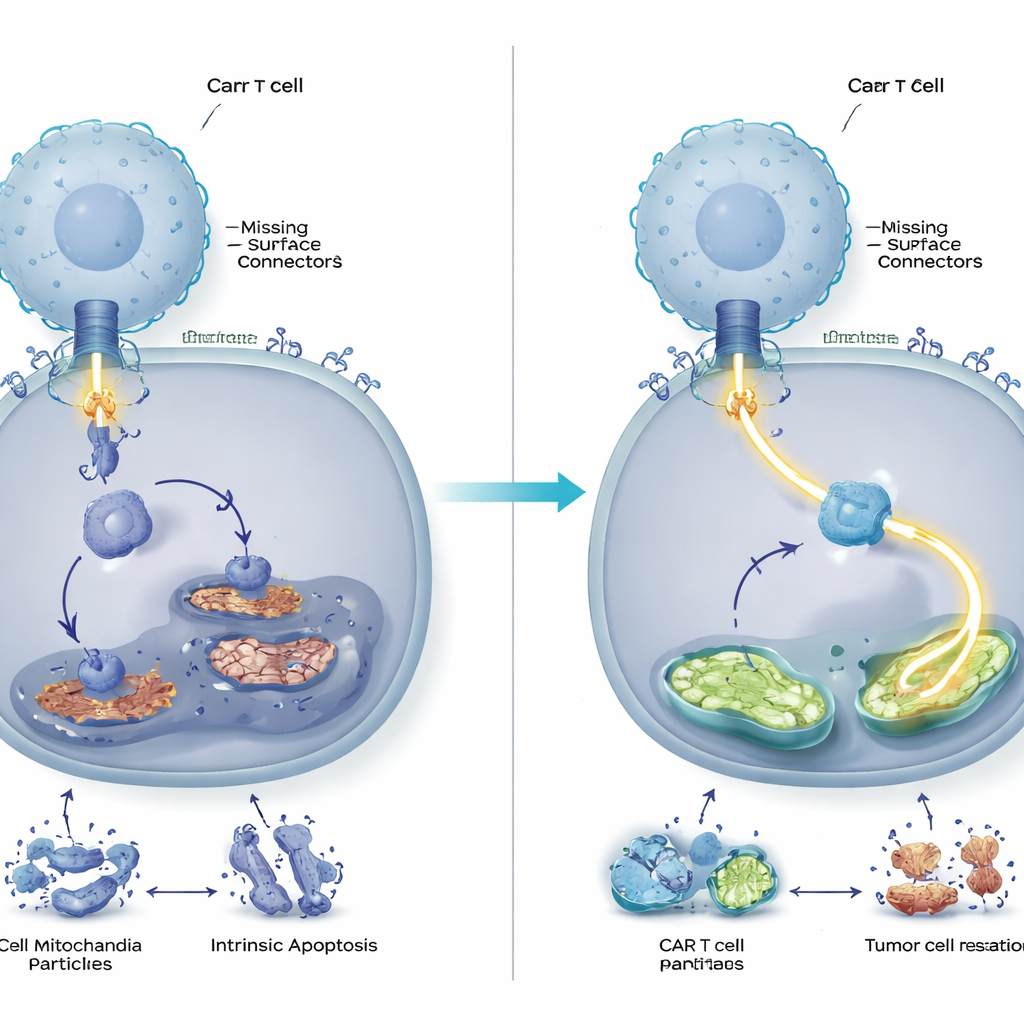
Stärkerer, länger anhaltender Tumorkontrolle im Tiermodell
Das Team prüfte anschließend, ob diese molekulare Feinabstimmung in lebenden Systemen von Bedeutung ist. In Mäusen mit menschlichen Blutkrebszellen, die entweder CD58 hatten oder nicht, beseitigten DUSP6‑defiziente CAR‑T‑Zellen Tumoren effektiver und hielten sie länger in Schach als konventionelle CAR‑T‑Zellen. Die veränderten Zellen vermehrten sich robuster, zeigten weniger Erschöpfungsmarker und sezernierten höhere Mengen wichtiger immunologischer Botenstoffe. Bemerkenswerterweise zeigten sich die Vorteile der DUSP6‑Entfernung nicht nur bei Tumoren ohne CD58, sondern auch bei solchen mit CD58, was darauf hindeutet, dass diese Modifikation CAR‑T‑Therapien allgemein verbessern könnte, statt nur eine enge Lösung für einen seltenen Tumortyp zu sein.
Hinweise aus Patientendaten
Um die Relevanz beim Menschen zu prüfen, analysierten die Forschenden Genexpressionsdaten von Personen, die mit CAR‑T‑Zellen oder mit Checkpoint‑Inhibitoren behandelt wurden. Bei Patienten mit diffus großzelligem B‑Zell‑Lymphom, die eine dual zielende CAR‑T‑Therapie erhielten, standen niedrigere DUSP6‑Spiegel in CD8‑T‑Zellen vor oder kurz nach der Infusion mit höheren Komplette‑Ansprech‑Raten in Verbindung. In einer separaten Hautkrebs‑Kohorte, die mit Anti‑PD‑1‑Antikörpern behandelt wurde, exprimierten erschöpfte CD8‑T‑Zellen von Nichtansprechern tendenziell mehr DUSP6 als diejenigen von Ansprechern. Zusammengenommen deuten diese Beobachtungen darauf hin, dass DUSP6 als negativer Marker für die Fitness von T‑Zellen in verschiedenen Immuntherapien wirkt und dass seine Herunterregulierung die Ergebnisse verbessern könnte.
Was das für künftige Krebstherapien bedeutet
Für eine allgemein verständliche Leserschaft lautet die Botschaft: Manche Tumoren entkommen dem Angriff von CAR‑T‑Zellen nicht nur durch Verstecken vor der Erkennung, sondern indem sie die internen Motoren der Zellen sabotieren. Der Verlust des CD58‑„Griffs“ an Tumorzellen senkt stillschweigend die AP‑1‑Signalgebung in CAR‑T‑Zellen, entleert ihre Mitochondrien, erhöht toxische Nebenprodukte und schubst sie in Richtung frühen Zelltod. Durch das Entfernen der DUSP6‑Bremse können Forschende dieses verlorene Signal wiederherstellen, die mitochondriale Gesundheit reparieren und CAR‑T‑Zellen größere Ausdauer und tödliche Kraft verleihen — selbst gegen resistente Tumoren. Obwohl weitere Sicherheits‑ und klinische Prüfungen nötig sind, erweist sich die DUSP6‑Ablation als vielversprechende ingenieurbiologische Strategie, um lebende Krebsmedikamente wirkungsvoller, langlebiger und potenziell für eine breitere Patientengruppe anwendbar zu machen.
Zitation: Ma, X., Zhang, Y., Wang, Y. et al. DUSP6 ablation restores CAR T-cell fitness impaired by tumor CD58 loss through invigoration of AP-1 signaling. Sig Transduct Target Ther 11, 100 (2026). https://doi.org/10.1038/s41392-026-02597-5
Schlüsselwörter: CAR-T-Zellen, CD58, DUSP6, Krebsimmuntherapie, T-Zell-Stoffwechsel