Clear Sky Science · de
Das Potenzial bimetallischer Nanobomben-aktivierter STING-Signalwege zur Verbesserung bispezifischer T‑Zell‑Engager für die Fotoimmuntherapie von Darmkrebs freisetzen
Das Immunsystem gegen Darmkrebs zurückgewinnen
Darm‑ und Rektumkarzinome sind häufig und oft tödlich, teilweise weil Tumoren lernen, sich dem Immunsystem zu entziehen. Diese Studie untersucht eine neue Strategie, die mehrere krebsbekämpfende Mechanismen in einer winzigen „Nanobombe“ vereint, um die Abwehrkräfte des Körpers zu wecken, Immunzellen den Tumor finden zu lassen und ein Wiederauftreten oder Streuen des Krebses zu verhindern.
Warum heutige Immunmedikamente ein Upgrade brauchen
Eine vielversprechende Medikamentenklasse, die sogenannten bispezifischen T‑Zell‑Engager, funktioniert wie biologische Kuppler: Ein Ende greift eine T‑Zelle (einen wichtigen Immunkämpfer), das andere heftet sich an ein Merkmal auf einer Tumorzelle, sodass beide zusammengebracht werden und die T‑Zelle töten kann. Während sie bei Blutkrebserkrankungen wirksam sind, tun sie sich bei soliden Tumoren wie Darmkrebs schwer. Sie werden schnell aus dem Körper entfernt, können gesunde Gewebe angreifen, die dasselbe Merkmal teilen, und stoßen oft auf „kalte“ Tumoren, denen es an ausreichenden Immunzellen fehlt, damit die Therapie funktioniert. Ärzte und Wissenschaftler suchen daher nach Wegen, diese Wirkstoffe sicherer zu liefern und kalte Tumoren in „heiße“ umzuwandeln, die von aktivierten Immunzellen durchdrungen sind.
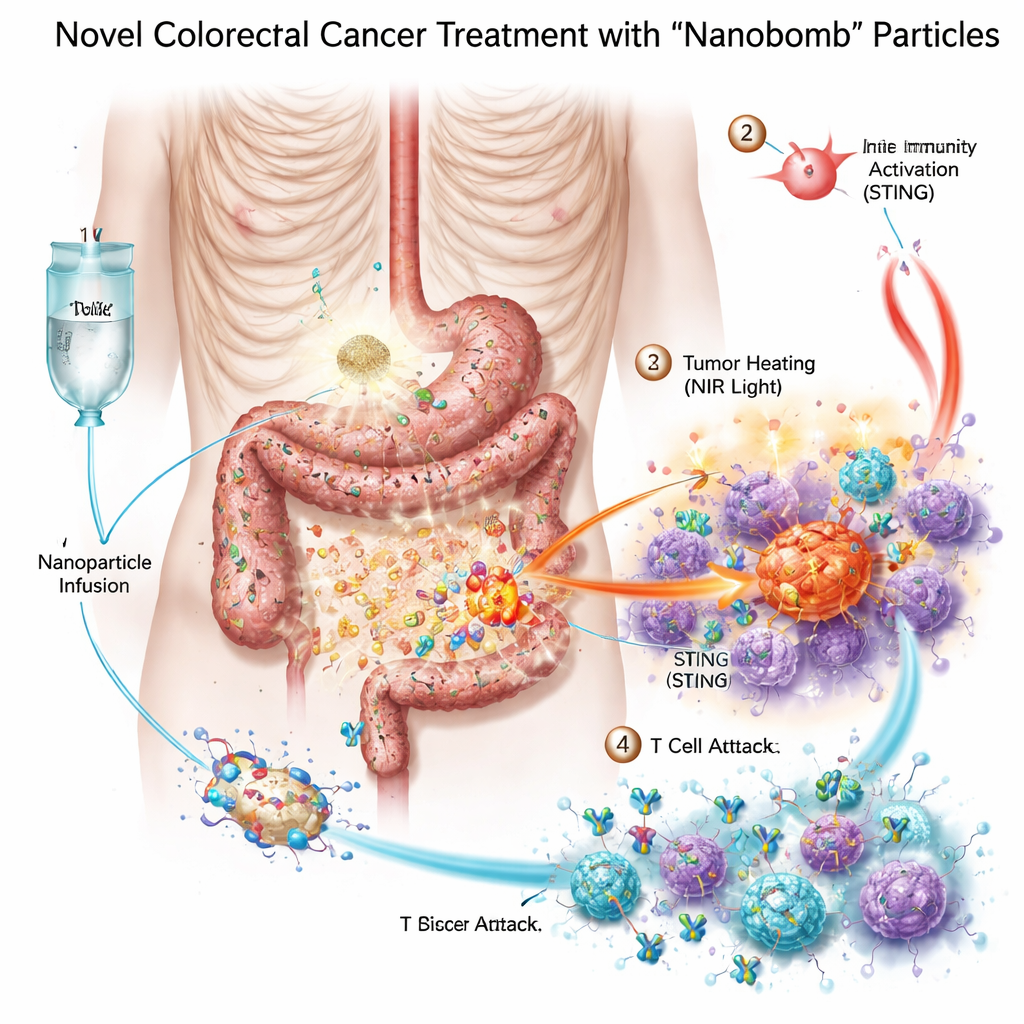
Drei Waffen in einer winzigen „Nanobombe“ bündeln
Die Forscher entwarfen eine bimetallische Nanobombe — wissenschaftlich MnO2/Co‑DA@BiTE/HPT genannt — die drei Behandlungsmodi in einem Partikel kombiniert. Erstens enthält der Kern Mangan und Kobalt, Metalle, die ein zelluläres Alarmsystem namens STING aktivieren können, das dem Körper hilft, Gefahr zu erkennen und Immunzellen herbeizurufen. Zweitens ist die Oberfläche des Partikels mit einem bispezifischen T‑Zell‑Engager beschichtet, der T‑Zellen mit Krebszellen verbindet. Drittens absorbiert das Material nahinfrarotes Licht, sodass Ärzte den Tumor von außen mit einer Form der photothermischen Therapie erhitzen können. Damit die Nanobomben gezielt Darmkrebszellen ansteuern, fügten die Autoren ein kurzes DNA‑Stück, ein Aptamer, hinzu, das PD‑L1 erkennt — ein Molekül, das auf diesen Tumoren oft reichlich vorkommt. Erreichen die Partikel den Tumor, helfen natürliche Enzyme im Tumorgewebe, sie zu zerlegen und ihre Fracht genau dort freizusetzen, wo sie gebraucht wird.
Erhitzen, Alarmieren und die Immunarmee rekrutieren
In Zellkulturversuchen töteten die Nanobomben Darmkrebszellen effektiver als jede einzelne Komponente allein. Unter Nahinfrarotbestrahlung erwärmten sich die Partikel, setzten die Tumorzellen unter Stress und schädigten sie, und trugen zur Bildung reaktiver Sauerstoffspezies bei — hochreaktive Moleküle, die Tumorzellen zusätzlich verletzen. Dieser Stress beschädigte die DNA der Zellen und trieb sie in eine besonders signalstarke Form des Zelltods, die „Gefahr“-Signale aussendet. Nahegelegene Immunzellen, vor allem dendritische Zellen, nahmen das sterbende Tumormaterial auf und schalteten mit Hilfe des freigesetzten Mangans und Kobalts den STING‑Signalweg ein. Sie produzierten daraufhin Interferone und andere entzündungsfördernde Botenstoffe, die T‑Zellen reifen lassen und anlocken. Gleichzeitig verband der bispezifische Engager auf der Nanobombe T‑Zellen physisch mit PD‑L1‑positiven Tumorzellen, was die T‑Zell‑Aktivierung und Tumorzellabtötung auch in zuvor kalten Tumoren verbesserte.
Vom Tumorschwund zur dauerhaften Immunerinnerung
In mehreren Mausmodellen — darunter subkutane Darmtumoren, Tumoren an beiden Körperseiten, Lungenmetastasen und ein Modell für Rückfälle nach Operation — verlangsamten oder stoppten die Nanobomben plus Licht das Tumorwachstum deutlich. Behandelte Tumore enthielten deutlich mehr krebsabtötende CD8‑T‑Zellen und weniger regulatorische T‑Zellen, die normalerweise Immunantworten dämpfen. Dendritische Zellen im Tumor und in den Lymphknoten zeigten Reifungszeichen, und Bluttests zeigten erhöhte Spiegel immunstimulierender Zytokine. Wichtig ist, dass Mäuse, die nach Nanobombenbehandlung ihre Tumore beseitigten, beim erneuten Einbringen des Krebses besser geschützt waren und weniger Lungenmetastasen entwickelten — ein Hinweis darauf, dass die Therapie eine langfristige Immunerinnerung aufbaute und nicht nur einmaligen Tumorschwund verursachte.
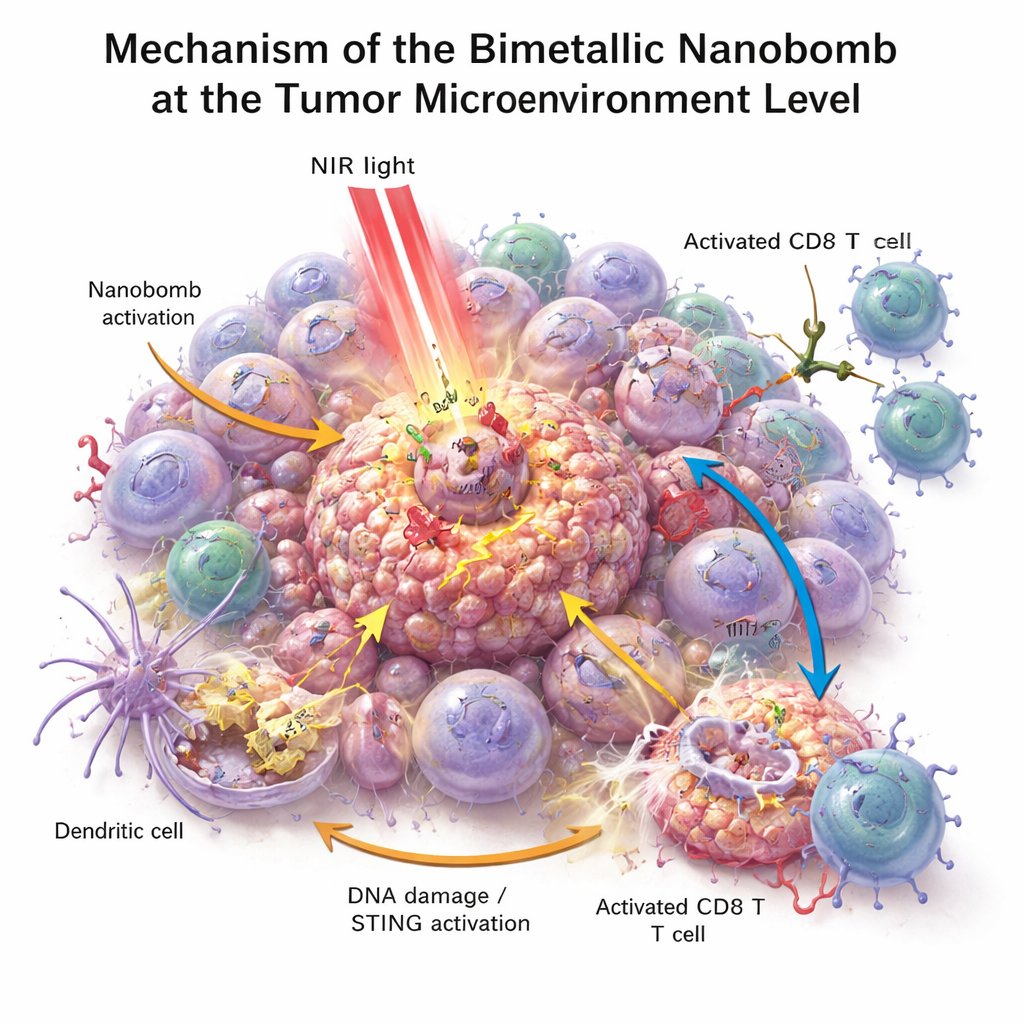
Was das für die künftige Krebsbehandlung bedeuten könnte
Diese Arbeit stellt eine „Dreifach‑Angriffs“-Nanomedizin vor, die Tumore erhitzt, einen internen Gefahrenalarm auslöst und T‑Zellen direkt zu Krebszellen führt — alles in einem einzelnen zielgerichteten Partikel. In Mäusen verwandelte dieser Ansatz kalte Darmtumoren in heiße, entzündete Tumoren und half zudem, Rezidive und Metastasen zu verhindern. Obwohl die Technologie noch weit von der klinischen Anwendung entfernt ist — Skalierung, Langzeitsicherheit und Tests am Menschen bleiben große Herausforderungen — liefert sie ein Konzept für künftige Behandlungen, die intelligente Materialien mit Immunwirkstoffen kombinieren, um Patienten eine stärkere und nachhaltig wirkende Anti‑Krebs‑Antwort zu bieten.
Zitation: Mu, M., Li, H., Chen, B. et al. Unleashing the potential of bimetallic nanobomb-mediated STING pathway to enhance bispecific T-cell engager against colorectal cancer photo-immunotherapy. Sig Transduct Target Ther 11, 80 (2026). https://doi.org/10.1038/s41392-026-02596-6
Schlüsselwörter: Darmkrebs, Immuntherapie, Nanopartikel, STING-Signalweg, bispezifischer T‑Zell‑Engager