Clear Sky Science · de
Personalisierte pharmakokinetisch–pharmakodynamisch gesteuerte Therapie über eine aus induzierten pluripotenten Stammzellen abgeleitete Multi-Organoid-Plattform bei NF1-mutiertem Brustkrebs
Warum diese Forschung für Patientinnen und Patienten wichtig ist
Viele Menschen mit Krebs erhalten Medikamente, die bei einigen Patienten gut wirken, bei anderen jedoch nicht, und die häufig starke Nebenwirkungen verursachen. Diese Studie beschreibt einen neuen Weg, Krebstherapien außerhalb des Körpers zu testen, indem im Labor gezüchtete Mini-Organe aus den eigenen Zellen einer Patientin genutzt werden. Die Arbeit konzentriert sich auf eine schwer zu behandelnde Form von Brustkrebs, die durch Veränderungen im Gen NF1 angetrieben wird, und zeigt, wie die Kombination einer genkorrigierenden Strategie mit einem zielgerichteten Medikament zu einer sichereren, wirksameren und wirklich personalisierten Therapie führen könnte.
Aufbau einer Mini-Version des Körpers der Patientin
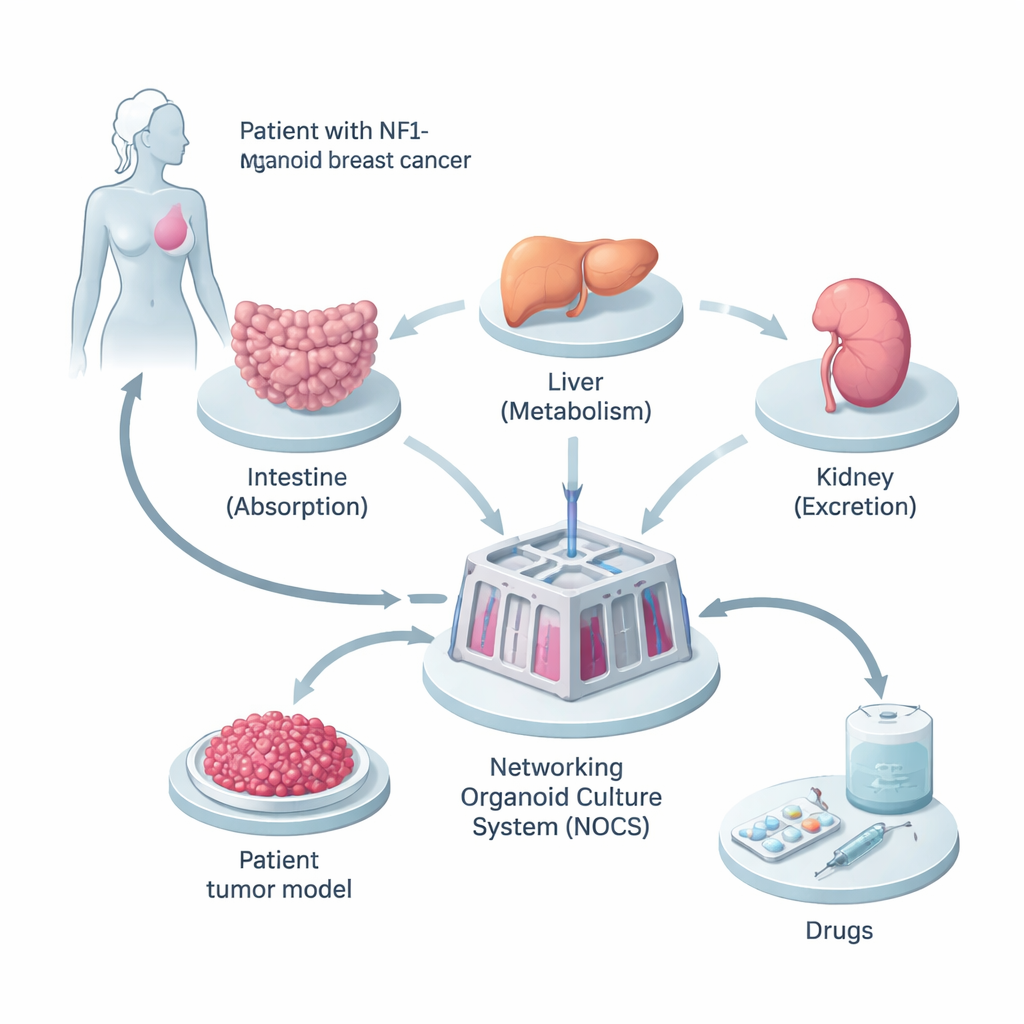
Die Forscherinnen und Forscher begannen mit Gewebe einer Frau, deren Brustkrebs eine vererbte Mutation im NF1-Gen trug. Sie reprogrammierten ihre normalen, hautähnlichen Zellen zu induzierten pluripotenten Stammzellen, die sich in fast jeden Zelltyp des Körpers verwandeln können. Aus diesen entstanden drei Arten miniaturisierter Organe – Dünndarm, Leber und Niere – weil dies die wichtigsten Orte sind, an denen Medikamente aufgenommen, verarbeitet und ausgeschieden werden. Parallel dazu erzeugten sie 3D-Tumor-„Sphäroide“ aus ihren Krebszellen und bewahrten dabei die Zusammensetzung der Zelltypen und die genetischen Veränderungen des ursprünglichen Tumors.
Ein lebender Wirkstoff-Testkreislauf
Damit sich diese Mini-Organe mehr wie ein echter Körper verhalten, verband das Team sie in einem flüssigkeitsgefüllten Gerät, dem Networking Organoid Culture System (NOCS). In diesem Aufbau fließt Medium zwischen den Kompartimenten für Darm, Leber, Niere und Tumor und ahmt damit die Blutzirkulation nach. Medikamente können so zugegeben werden, wie man eine Pille schluckt oder eine Injektion erhält, und Sensoren sowie Pumpen steuern Flussgeschwindigkeit und Erneuerung der „Blut“-Flüssigkeit. Das erlaubte den Wissenschaftlern zu verfolgen, wie viel Wirkstoff aufgenommen wird, wie schnell er abgebaut wird und wie stark er auf den Tumor wirkt – alles in einem patientenspezifischen, humanen Modell.
Ein defektes Gen mit Exon-Skipping reparieren
Der Tumor der Patientin trug eine schädigende NF1-Mutation, die Wachstumswege dauerhaft aktiviert und viele Standardmedikamente unwirksam macht. Das Team entwarf kurze genetische Bausteine, sogenannte Antisense-Oligonukleotide, um die RNA-Verarbeitungsmaschinerie der Zelle dazu zu bringen, das fehlerhafte Stück (Exon 2) des NF1-Gens zu überspringen. Mithilfe eines viralen Liefersystems, das über Tage aktiv bleibt, induzierten sie ein stabiles „Exon-Skipping“ in den Krebszellen der Patientin. Das erzeugte ein kürzeres, aber funktionales NF1-Protein, dämpfte die überaktiven Wachstumssignale und machte die Tumorzellen empfindlicher gegenüber Behandlungen.
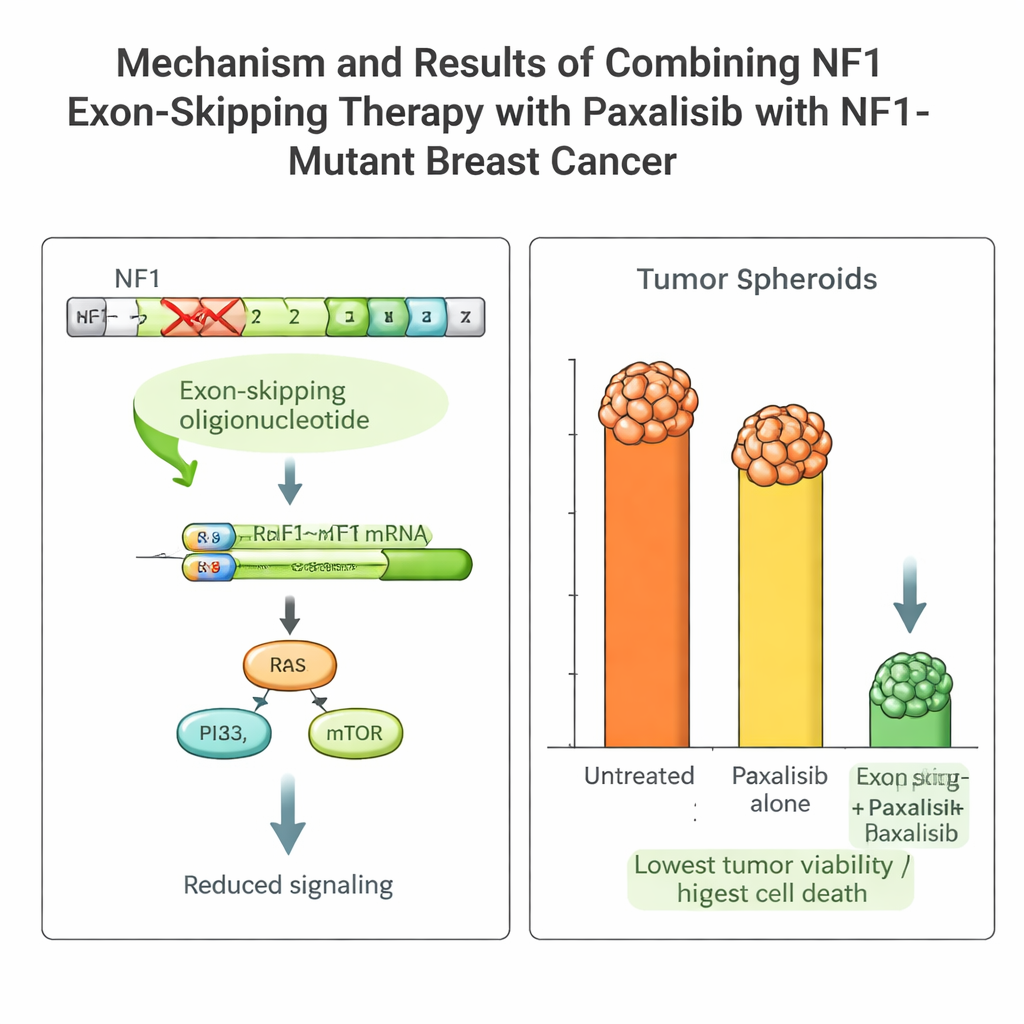
Die richtige zielgerichtete Therapie mit PK/PD-Leitlinien auswählen
Mit dieser Plattform verglich das Team mehrere fortgeschrittene Wirkstoffe, die den PI3K–mTOR-Signalweg blockieren, der dem NF1-Weg nachgelagert ist. Sie maßen Pharmakokinetik (wie der Körper das Medikament verarbeitet) und Pharmakodynamik (wie das Medikament auf den Tumor wirkt) sowohl in Mäusen als auch im NOCS. Ein Wirkstoff, Paxalisib, stach hervor: Er wurde im Darm gut aufgenommen, blieb systemisch in nützlichen Konzentrationen erhalten und zeigte ein ähnliches Verhalten in Tieren wie im Organoid-Gerät. In Kombination mit dem NF1-Exon-Skipping erhöhte Paxalisib die Tumorzellabtötung der Patientin dramatisch, mit starken Reduktionen des Wachstums und klaren Anzeichen programmierter Zellnekrose, sowohl im NOCS als auch in Mäusen, die den Tumor der Patientin trugen.
Nutzen und Risiko über Organe hinweg abwägen
Da Dünndarm-, Leber- und Nierenmodelle Teil desselben Kreislaufs waren, konnten die Forschenden auch frühe Hinweise auf Organschäden beobachten. Paxalisib rief Stressreaktionen und subtile Abschwächungen der Barrierefunktion in Darm- und Nierenmodellen sowie Anzeichen von Belastung in der Leber hervor, jedoch ohne größeren Verlust der Zellvitalität bei der getesteten Dosis. Diese Art der Ganzkörperbetrachtung mit humanem Gewebe bietet eine Möglichkeit, Behandlungsoptionen nicht nur danach zu vergleichen, wie gut sie Tumore verkleinern, sondern auch, wie sie gesunde Organe beeinflussen könnten, bevor ein Medikament je an eine Patientin oder einen Patienten verabreicht wird.
Was das für die zukünftige Krebsbehandlung bedeuten könnte
Einfach gesagt zeigt diese Studie, dass es inzwischen möglich ist, einen vereinfachten, patientenspezifischen „Mini-Körper auf einem Chip“ zu züchten, der testen kann, wie verschiedene Medikamente – und sogar genkorrigierende Ansätze – sich verhalten und miteinander interagieren. Für diese Patientin mit NF1-mutiertem Brustkrebs war die optimale Strategie eine Kombination aus NF1-Exon-Skipping-Therapie und dem oral einzunehmenden Wirkstoff Paxalisib, die zusammen das Tumorwachstum deutlich stärker verlangsamten als jede Einzeltherapie. Wenn solche Plattformen weiterentwickelt und an mehr Patientinnen und Patienten getestet werden, könnten sie Ärzte zu Therapieplänen führen, die auf die jeweilige Genetik und Biologie der Person zugeschnitten sind, und damit die Erfolgschancen verbessern und unnötige Toxizität verringern.
Zitation: Lim, J.H., Mun, S.J., Kang, H.M. et al. Personalized pharmacokinetic–pharmacodynamic guided therapy via an induced pluripotent stem cell–derived multi-organoid platform in NF1-mutant breast cancer. Sig Transduct Target Ther 11, 79 (2026). https://doi.org/10.1038/s41392-026-02595-7
Schlüsselwörter: personalisierte Onkologie, Brustkrebs, Organoide, NF1-Mutation, zielgerichtete Therapie