Clear Sky Science · de
Ausnutzung lipidgetriebener immunometabolischer Wege in Omentummetastasen zur Verbesserung der Immuntherapie bei Patientinnen mit Eierstockkrebs
Warum das Fett im Bauchraum für Eierstockkrebs wichtig ist
Eierstockkrebs breitet sich häufig auf eine fettige Gewebeschürze im Bauchraum aus, das sogenannte Omentum. Diese Region ist reich an Fettzellen und Immunzellen und erweist sich als weitaus mehr als nur ein passiver Zuschauer. Die hier zusammengefasste Studie zeigt, dass die Art und Weise, wie Immunzellen in diesen omentalen Ablagerungen Fette nutzen und verarbeiten, helfen kann zu erklären, warum nur ein kleiner Bruchteil der Patientinnen von modernen Immuntherapien profitiert. Sie deutet außerdem auf neue Wirkstoffkombinationen und bildgebungsbasierte Tests hin, die diese Behandlungen für mehr Menschen wirksam machen könnten.
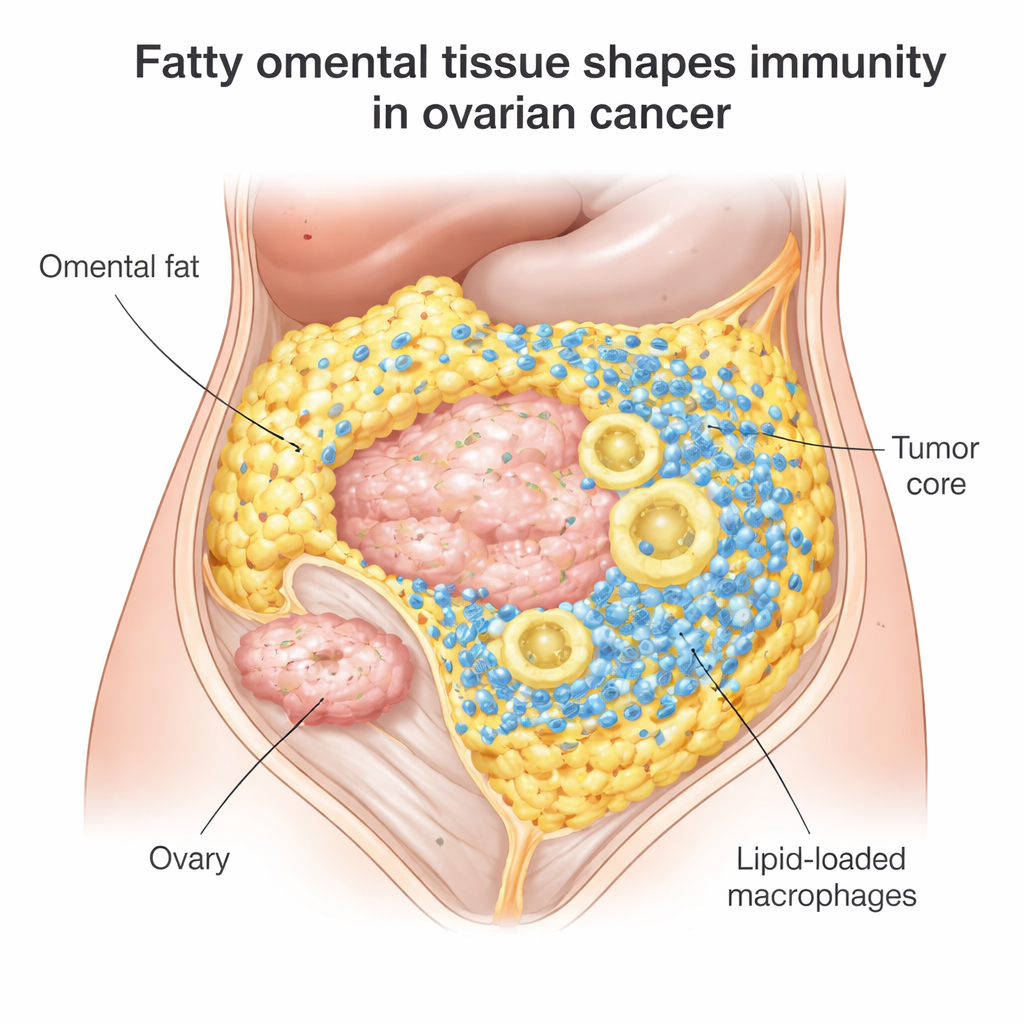
Ein verstecktes Schlachtfeld im Bauchfett
Die meisten Frauen mit epithelialem Eierstockkrebs sprechen zunächst auf Operation und Chemotherapie an, doch bei 70–80 % tritt die Erkrankung zurück, und Immun-Checkpoint-Medikamente wie Nivolumab oder Pembrolizumab helfen nur etwa 10–15 %. Die Forschenden konzentrierten sich auf omentale Metastasen, einen häufigen Ort, an dem sich Eierstocktumoren zwischen Fettzellen ansiedeln. Bei der Untersuchung von mehr als 100 Tumorproben stellten sie fest, dass omentale Tumoren voller Immunzellen waren: zytotoxische T‑Zellen, die Krebs angreifen können, und große Fresszellen, sogenannte Makrophagen. Es gab jedoch einen Haken. Diese T‑Zellen gruppierten sich eher am Rand, wo Tumor auf Fett trifft, statt in den Tumorkern vorzudringen, wo sie am dringendsten gebraucht würden.
Fett, das einige Immunzellen stärkt, andere aber überfordert
Bei genauerer Analyse zeigte das Team, dass T‑Zellen in diesen fettreichen Tumoren sich an die lokale Umgebung anpassen, indem sie Lipide, also Fette, aus benachbarten Fettzellen aufnehmen. Das scheint sie metabolisch „fit“ zu halten: Genexpressionsprofile und Laborbefunde zeigten, dass sie in der Lage waren, die Tumorzellen der Patientin zu erkennen und anzugreifen. Gleichzeitig waren viele tumorassoziierte Makrophagen im Omentum stark mit Fetttropfen beladen. Diese lipidüberladenen Makrophagen zeigten Anzeichen erhöhter oxidativer Belastung – chemischer Verschleiß, der mit reaktiven Sauerstoffspezies verbunden ist – und verlagerten sich in einen immunsuppressiven, tumorunterstützenden Zustand. Mit anderen Worten: Dasselbe fettreiche Milieu, das effektive T‑Zellen ernähren kann, drängt Makrophagen in einen schädlichen Modus, der den gesamten Immunangriff abschwächt.
Überfütterte Makrophagen mit zugelassenen Medikamenten umprogrammieren
Die Wissenschaftlerinnen und Wissenschaftler fragten dann, ob sie diese gestressten Makrophagen wieder zu Verbündeten machen könnten. An frischen Tumorfragmenten, die im Labor kultiviert wurden, testeten sie zwei Ansätze. Der eine verwendete Maraviroc, ein HIV‑Medikament, das CCR5 blockiert, einen Rezeptor für das Immunsignal CCL5, das an der Tumor‑Fett‑Grenze in hoher Konzentration vorkommt. Der andere blockierte CD36, einen wichtigen „Fress“-Rezeptor, der Makrophagen die Aufnahme fetter Säuren ermöglicht. Beide Behandlungen reduzierten die Fettlast in den Makrophagen, senkten Marker für oxidativen Stress und schädliche Lipidperoxidation und lösten Wellen entzündlicher Signale aus. Entscheidenderweise erlaubten sie zytotoxischen T‑Zellen, sich zu vermehren und vom fettreichen Rand in den Tumorkern vorzudringen, wodurch die lokale Immunaktivität gesteigert wurde, ohne zusätzliche Immunzellen von außen zuzuführen.
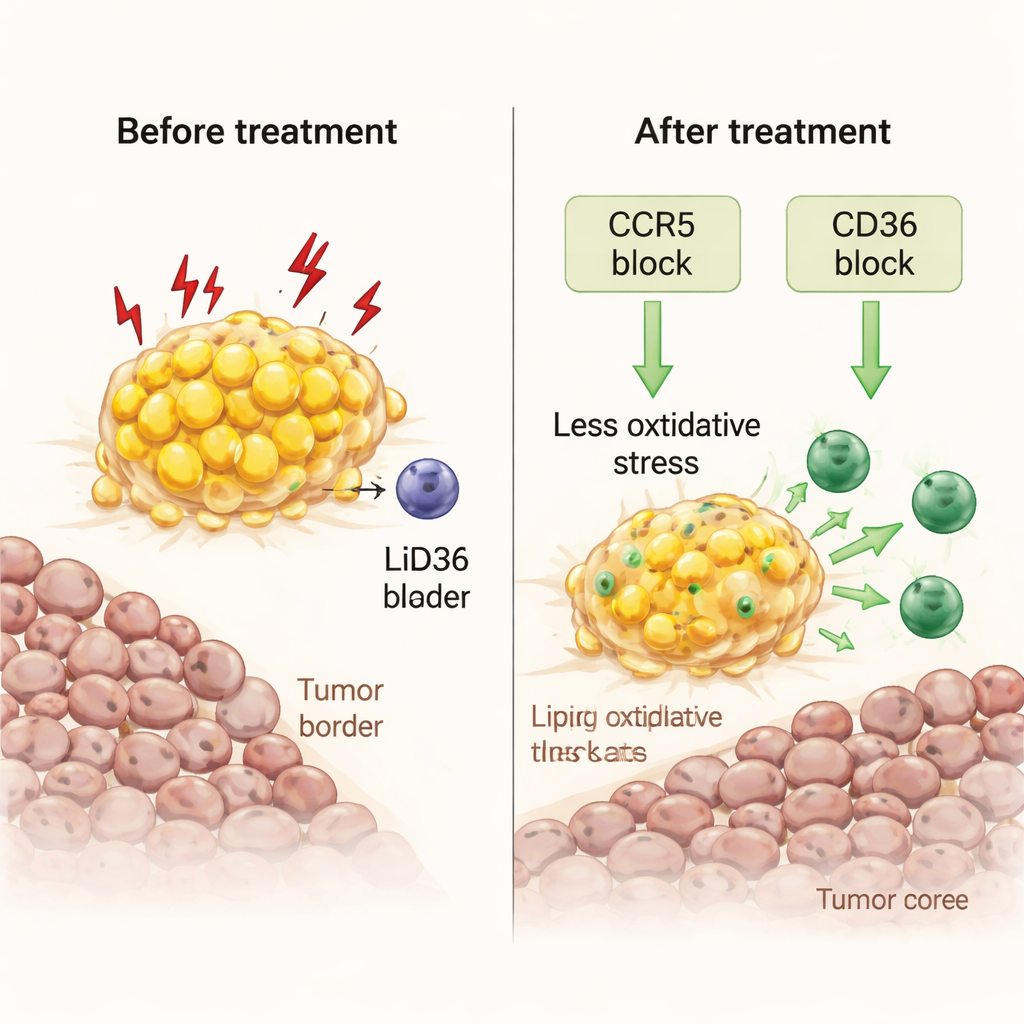
Von zellulären Signalwegen zu realistischen Modellen und Patientinnen
Um diese Ideen in einem realistischeren Kontext zu prüfen, nutzte das Team humanisierte Mäuse, die mit einem humanähnlichen Immunsystem ausgestattet waren, und verpflanzte menschliche Brusttumoren in fettreiche Gewebe. Die Maraviroc‑Behandlung programmierte die humanen Makrophagen in diesen Tieren auf eine Weise um, die den patientengebundenen Proben ähnelte: reduzierte Lipid‑ und Stresssignaturen, erhöhte Zytokinproduktion und stärkere Unterstützung von T‑Zell‑bezogenen Signalwegen. Klinisch wertvoll war außerdem, dass die Forschenden eine japanische Studie zu Nivolumab bei chemoresistentem Eierstockkrebs neu auswerteten. Jede Patientin, die von dem Medikament profitierte, hatte in den chirurgischen Proben sichtbare omentale Metastasen. Mithilfe von CT‑ oder MRT‑Aufnahmen kombiniert mit maschinellen Lernverfahren zur Analyse der Fettverteilung im Körper bauten sie einen Entscheidungsbaum, der noninvasiv Patientinnen identifizieren konnte, deren Tumoren wahrscheinlich in der Nähe von viszeralem Fett sitzen – und in einem prospektiven Fall sagte diese Methode korrekt eine Patientin voraus, die später auf Nivolumab ansprach.
Was das für zukünftige Behandlungen bedeuten könnte
Für Nichtfachleute lautet die Kernaussage: Der Ort, an dem Eierstockkrebs im Körper wächst, und die Art, wie benachbartes Fett Immunzellen umgestaltet, können stark beeinflussen, ob eine Immuntherapie wirkt. Fettreiche omentale Ablagerungen scheinen zwar lebhafte T‑Zellen zu beherbergen, enthalten aber auch überfressene, gestresste Makrophagen, die den Angriff dämpfen. Indem man die Lipidlast in diesen Makrophagen verringert und ihre oxidative Belastung mindert – etwa mit CCR5‑Blockern wie Maraviroc, CD36‑gerichteten Wirkstoffen oder verwandten Strategien – könnte es möglich werden, eine teilweise blockierte Immunantwort in einen umfassenden Angriff auf den Tumor zu verwandeln. Gleichzeitig könnten bildgebungsbasierte Messungen des Omentumbefalls Ärzten helfen zu entscheiden, welche Patientinnen am ehesten von Immun-Checkpoint‑Medikamenten profitieren, und so einen personalisierteren und potenziell wirksameren Ansatz zur Behandlung von Eierstockkrebs ermöglichen.
Zitation: Suarez-Carmona, M., Hampel, M., Zhang, XW. et al. Harnessing lipid-driven immunometabolic pathways in omental metastases to enhance immunotherapy in patients with ovarian cancer. Sig Transduct Target Ther 11, 78 (2026). https://doi.org/10.1038/s41392-026-02594-8
Schlüsselwörter: Eierstockkrebs, Omentumfett, Immuntherapie, tumorassoziierte Makrophagen, Lipidstoffwechsel