Clear Sky Science · de
Aktivierung des Thromboxanrezeptors in dendritischen Zellen mildert Sepsis durch Unterdrückung der S100a8/a9-vermittelten Neutrophilenrekrutierung
Warum es wichtig ist, eskalierende Infektionen zu zügeln
Sepsis ist eine lebensbedrohliche Überreaktion des Körpers auf eine Infektion, die oft in Lunge oder Darm beginnt und zu einem Versagen mehrerer Organe führen kann. Selbst mit moderner Intensivmedizin fordert Sepsis weltweit Millionen Todesopfer, weil Standardtherapien hauptsächlich die ausgefallenen Organe stützen, statt das fehlgeleitete Immunsystem gezielt zu beruhigen. Diese Studie offenbart eine zuvor verborgene „Bremse“ in einem wichtigen Immunzelltyp — den dendritischen Zellen — die schädliche Entzündungen zurückfahren kann, ohne die Fähigkeit des Körpers, Krankheitserreger zu bekämpfen, auszuschalten.
Immun-Wachposten unter Druck
Dendritische Zellen fungieren als Sentineln des Immunsystems: Sie erkennen Gefahren, alarmieren andere Immunzellen und helfen zu entscheiden, wie stark eine Antwort ausfallen soll. In Blutproben von Sepsispatienten fanden die Autorinnen und Autoren nicht nur eine verringerte Zahl dendritischer Zellen, sondern auch deutlich reduzierte Spiegel eines Rezeptors namens TP, der normalerweise auf das fettartige Molekül Thromboxan A₂ reagiert. Patienten, deren dendritische Zellen die niedrigsten TP-Spiegel aufwiesen, hatten tendenziell mehr zirkulierende Neutrophile — die ersten weissen Blutkörperchen in der Infektionsabwehr — und schwerere Verläufe. Das deutet darauf hin, dass, wenn diese dendritische „Bremse“ versagt, Entzündungen außer Kontrolle geraten können.
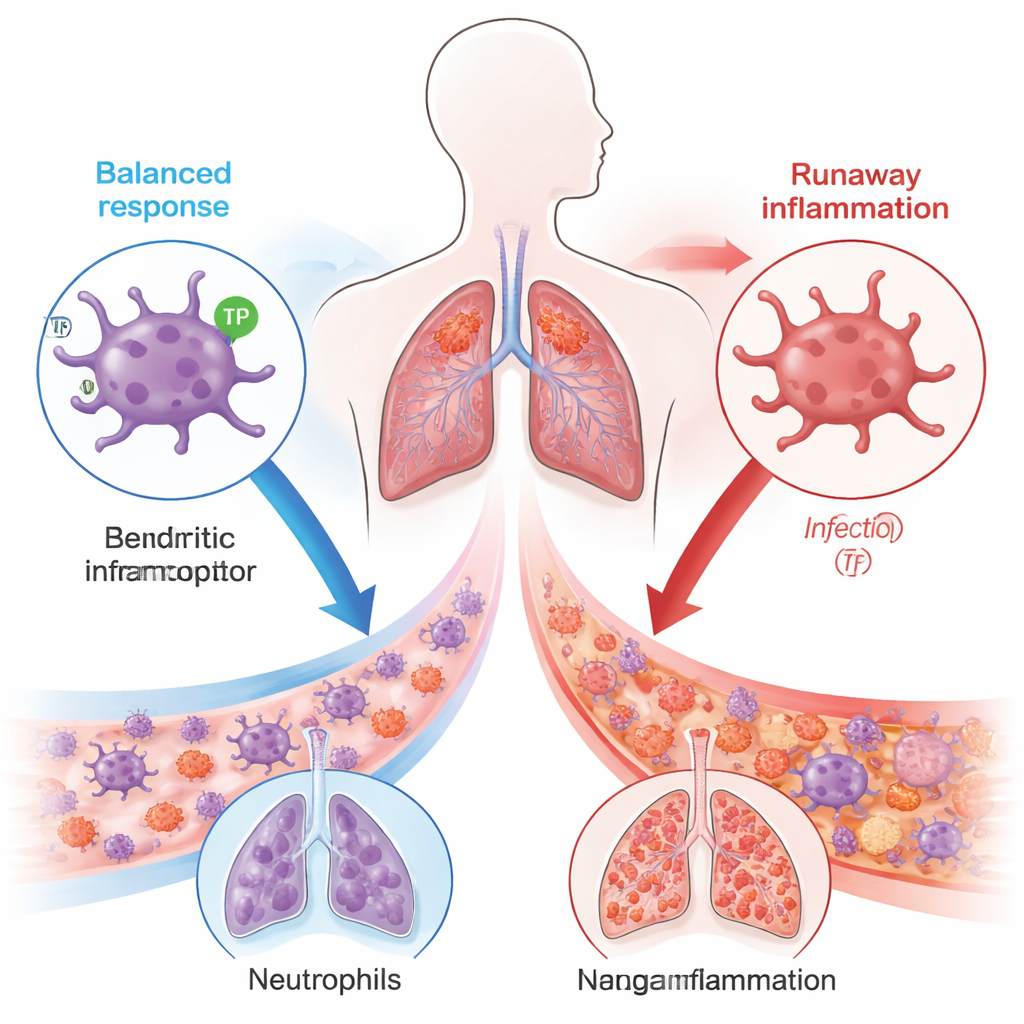
Wenn die Bremse versagt, überfluten Neutrophile die Lungen
Um Ursache und Wirkung zu klären, verwendete das Team Mausmodelle der Sepsis, ausgelöst entweder durch Perforation des Darms (ein Eingriff, der Darmbakterien in die Bauchhöhle freisetzt) oder durch Verabreichung bakterieller Toxine. Mäuse, denen TP nur in ihren dendritischen Zellen fehlte, hatten deutlich schlechtere Chancen: Sie starben häufiger, zeigten durchlässigere, mit Flüssigkeit gefüllte Lungen und Zeichen starker Neutrophileninfiltrate und Gewebeschädigung. Wenn dendritische Zellen von TP-defizienten Tieren in gesunde Mäuse übertragen wurden, entwickelten auch diese Empfänger schwerere Sepsis, was bestätigt, dass allein gestörte Signalgebung in dendritischen Zellen das Gleichgewicht zugunsten tödlicher Entzündung kippen kann.
Ein Gefahrensignal, das zu viele Verteidiger herbeiruft
Bei tiefergehender Analyse untersuchten die Forschenden, welche Gene sich in dendritischen Zellen veränderten, wenn TP fehlte. Zwei gefahrassoziierte Proteine, S100A8 und S100A9, fielen als stark erhöht auf. Diese Moleküle wirken wie Leuchtfeuer, die Neutrophile in entzündete Gewebe rufen. Das Team zeigte, dass dendritische Zellen aus septischen Mäusen in Laborversuchen mehr Neutrophile anzogen, und dass das Blockieren von S100A8/A9 mit einem Wirkstoff diesen Zug deutlich verminderte. Sowohl in Mäusen als auch bei Patienten gingen höhere S100A8/A9-Spiegel mit niedrigeren TP-Spiegeln einher. In lebenden Tieren reduzierte das gezielte Entfernen von S100A9 in dendritischen Zellen — oder die Blockade seines Hauptrezeptors, des Immunsensors TLR4 — den Neutrophilenansturm, verringerte die Bildung klebriger DNA-Protein-Netze (NETs) und schützte die Lungen vor Schäden.
Die Signalkette hinter einer gezielten Bremse
Die Autorinnen und Autoren kartierten dann, wie TP die S100A8/A9-Produktion in dendritischen Zellen steuert. Die Aktivierung von TP löste eine interne Kaskade aus, an der eine Proteinkinase (PKCδ) und ein Transkriptionsfaktor namens STAT1 beteiligt sind, der in den Zellkern wandert, um die Genaktivität zu beeinflussen. Wenn dieser Weg intakt war, trug STAT1 dazu bei, S100A8/A9-Spiegel in Schach zu halten und damit die Rekrutierung von Neutrophilen zu begrenzen. Die Blockade von PKCδ oder STAT1 unterbrach diesen Schutzmechanismus, sodass S100A8/A9 anstieg. Schließlich entwickelten die Forschenden einen nanoskaligen Wirkstoff, der eine TP-aktivierende Verbindung an ein Peptid koppelt, das gezielt dendritische Zellen ansteuert. In septischen Mäusen stellte diese gezielte Behandlung das TP-Signal nur in dendritischen Zellen wieder her, senkte S100A8/A9, reduzierte Anhäufung von Neutrophilen und NETs in den Lungen und verbesserte das Überleben — und das, ohne das Immunsystem generell zu unterdrücken.
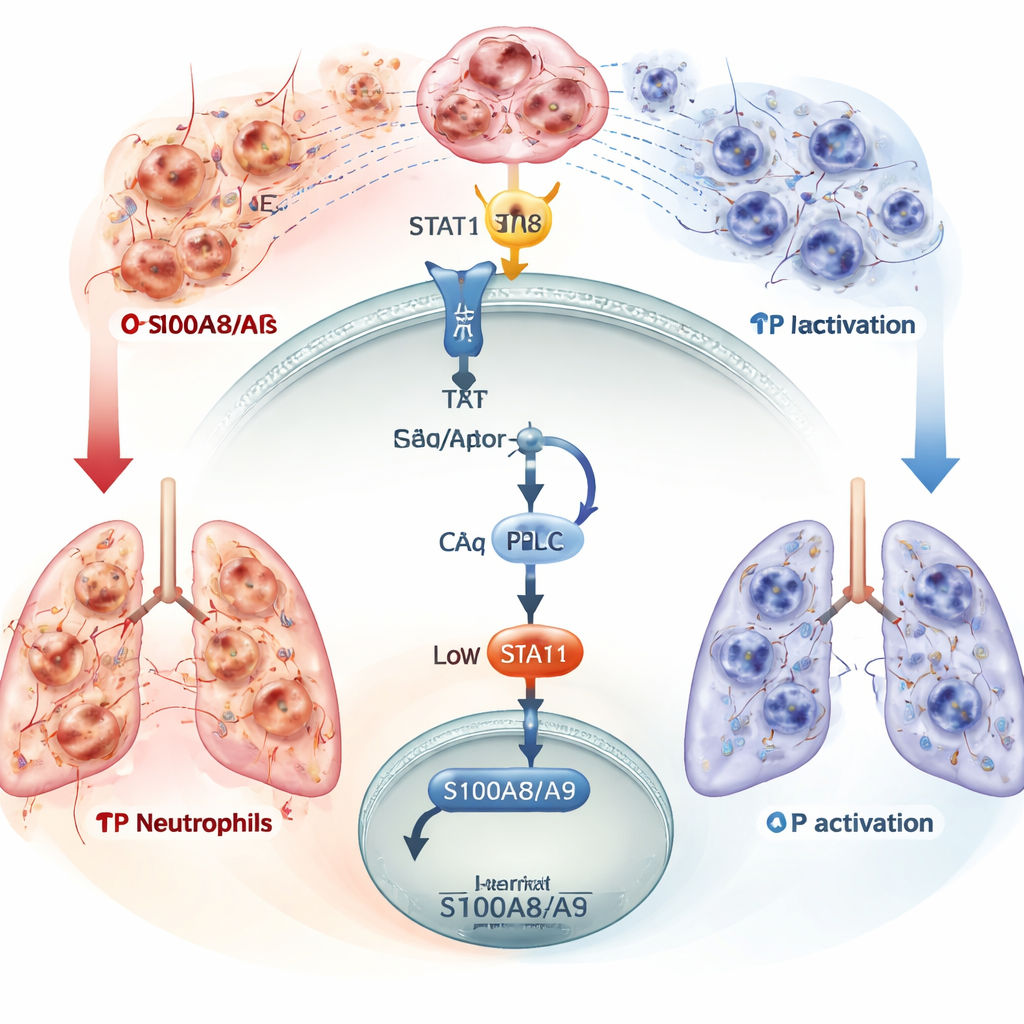
Aus einer Entdeckung künftige Sepsis-Therapien machen
Für eine allgemeine Leserschaft lautet die Kernbotschaft: Nicht jede Entzündung ist schlecht — aber zu viel an der falschen Stelle kann tödlich sein. Diese Arbeit identifiziert einen präzisen Schaltkreis in dendritischen Zellen, der normalerweise verhindert, dass Neutrophile die Lungen bei schweren Infektionen überfluten. Fällt die TP-Signalgebung aus, produzieren dendritische Zellen das Alarmsignal S100A8/A9 im Übermaß und rufen Wellen von Neutrophilen herbei, die Gewebe schädigen statt zu helfen. Durch die Reaktivierung von TP ausschließlich auf dendritischen Zellen — oder durch Blockade des S100A8/A9-Wegs — könnte man die schädliche Seite der Entzündung abkühlen und zugleich die Fähigkeit des Körpers, Infektionen zu bekämpfen, weitgehend erhalten. Zwar beruhen die Befunde bislang auf Tiermodellen, doch diese zielgerichtete Strategie bietet einen vielversprechenden Ansatz für künftige, präzisere Sepsisbehandlungen.
Zitation: Du, R., Pan, T., Wang, Y. et al. Thromboxane receptor activation in dendritic cells mitigates sepsis by suppressing S100a8/a9-mediated neutrophil recruitment. Sig Transduct Target Ther 11, 75 (2026). https://doi.org/10.1038/s41392-026-02592-w
Schlüsselwörter: Sepsis, dendritische Zellen, Neutrophile, Entzündung, Immunregulation