Clear Sky Science · de
GPR54 reguliert die Entwicklung von nicht-kleinzelligem Lungenkrebs über die Dopa-Decarboxylase
Warum diese Lungenkrebsstudie wichtig ist
Lungenkrebs bleibt eine der tödlichsten Krebsarten, und die Mehrheit der Fälle gehört zu einer Form, die als nicht-kleinzelliger Lungenkrebs (NSCLC) bezeichnet wird. Viele Patientinnen und Patienten erschöpfen früher oder später die wirksamen Behandlungsoptionen, weil Tumoren sich anpassen oder gegen vorhandene Medikamente resistent werden. Diese Studie enthüllt ein bisher unterschätztes Kontrollsystem innerhalb von Lungenkrebszellen, das sich um den Rezeptor GPR54 und das Enzym Dopa-Decarboxylase (DDC) dreht. Indem Forscherinnen und Forscher untersuchen, wie diese Moleküle Tumoren beim Wachsen und bei der Energieversorgung unterstützen, zeigen sie neue Ansätze auf, NSCLC zu verlangsamen oder sogar zu verkleinern.
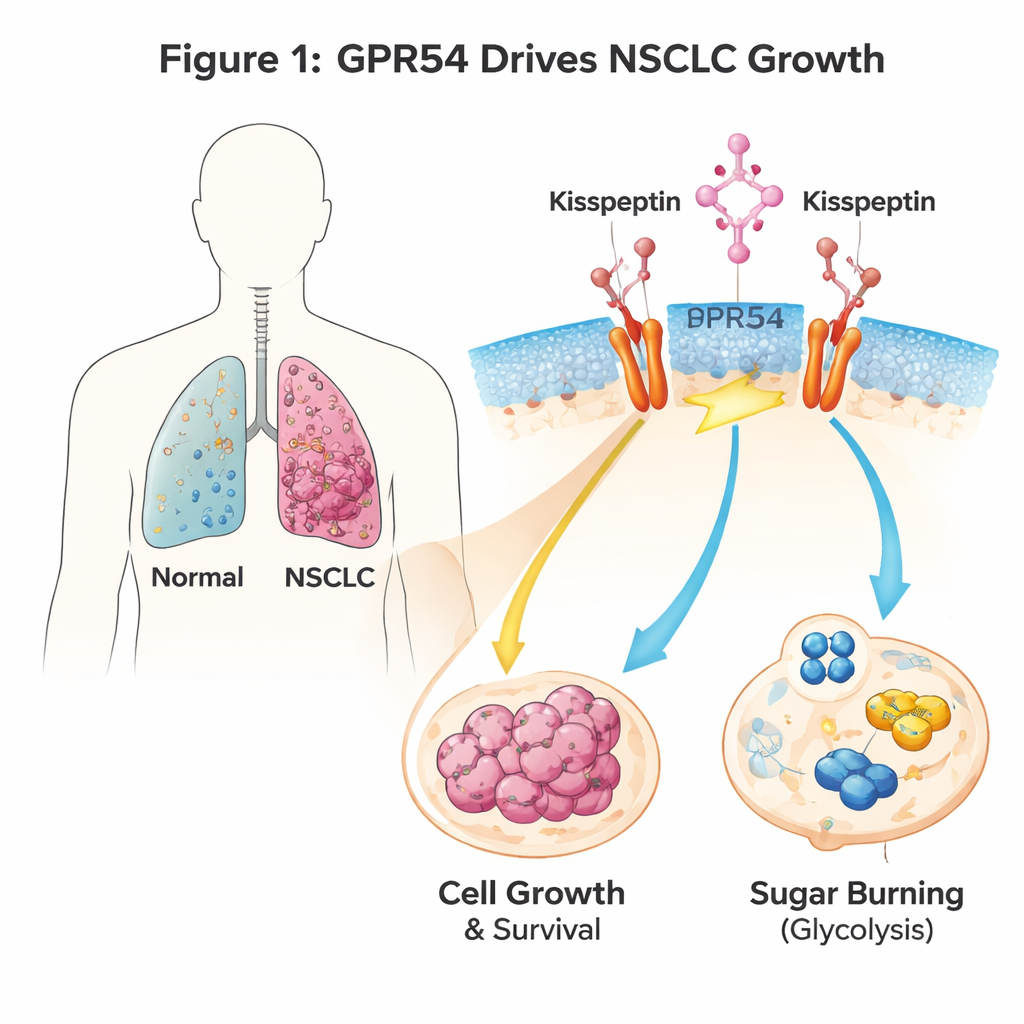
Ein Signalschalter auf Lungenkrebszellen
GPR54 ist ein Sensor auf der Zelloberfläche, der auf ein natürliches Signal namens Kisspeptin reagiert. Bekannt ist er vor allem für seine Rolle bei Pubertät und Fortpflanzung, doch er tritt auch in vielen Krebsarten auf. Die Autorinnen und Autoren verwendeten gentechnisch veränderte Mäuse, die NSCLC entwickeln, wenn in Lungenzellen ein krebstreibendes Gen namens Kras eingeschaltet wird. Wenn sie das Gpr54-Gen in diesen Mäusen entfernten, lebten die Tiere länger, entwickelten weniger und kleinere Lungentumoren, und ihre Krebszellen zeigten eindeutige Anzeichen von Selbstzerstörung (Apoptose). Menschliche NSCLC-Zelllinien bestätigten das Bild: Bei reduzierten GPR54-Werten wuchsen Tumorzellen langsamer, bildeten weniger Kolonien und gingen leichter zugrunde, unabhängig von ihren speziellen genetischen Veränderungen.
Wie GPR54 Tumorzellen am Leben erhält
Bei tiefer gehender Untersuchung fragten die Forschenden, welche internen Schaltungen GPR54 verwendet. Sie fanden heraus, dass GPR54 in zwei große Wachstumswege innerhalb der Zelle einspeist, bekannt als AKT und ERK. Beide sind verbreitete „Verkabelungsknoten“, die Krebszellen zur Teilung anregen und sie gegen Zelltod schützen. Wenn GPR54 blockiert oder entfernt wurde, sank die Aktivität von AKT und ERK, und die Zellen wurden anfälliger für Apoptose. Die Wiederherstellung starker AKT- oder ERK-Signale konnte die Zellen teilweise retten, was bestätigt, dass GPR54 NSCLC-Zellen durch die Unterstützung dieser Wachstumswege am Überleben hindert.
Umschaltung des Zuckerstoffwechsels bei Krebs
Krebszellen programmieren häufig ihre Nährstoffnutzung um und bevorzugen einen schnellen Zuckerabbau (Glykolyse), um Wachstum zu ermöglichen. Die Genexpressionsanalyse von Tumoren aus Gpr54-defizienten Mäusen zeigte, dass viele Gene, die an Zuckertransport und Energieproduktion beteiligt sind, herunterreguliert waren. In Lungenkrebszellen, die mit Kisspeptin behandelt wurden, um GPR54 zu aktivieren, zeigten Messungen von Sauerstoffverbrauch und Säureproduktion — Stellvertreter für den Energiestoffwechsel — dass GPR54 die Glykolyse fördert. Die Blockade der GPR54-Signalachse an verschiedenen Stellen (der Gαq/11-Schalter, PI3K, AKT oder mTOR) reduzierte Glukoseverbrauch und Laktatproduktion und trieb die Zellen in Richtung Apoptose. Einfach ausgedrückt: GPR54 hilft NSCLC-Zellen, Zucker schneller und effizienter zu verbrennen und so ihr rasches Wachstum zu unterstützen.
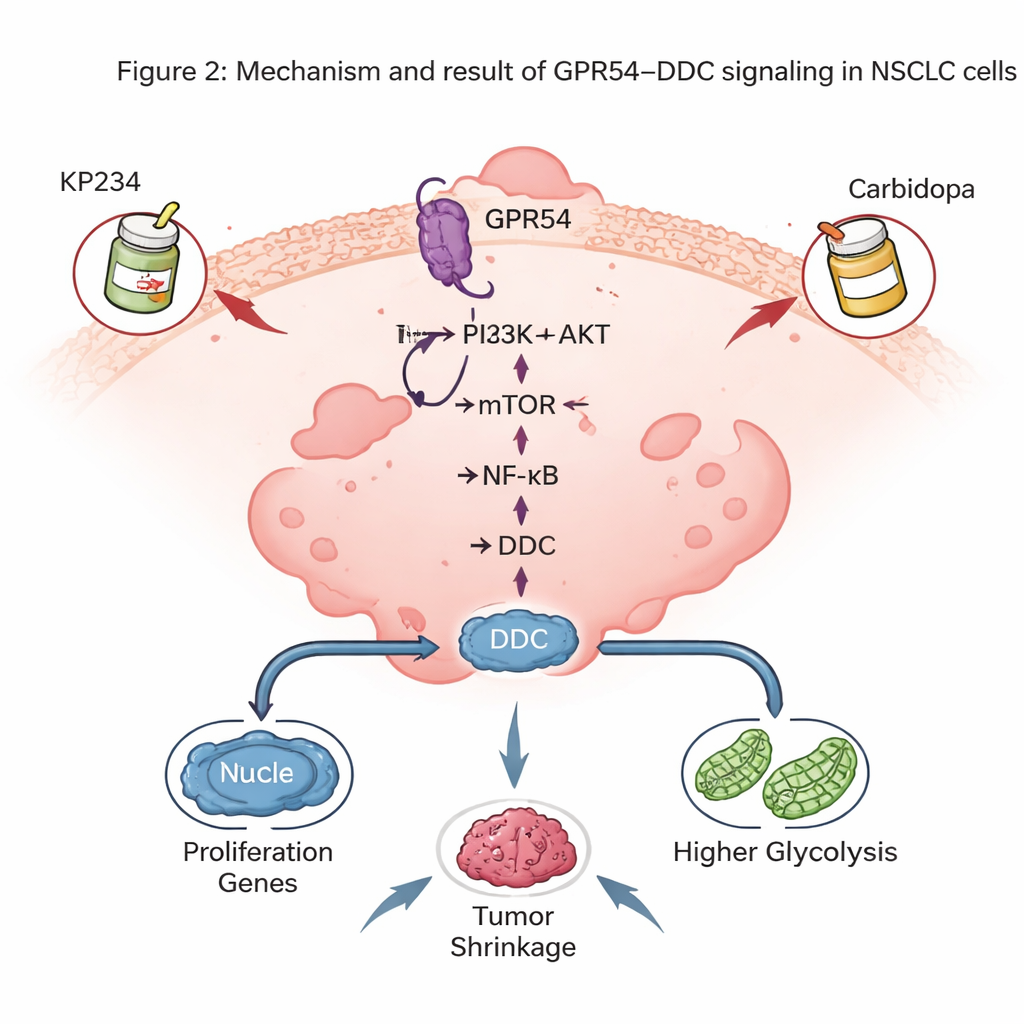
Die überraschende Rolle eines hauptsächlich im Gehirn bekannten Enzyms
Eine der auffälligsten Entdeckungen war, dass GPR54 die Mengen an DDC steuert, einem Enzym, das vor allem dafür bekannt ist, die Hirnbotenstoffe Dopamin und Serotonin zu synthetisieren. In Mäusetumoren korrelierten die DDC-Spiegel eng mit der Menge an GPR54: Weniger GPR54 bedeutete weniger DDC. Menschliche NSCLC-Tumoren und Zelllinien zeigten ebenfalls höhere DDC-Werte als normales Lungengewebe, und Patientinnen und Patienten mit erhöhtem DDC hatten eine schlechtere Überlebensprognose. Die Herunterregulierung von DDC in Lungenkrebszellen verlangsamte das Tumorwachstum in Mäusen, reduzierte die Zellteilung in Kulturen und löste mehr Apoptose aus. Auf molekularer Ebene unterstützte DDC die Aktivität des NF-κB-Signalwegs, eines zentralen Reglers, der das Überleben von Krebszellen und Entzündungsprozesse fördert, und trug außerdem zur hochglykolytischen Stoffwechsellage der Tumorzellen bei.
Erprobung einer Wirkstoff-Kombinationsstrategie
Da DDC bereits bei der Parkinson-Behandlung durch ein Medikament namens Carbidopa adressiert wird, prüften die Autorinnen und Autoren, ob die Kombination eines GPR54-Blockers (KP234) mit Carbidopa NSCLC von zwei Seiten angreifen könnte. In Zellkulturen und in Mäusemodellen, in denen menschliche NSCLC-Zellen in der Lunge wuchsen, reduzierte die Doppelbehandlung das Tumorwachstum stärker als eines der Medikamente allein und erhöhte das Absterben der Krebszellen, ohne dass die Tiere auffälliges Gewichtsverlust zeigten. Diese Kombinationen zeigten auch in Verbindung mit einigen modernen zielgerichteten Wirkstoffen gegen mutierte RAS-Gene vielversprechende Effekte, was darauf hindeutet, dass die GPR54–DDC-Signalgebung auf bestehende Präzisionstherapien aufgesetzt werden kann.
Was das für künftige Lungenkrebsbehandlung bedeutet
Für Nichtfachleute lautet die Kernbotschaft: NSCLC-Zellen sind auf eine bisher unterschätzte Zusammenarbeit zwischen einem Oberflächenschalter (GPR54) und einem Stoffwechselenzym (DDC) angewiesen, um zu überleben und Energie schnell zu verbrennen. Das Stören dieser Partnerschaft schwächt Tumoren, lässt sie langsamer wachsen und macht sie in experimentellen Modellen anfälliger für Zelltod. Zwar ist noch viel Arbeit nötig, bevor solche Strategien klinisch anwendbar sind, doch die Studie positioniert GPR54 und DDC als potenzielle Biomarker zur Identifizierung aggressiver NSCLC-Fälle und als vielversprechende Ziele für neue Kombinationstherapien, die die Behandlungsergebnisse für Patientinnen und Patienten verbessern könnten, deren Tumoren aktuellen Therapien entgehen.
Zitation: Hwang, HH., Lee, S.Y., Lee, C. et al. GPR54 regulates non-small cell lung cancer development via dopa decarboxylase. Sig Transduct Target Ther 11, 74 (2026). https://doi.org/10.1038/s41392-026-02591-x
Schlüsselwörter: nicht-kleinzelliger Lungenkrebs, GPR54, Dopa-Decarboxylase, Krebsstoffwechsel, zielgerichtete Therapie