Clear Sky Science · de
Reaktive Sauerstoffspezies (ROS) beim Krebs: vom Mechanismus zu therapeutischen Implikationen
Wenn nützliche Moleküle gefährlich werden
In jeder Zelle entstehen ständig winzige chemische Funken, sogenannte reaktive Sauerstoffspezies oder ROS, als Teil normaler Lebensprozesse. In angemessenen Mengen unterstützen sie Zellwachstum, Kommunikation und Abwehr gegen Erreger. Diese Übersicht erklärt jedoch, wie dieselben Moleküle DNA schädigen, zelluläre Steuerung unrund machen und Krebswachstum, Ausbreitung und Therapie‑Resistenz fördern können. Das Verständnis dieses „Doppellebens“ der ROS hilft Forschern, neue Krebstherapien zu entwickeln, die schädlichen oxidativen Stress dämpfen oder ihn gezielt über die Grenze treiben, um Tumorzellen zu töten.
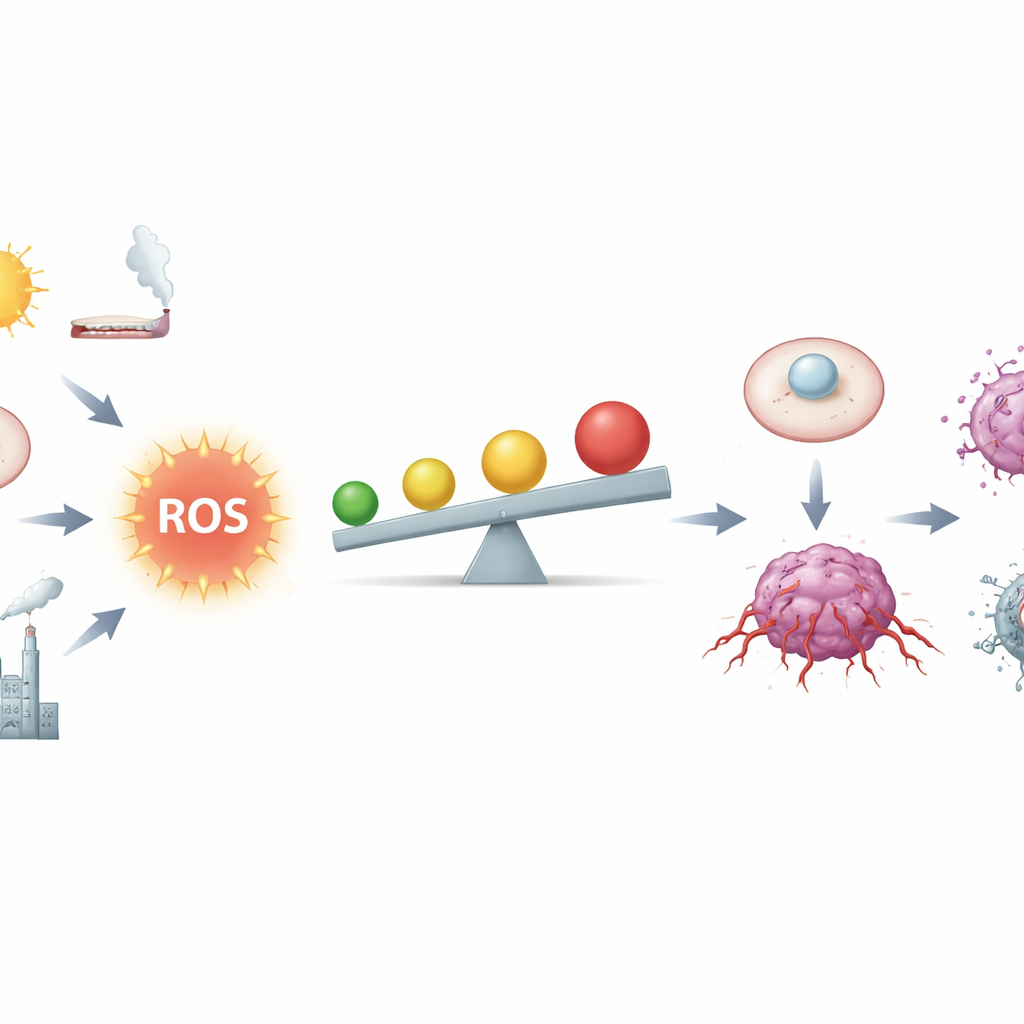
Die schmale Grenze zwischen Brennstoff und Brand
Die Autorinnen und Autoren beschreiben ROS als chemische Nebenprodukte von Atmung und Stoffwechsel, zugleich aber als starke Botenstoffe. In gesunden Geweben helfen niedrige ROS‑Mengen, den Zellzyklus zu steuern, Schäden zu reparieren und die Immunantwort feinzujustieren. Zellen halten diese Signale mit einem komplexen Antioxidantiennetzwerk in Schach, zu dem Moleküle wie Glutathion und Enzyme gehören, die von einem zentralen Schalter namens Nrf2 reguliert werden. Krebszellen hingegen leben näher an der Gefahrenzone: fehlerhafte Gene, überlastete Mitochondrien, chronische Entzündung, Tabakrauch, Strahlung und bestimmte Metalle erhöhen alle ROS. Bei mäßig erhöhten Werten können ROS DNA anritzen, Chromosomen destabilisieren und dauerhaft Wachstums‑ und Überlebensprogramme einschalten, wodurch es für eine normale Zelle leichter wird, zur Krebszelle zu werden.
Wie oxidativer Stress das Tumorverhalten prägt
Sobald ein Tumor etabliert ist, formen ROS weiterhin seine Biologie. Mäßiger oxidativer Stress aktiviert viele Wachstumswege, die Zellen zur Teilung anregen, Blutgefäße bilden lassen, in umliegendes Gewebe eindringen und Chemotherapie besser überstehen. ROS können umprogrammieren, wie Krebszellen Zucker, Fette und Aminosäuren nutzen, und den Stoffwechsel in Bahnen lenken, die zusätzliches antioxidatives Potenzial und Bausteine für neue Zellen liefern. Sie beeinflussen auch Schicksalsentscheidungen der Zelle: je nach Intensität und Kontext können ROS das Gleichgewicht zugunsten von Überlebenssignalen oder zugunsten mehrerer Formen programmierten Zelltods verschieben, darunter klassische Apoptose und neuere Formen wie Ferroptose, Nekroptose und Cuproptose. Damit sind ROS sowohl Komplizen des Tumorwachstums als auch potenzielle Auslöser der Tumor‑Selbstzerstörung.
Umprogrammierung von Immunität und Medikamenten‑Antwort
Die Übersichtsarbeit betont, dass ROS nicht nur innerhalb von Krebszellen wirken – sie verändern das Tumornachbarschaft. Hoher oxidativer Stress kann krebsbekämpfende T‑Zellen und natürliche Killerzellen erschöpfen oder abtöten, während er suppressive Zelltypen begünstigt, die den Tumor vor Angriffen schützen. ROS helfen Tumoren außerdem, „töt mich nicht“-Signale wie Checkpoint‑Proteine hochzuregulieren und damit die Wirksamkeit der Immuntherapie abzuschwächen. Gleichzeitig können moderate ROS Wirkungsresistenz fördern, indem sie Medikamenten‑Auspumpmechanismen und Stressantworten verstärken, wodurch Krebszellen Chemotherapeutika ausstoßen oder entstandene Schäden reparieren. Unter anderen Bedingungen kann das Überschreiten einer kritischen ROS‑Schwelle diese Abwehrmechanismen jedoch demontieren und Tumore wieder empfindlich für Behandlungen machen.
Redox‑Schwächen als therapeutische Strategie nutzen
Weil Krebszellen ein Kunststück vollführen zwischen der Nutzung von ROS und ihrer Vergiftung durch diese, sehen die Autorinnen und Autoren das ROS‑Gleichgewicht als therapeutischen Hebel. Eine Strategie besteht darin, schädliche ROS zu reduzieren oder Antioxidantien zu stärken, vor allem zur Prävention oder zum Schutz gesunden Gewebes während einer Behandlung. Eine andere verfolgt das Gegenteil im Tumor: Antioxidantien‑Systeme hemmen oder ROS‑Produktion steigern, bis Krebszellen eine tödliche Schwelle überschreiten, insbesondere in Kombination mit Strahlentherapie, zielgerichteten Wirkstoffen oder Immuntherapie. Ein dritter Ansatz belässt ROS‑Spiegel weitgehend, blockiert aber spezifische ROS‑sensible Schalter – Signalmoleküle, Stoffwechselenzyme oder Todeswege –, auf die Tumore angewiesen sind. Allen Ansätzen gemeinsam ist das Thema Personalisierung: Verschiedene Krebsarten tragen unterschiedliche „Redox‑Signaturen“, sodass künftige Therapien Blut‑ oder Gewebetests zu oxidativen Schäden, Antioxidantienkapazität und ROS‑verknüpften Genen benötigen könnten, um die richtige redoxgezielte Behandlung für jede Patientin und jeden Patienten auszuwählen.
Was das für Patientinnen und Patienten bedeutet
Einfach gesagt argumentiert der Artikel, dass ROS weder rein schlecht noch rein gut sind; sie sind mächtige Werkzeuge, die Zellen – und Krebs – nutzen. Krebszellen operieren tendenziell näher an einem Kipppunkt des oxidativen Stresses als gesunde Zellen, was ein therapeutisches Fenster eröffnen könnte. Da sowohl Antioxidantien als auch Pro‑Oxidantien je nach Dosis, Zeitpunkt und Tumortyp helfen oder schaden können, ist eine pauschale Einnahme von Nahrungsergänzungsmitteln oder ROS‑anhebenden Medikamenten riskant. Die Autorinnen und Autoren kommen zu dem Schluss, dass die Zukunft in sorgfältig entwickelten Therapien und Diagnostika liegt, die den Redox‑Zustand jedes Tumors bestimmen und ROS‑ sowie Antioxidantien‑Systeme so dosiert beeinflussen, dass normales Gewebe geschützt wird oder Krebszellen über ihre Belastungsgrenze hinausgetrieben werden.
Zitation: Akter, S., Madhuvilakku, R., Kar, A.K. et al. Reactive oxygen species (ROS) in cancer: from mechanism to therapeutic implications. Sig Transduct Target Ther 11, 111 (2026). https://doi.org/10.1038/s41392-026-02583-x
Schlüsselwörter: reaktive Sauerstoffspezies, oxidativer Stress, Krebsstoffwechsel, Redox-Therapie, Tumormikroumgebung