Clear Sky Science · de
Übereinstimmungsanalyse von DNA- und RNA-Profilen: Die IMPACT2-Studie des MD Anderson in der Präzisionsonkologie
Warum diese Forschung für Krebspatienten wichtig ist
Die Krebsbehandlung wird zunehmend von der genetischen Beschaffenheit des jeweiligen Tumors geleitet. Ärztinnen und Ärzte nutzen bereits DNA-Tests, um Mutationen zu finden, die mit bestimmten Medikamenten ansprechbar sind, doch diese Tests erfassen nicht alles darüber, wie sich ein Tumor verhält. Diese Studie des MD Anderson Cancer Center stellt eine praktische Frage: Wenn wir zusätzlich RNA betrachten – die „arbeitskopien“ von Genen, die zeigen, welche Gene tatsächlich ein- oder ausgeschaltet sind – können wir dann das Krebsbild eines Patienten und seine Überlebensaussichten besser verstehen?
Zwei Informationsebenen: DNA und RNA
Jede Krebszelle trägt Veränderungen in ihrer DNA, doch die DNA ist überwiegend ein statischer Bauplan. RNA hingegen bildet ab, was die Zelle in einem bestimmten Moment aktiv tut. In der IMPACT2-Studie ließen sich mehr als 800 Patientinnen und Patienten mit fortgeschrittenen Krebserkrankungen genetisch profilieren. Bei 253 von ihnen lagen sowohl DNA- als auch RNA-Daten vor. Die Forschenden verglichen, welche Gene auf DNA-Ebene verändert waren (wie Mutationen oder Kopienzahlveränderungen) und welche Gene ungewöhnlich hohe oder niedrige RNA-Spiegel zeigten, um zu prüfen, wie oft beide Ebenen dasselbe Bild gaben und ob diese Informationen mit der Überlebensdauer der Patienten zusammenhingen.
Wenn Genveränderungen und Aktivität übereinstimmen
Das Team suchte zunächst nach „koncordanten" Ereignissen – Fällen, in denen dasselbe Gen sowohl auf DNA- als auch auf RNA-Ebene auffällig war. Unter den 253 Patientinnen und Patienten hatten 50 mindestens eine solche Übereinstimmung, insgesamt 58 Ereignisse in 23 Genen. Die meisten betrafen zusätzliche oder fehlende Kopien eines Gens, das zugleich erhöhte oder verringerte RNA-Spiegel zeigte; diese Übereinstimmung war am stärksten für bekannte Krebs-Treiber wie CDKN2A, AR, ESR1, KRAS, PIK3CA, AKT2, TP53 und CCND1. Diese Befunde stützen die Auffassung, dass strukturelle DNA-Veränderungen bei einigen Schlüsselgenen tatsächlich in eine erhöhte oder verringerte Genaktivität übersetzt werden und damit ihre Bedeutung als therapeutische Ziele unterstreichen.
Verborgene Zusammenhänge, aufgedeckt durch RNA‑Signale
Über einfache Eins-zu-eins-Übereinstimmungen hinaus testeten die Forschenden mehr als 12.000 Genpaare, um zu sehen, ob eine DNA-Veränderung in einem Gen konsistent mit abnormen RNA-Spiegeln in einem anderen verknüpft war. Sie fanden 123 signifikante Paare. Viele davon gruppierten sich in einem wichtigen Wachstums- und Überlebensnetzwerk, der PI3K/AKT-Signalbahn, die oft Ziel von gezielten Therapien ist. Ein besonders auffälliges Muster verband Veränderungen im Tumorsuppressorgen TP53 mit überaktiven RNA-Signalen von VEGFA, einem Gen, das Tumoren beim Aufbau neuer Blutgefäße hilft. Diese Beziehung könnte erklären, warum einige Patientinnen und Patienten mit TP53-Veränderungen in ihrem Tumor auf Bevacizumab ansprechen, ein Medikament, das die Gefäßneubildung hemmt, und zeigt, wie RNA-Daten klinisch relevante Gen‑Gen-Interaktionen offenbaren können, die allein durch DNA-Daten verborgen bleiben.
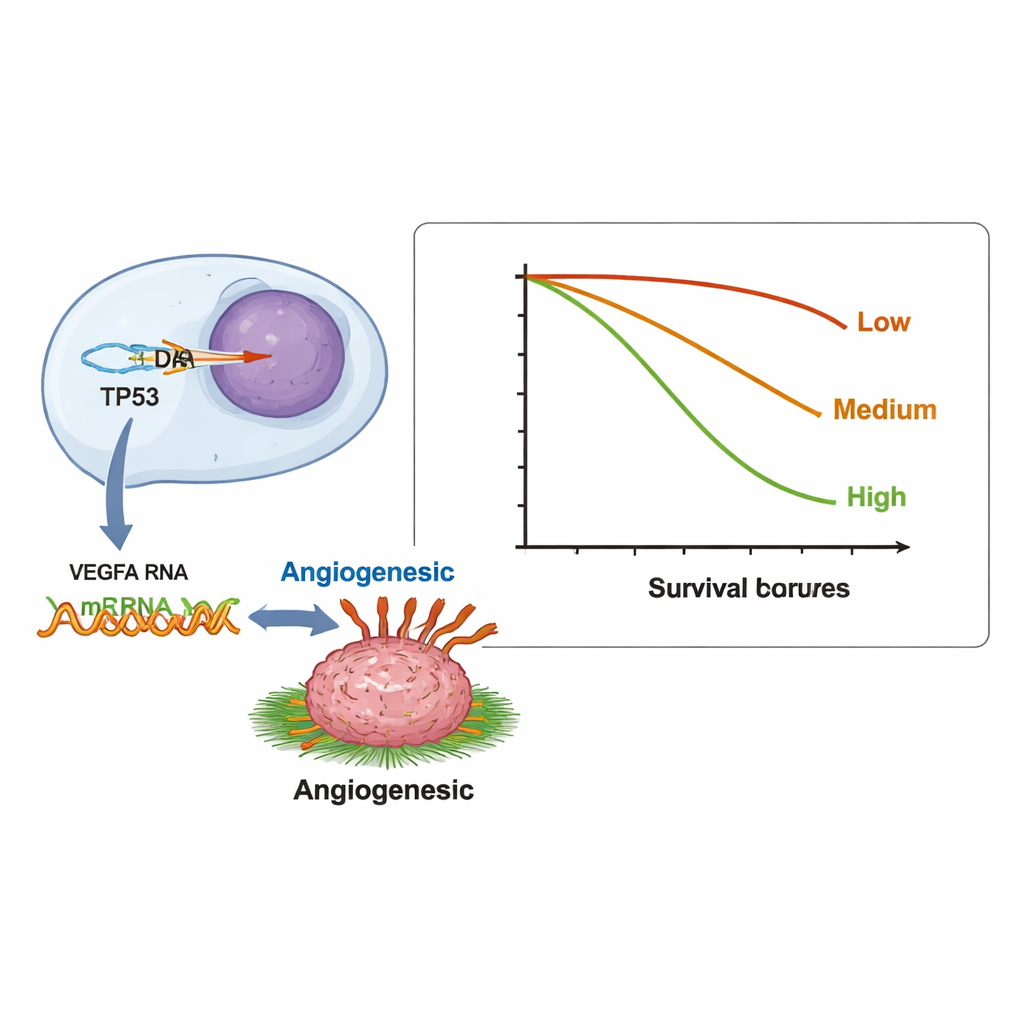
Genaktivitätslast und Patient:innenüberleben
Die Untersuchenden fragten außerdem, ob die Gesamtmenge abnormaler Genaktivität in einem Tumor – was sie als transkriptionelle Tumorlast (TTB) bezeichnen – mit der Überlebenszeit der Patientinnen und Patienten zusammenhing. Sie erfassten, wie viele Gene bei jeder Person veränderte RNA-Spiegel zeigten, und gruppierten die Fälle in niedrig (0–2 Gene), mittel (3–5) und hoch (6 oder mehr). Patientinnen und Patienten in der Hochgruppe lebten median 6,7 Monate, verglichen mit 9,8 bzw. 11,9 Monaten in den niedrigeren Gruppen. Anders gesagt: Tumoren mit vielen fehlregulierten Genen auf RNA‑Ebene neigten dazu, aggressiver zu sein. Tumoren ohne PD-L1, einen häufig zur Auswahl für Immuntherapien verwendeten Marker, wiesen ebenfalls tendenziell mehr Gene mit abweichender Expression auf, was auf einen möglichen Zusammenhang zwischen weitreichender Genstörung und einem Tumormikromilieu, das Immunangriffen widersteht, hindeutet.
Was das für die künftige Krebsversorgung bedeutet
Die Studie zeigt, dass RNA-Profiling nützliche, ergänzende Informationen zu DNA-Tests bei realen Patientengruppen mit fortgeschrittenen Krebserkrankungen liefert. Bei einigen Genen stimmen DNA‑Veränderungen und RNA‑Aktivität überein und bestätigen bekannte Therapieziele; bei anderen decken RNA‑Muster neue Beziehungen auf, die Therapieentscheidungen leiten könnten, wie die Verbindung zwischen TP53 und VEGFA. Am wichtigsten für Patientinnen und Patienten war, dass eine hohe Last an abnormaler Genaktivität mit kürzerem Überleben verbunden war, was darauf hindeutet, dass RNA-basierte Maße Ärztinnen und Ärzten helfen könnten, die Aggressivität eines Tumors besser einzuschätzen und die Prognose zu verfeinern. Auch wenn RNA-Tests noch nicht routinemäßig zur Auswahl von Therapien eingesetzt werden, stützen diese Ergebnisse das Potenzial der Transkriptomik als nächsten Schritt in der Präzisionsonkologie, insbesondere wenn größere Studien und bessere Analysetools die Profilierung von Transkripten in die alltägliche Krebsversorgung bringen.
Zitation: Schmidt, S.T., Baysal, M.A., Fu, S. et al. Concordance analysis of DNA and RNA profiling: The MD Anderson IMPACT2 study in precision oncology. Sig Transduct Target Ther 11, 68 (2026). https://doi.org/10.1038/s41392-026-02580-0
Schlüsselwörter: Präzisionsonkologie, RNA-Profiling, DNA-Sequenzierung, transkriptionelle Tumorlast, Krebs-Biomarker