Clear Sky Science · de
Die konsensualen molekularen Subtypen des Plattenepithelkarzinoms der Speiseröhre
Warum diese Forschung für Patienten wichtig ist
Das Plattenepithelkarzinom der Speiseröhre ist eine tödliche Kehlkopf‑/Speiseröhrenkrebserkrankung mit wenigen maßgeschneiderten Behandlungsoptionen und insgesamt schlechter Überlebensprognose. Ärztinnen und Ärzte wissen, dass nicht alle Tumoren gleich reagieren, aber bisher gab es keinen klaren, einheitlichen Weg, diese Krebsarten in biologisch sinnvolle Gruppen einzuteilen. Diese Studie verknüpft vielfältige genetische und bildgebende Daten, um vier Haupttypen dieses Krebses zu definieren, und zeigt, dass oft schon ein einfaches Mikroskop‑Bild erkennen kann, welchen Typ ein Patient hat. Das eröffnet die Möglichkeit für präzisere, weniger trial‑and‑error‑basierte Behandlungen.
Ordnung in eine verwirrende Krebslandschaft bringen
Im vergangenen Jahrzehnt schlugen verschiedene Forscherteams mindestens sieben unterschiedliche Einteilungen dieses Krebses vor, basierend auf DNA‑Mutationen, Kopienzahländerungen, Genaktivität oder anderen molekularen Messgrößen. Jedes System nutzte unterschiedliche Daten und Methoden, wodurch sich überlappende, aber nicht identische Subtypen entstanden und die klinische Anwendung erschwert wurde. Die Autorinnen und Autoren analysierten zunächst eine gut charakterisierte Kohorte von 152 chinesischen Patientinnen und Patienten erneut, für die mehrere Datenschichten vorlagen, darunter Ganzgenomsequenzierung, Genexpressionsdaten, DNA‑Methylierung und microRNA‑Profile. Mithilfe einer Methode namens Similarity Network Fusion kombinierten sie all diese Daten zu einem einheitlichen Bild und identifizierten vier Multi‑Omics‑Subtypen. Anschließend bauten sie ein statistisches „Netzwerk der Subtypen“, das ihre neuen Gruppen mit 21 zuvor publizierten Systemen verknüpfte und starke Verbindungen zwischen den Studien offenbarte.
Vier zentrale biologische Persönlichkeiten des Tumors
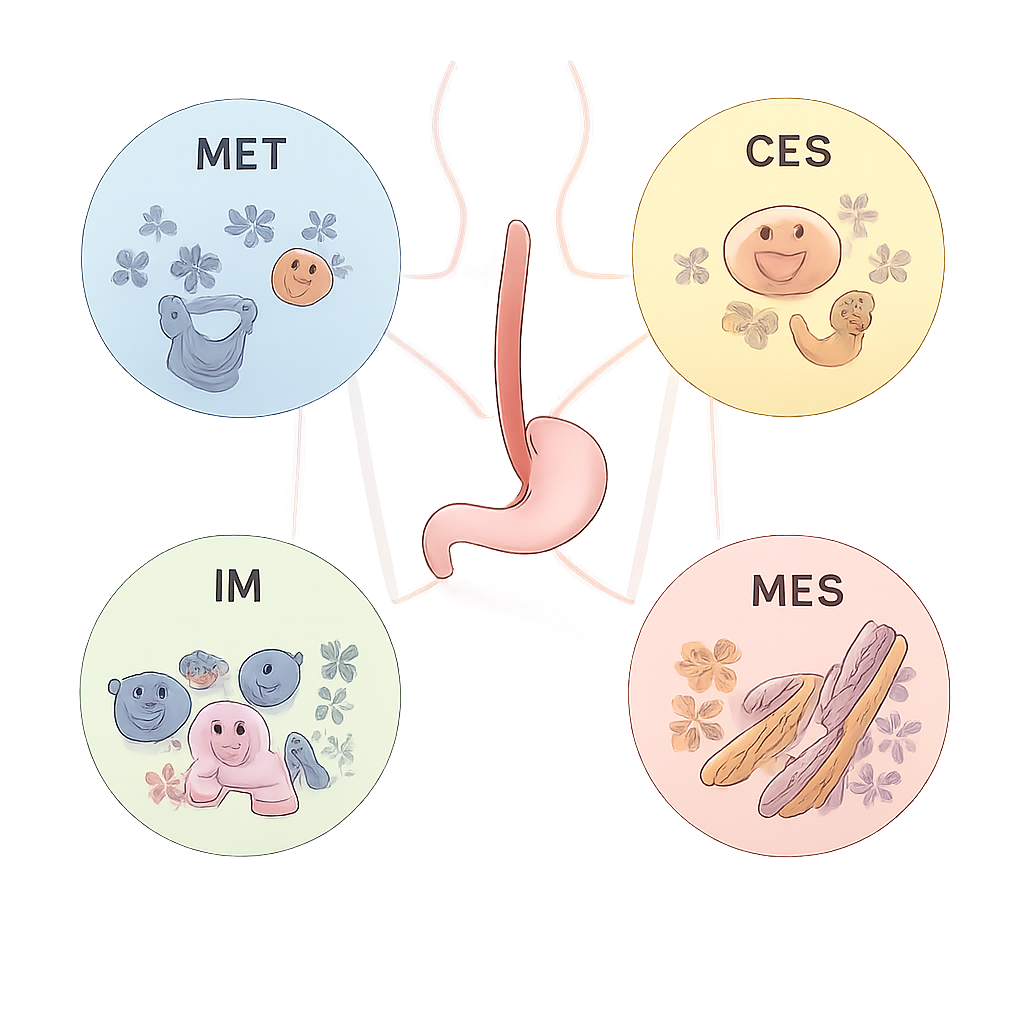
Aus diesem Netzwerk destillierte das Team vier konsensuale molekulare Subtypen, benannt ECMS1 bis ECMS4, jeweils mit unterschiedlichem Verhalten. ECMS1, der metabolische Typ (MET), zeigt hohe Aktivität in Signalwegen, die Medikamente und Nährstoffe verarbeiten, und häufige Aktivierung des Gens NFE2L2, was Resistenzen gegen Chemotherapie und Strahlentherapie fördern kann. ECMS2, der klassische Typ (CLS), ist von starker Zellzyklus‑ und Wachstums‑Signalaktivität geprägt und weist oft zusätzliche Kopien des ERBB2‑(HER2‑)Gens auf. ECMS3, der Immun‑Typ (IM), hat insgesamt eine geringere Mutationslast, aber eine starke Aktivierung des Immunsystems, einschließlich hoher Aktivität des PD‑1‑Checkpoint‑Pathways. ECMS4, der mesenchymale Typ (MES), zeigt Merkmale wie Gewebeumbau, Gefäßbildung und eine verstärkte Mobilität und Invasivität der Zellen – Eigenschaften, die mit schlechteren Prognosen verknüpft sind.
Subtypen mit Prognose und Therapieoptionen verknüpfen
Beim Vergleich dieser vier Gruppen mit klinischen Daten der Patienten zeigten sich klare Muster. Patientinnen und Patienten mit mesenchymalen ECMS4‑Tumoren hatten das höchste Rückfallrisiko sowie das schlechteste Gesamt‑ und tumorfrei‑Überleben. Die immunalen ECMS3‑Tumoren sprachen trotz ihres aktiven Immunumfelds schlecht auf die Standard‑Chemo‑Radiotherapie an, zeigten jedoch eine höhere Ansprechrate auf eine Anti‑PD‑1‑Immuntherapie. Die klassischen ECMS2‑Tumoren erschienen empfindlicher gegenüber gängigen Chemotherapeutika wie Cisplatin und Taxanen, und ihre häufige HER2‑Amplifikation legt nahe, dass sie von HER2‑gerichteten Medikamenten profitieren könnten. Die metabolischen ECMS1‑Tumoren, die durch NFE2L2‑Aktivität und bestimmte Wachstumsfaktorrezeptoren geprägt sind, könnten besser mit Wirkstoffen behandelt werden, die diese metabolischen und Signalwege gezielt hemmen. Kurz gesagt, die vier Subtypen deuten auf unterschiedliche Verwundbarkeiten und verschiedene wahrscheinliche Therapieantworten hin.
Einem Computer beibringen, molekulare Hinweise in Routinepräparaten zu sehen
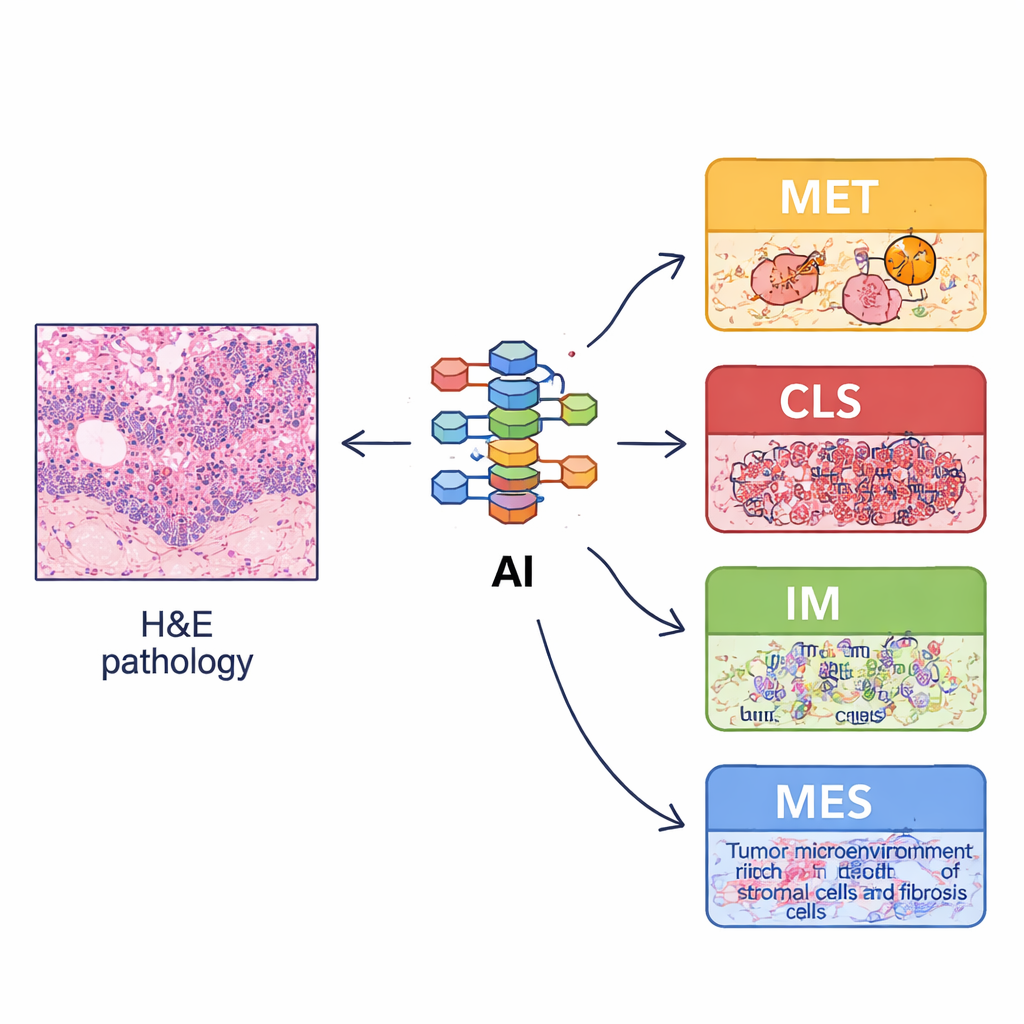
Da vollständige molekulare Profilierungen kostspielig sind und in vielen Krankenhäusern nicht verfügbar, prüfte das Team, ob gewöhnliche Hämatoxylin‑und‑Eosin‑(H&E‑)Präparate als Stellvertreter dienen könnten. Sie trainierten ein Deep‑Learning‑System mit Zehntausenden annotierter Bildausschnitte, um grundlegende Gewebeelemente wie Tumorzellen, Stroma, Lymphozyten, Drüsen und Muskel zu erkennen. Aus Ganzglasobjektträgerbildern berechneten sie anschließend „räumliche Organisationsmerkmale“ – wie viel von jedem Gewebetyp vorhanden ist, wie diese angeordnet sind und wie stark sie vermischt oder getrennt auftreten. Diese bildbasierten Muster spiegelten die Biologie der vier Subtypen wider: So zeigten beispielsweise die immunalen ECMS3‑Tumoren mehr Lymphozyten und normale Strukturen, während ECMS4‑Tumoren mehr unterstützendes Stroma aufwiesen. Mithilfe dieser Merkmale entwickelten sie einen bildbasierten Klassifikator namens imECMS, der Objektträger mit guter Genauigkeit in mehreren unabhängigen Patientengruppen den Typen MET, CLS, IM oder MES zuordnen konnte.
Was das für die künftige Versorgung bedeutet
Für Nicht‑Spezialisten lässt sich festhalten, dass diese Studie einen scheinbar einheitlichen Krebs in vier biologisch unterschiedliche Erkrankungen verwandelt, jede mit eigenem typischem Verlauf und optimierten Behandlungsstrategien. Noch wichtiger ist, dass ein großer Teil dieser Informationen automatisch aus den routinemäßigen Mikroskopbildern gewonnen werden kann, die bereits bei jeder Patientin und jedem Patienten vorliegen, ohne teure Sequenzierungen. Mit weiterer Validierung in größeren und diverseren Kohorten könnten die ECMS‑ und imECMS‑Systeme Ärztinnen und Ärzten helfen, Patientinnen und Patienten mit Plattenepithelkarzinom der Speiseröhre den Therapien zuzuordnen, von denen sie am ehesten profitieren, und sie gleichzeitig vor Behandlungen zu bewahren, die wahrscheinlich nicht wirken.
Zitation: Cui, H., Zhu, Z., Xu, E. et al. The consensus molecular subtypes of esophageal squamous cell carcinoma. Sig Transduct Target Ther 11, 65 (2026). https://doi.org/10.1038/s41392-026-02577-9
Schlüsselwörter: Speiseröhrenkrebs, Tumoruntertypen, präzisionsonkologie, Tiefenlern‑Pathologie, Immuntherapie