Clear Sky Science · de
Ringfingerprotein 213 reguliert B‑Zell‑Rezeptor‑Signalgebung, Stoffwechsel und Entwicklung in B-Lymphozyten
Wie ein wenig bekanntes Protein Antikörper auf Kurs hält
Unser Immunsystem ist auf B‑Zellen angewiesen, die Antikörper herstellen, uns bei der Bekämpfung von Infektionen helfen und sich an frühere Erreger erinnern. Diese Studie zeigt, wie ein riesiges, interferon‑antwortbares Protein namens RNF213 B‑Zellen während ihrer Reifung leitet, wie sie Gefahr wahrnehmen, ihren eigenen Betrieb mit Energie versorgen und schließlich wirksame Antikörper produzieren. Das Verständnis dieses Kontrollsystems könnte erklären, warum manche Menschen anfälliger für Infektionen oder Immunungleichgewichte sind, und könnte sogar einen Zusammenhang zwischen Immunstörungen und einer seltenen Gefäßerkrankung herstellen, die mit RNF213 verknüpft ist.
Ein Verkehrslotsen für B‑Zellen
B‑Zellen tun weit mehr, als nur Antikörper zu sekretieren: Sie müssen sich durch unterschiedliche Entwicklungsstadien bewegen, Signale von eindringenden Mikroben lesen und ihren Stoffwechsel an den Energiebedarf anpassen. Die Forschenden entdeckten, dass RNF213 in diesen Prozessen in der Milz, dem Aufenthaltsort vieler B‑Zellen, als wichtiger Verkehrslotsen wirkt. Mäuse ohne RNF213 zeigten eine verschobene Balance zwischen zwei Haupttypen von B‑Zellen: follikuläre B‑Zellen, die langfristige Antikörperantworten unterstützen, und marginalzonen B‑Zellen, die schnelle Abwehr gegen bestimmte im Blut vorkommende Mikroben liefern. Zwar blieben die Gesamtzahlen der B‑Zellen größtenteils unverändert, doch die Struktur des B‑Zell‑Kompartiments war deutlich gestört, was RNF213 als internen Organisator von B‑Zell‑Populationen nahelegt.
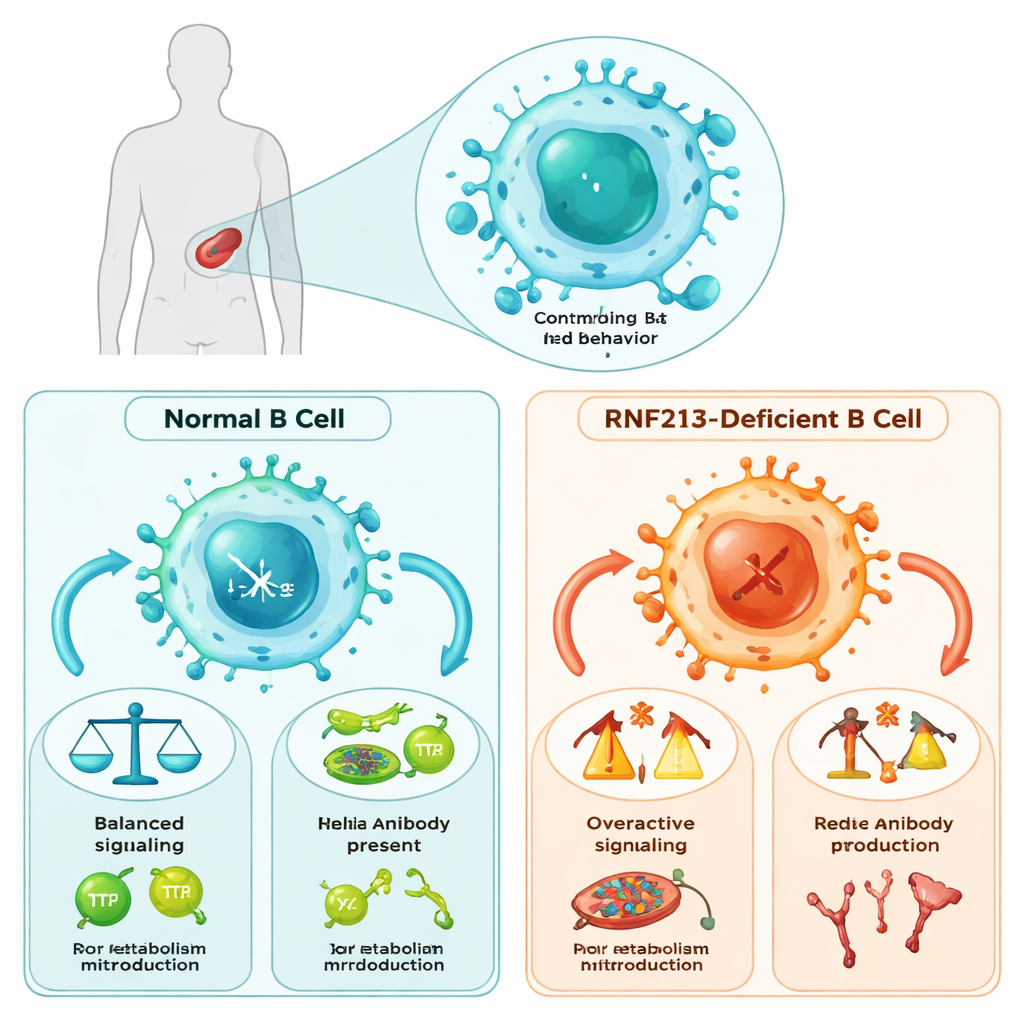
Wenn B‑Zellen den Alarm nicht mehr hören
Um ihre Aufgabe zu erfüllen, sind B‑Zellen auf eine molekulare „Antenne“ angewiesen, den B‑Zell‑Rezeptor (BCR), der fremde Moleküle erkennt und Signalkaskaden im Inneren der Zelle auslöst. Bei Mäusen ohne RNF213 funktionierte dieses Alarmsystem nicht richtig: BCRs kristallisierten schlecht auf der Zelloberfläche, und zentrale Signalproteine wurden weniger effizient aktiviert. Nachgeschaltete Hauptwege, die Genaktivität und Überleben steuern — etwa NFκB, STAT und MAPK — waren abgeschwächt. Am wichtigsten war, dass der PI3K–AKT–mTOR‑Weg, der eingehende Signale mit Energieverbrauch und Wachstum verbindet, stark geschwächt war. Diese Defekte traten in mehreren B‑Zell‑Untergruppen auf, was darauf hindeutet, dass RNF213 ein breit wirkendes Signalgerüst stützt und nicht nur einen einzelnen schmalen Pfad.
Stromversorgungsprobleme innerhalb von Immunzellen
Der Signalverlust ging mit einer Energiekrise einher. Metabolische Tests zeigten, dass RNF213‑defiziente B‑Zellen eine reduzierte mitochondriale Funktion aufwiesen und weniger reaktive Sauerstoffspezies produzierten, die normalerweise als kontrollierte „Zündfunken“ für die Immunaktivierung dienen. Sowohl die Glykolyse — der Zuckerabbau für schnelle Energie — als auch die oxidative Phosphorylierung — der langsamere mitochondriale Energiemechanismus — waren vermindert. Die Genexpressionsanalysen zeigten weitreichende Absenkungen in Stoffwechselprogrammen, einschließlich Fett‑ und Cholesterinverarbeitung. Zusammen deuten diese Befunde darauf hin, dass RNF213 nicht nur ein Signalphilfelement ist, sondern auch wesentlich dafür, den B‑Zell‑Stoffwechsel so umzubauen, dass die Zellen sich bei Antigenkontakt schnell hochfahren können.
Eine molekulare Kettenreaktion: Vom Genregler zum Treibstoffausfall
Tiefer gehende Untersuchungen ergaben, dass RNF213 einen Transkriptionsfaktor namens SPIB in Schach hält. RNF213 markiert SPIB mit einem molekularen „Abbauschild“ und schickt ihn zum zellulären Proteinrecyclingsystem. Ohne RNF213 akkumuliert SPIB und schaltet zusätzliche Kopien eines Gens namens Pik3c3 an, das das Enzym PIK3C3 codiert. Dieses Enzym erzeugt ein Lipidsignal, PI3P, auf frühen Endosomen — winzigen internen Membranhüllen. Überschüssiges PI3P zieht mehr des Enzyms PTEN an diese Membranen, wo PTEN ein anderes Lipidsignal, PIP3, abbaut, das entscheidend ist, um AKT und mTOR zu aktivieren. Kurz gesagt: Zu viel SPIB und PIK3C3 führt zu zu viel PI3P, das PTEN rekrutiert, um PIP3 zu zerstören, wodurch die AKT–mTOR‑Stromleitung durchtrennt und der B‑Zell‑Stoffwechsel und das Wachstum lahmgelegt werden.
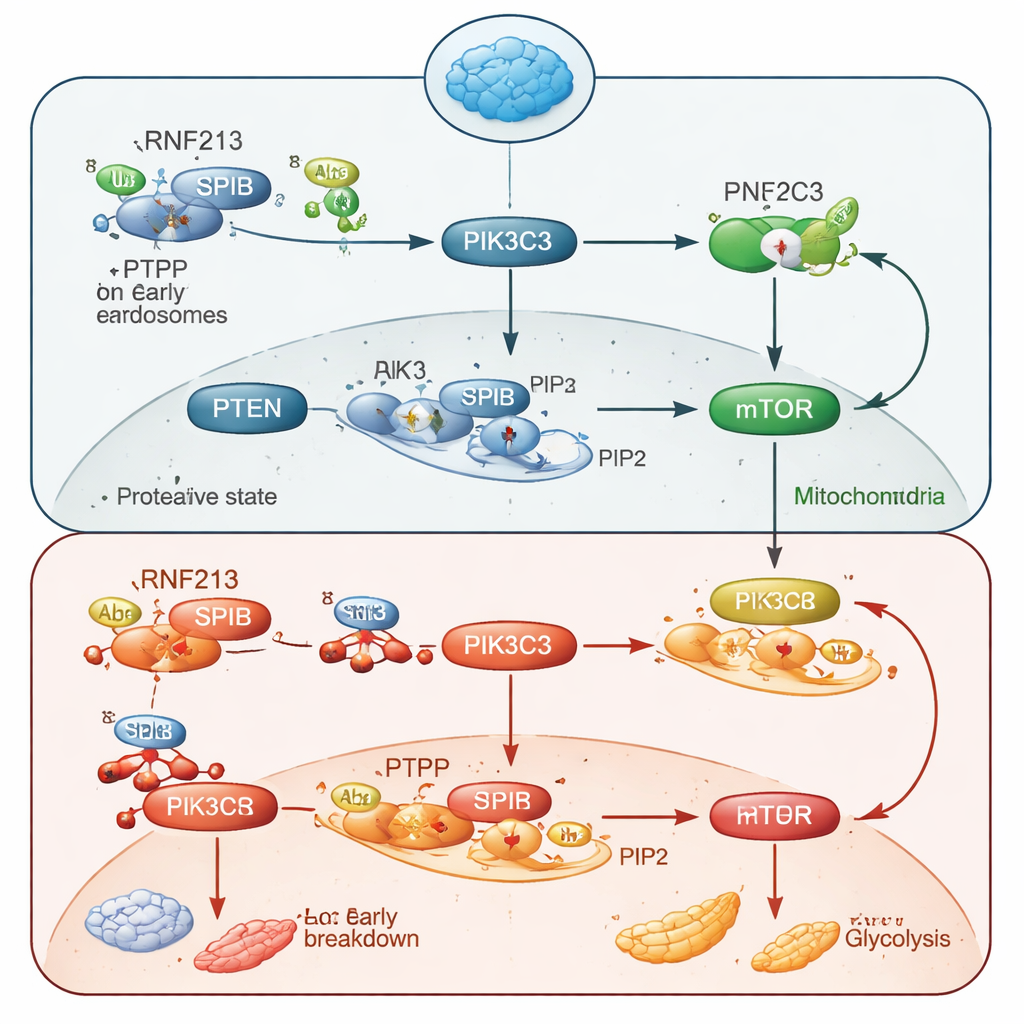
Den Schaltkreis reparieren und Antikörperantworten wiederherstellen
Die Forschenden prüften, ob die Kettenreaktion korrigiert und die B‑Zell‑Funktion gerettet werden kann. Als sie SPIB genetisch in Mäusen ohne RNF213 entfernten oder PIK3C3 mit dem Wirkstoff SAR405 blockierten, gewannen B‑Zellen stärkere AKT–mTOR‑Signalgebung, gesündere Mitochondrien und normalere metabolische Aktivität zurück. Diese Eingriffe reparierten auch viele der Entwicklungsdefekte bei den Milz‑B‑Zell‑Untergruppen. Funktionell zeigten RNF213‑defiziente Mäuse schwächere Antikörperantworten gegen sowohl T‑unabhängige Antigene (die überwiegend auf die schnelle Reaktion marginaler Zellen angewiesen sind) als auch T‑abhängige Antigene (die Keimzentren und Gedächtniszellen erfordern). Menge und Qualität der Antikörper — besonders hochaffine IgG1‑Antikörper — waren beeinträchtigt, was die Bedeutung von RNF213 für eine effektive humorale Immunität unterstreicht.
Warum das für Gesundheit und Krankheit wichtig ist
Für einen Nicht‑Spezialisten zeigt diese Arbeit, wie ein einziges interferon‑induzierbares Protein, RNF213, frühe Immunalarme mit den tiefen inneren Abläufen von B‑Zellen verknüpfen kann: ihre Genprogramme, die Treibstoffversorgung und die Fähigkeit, schützende Antikörper zu bilden. Indem es den Abbau von SPIB abstimmt und die PIK3C3–PI3P–PTEN‑Bremse auf die AKT–mTOR‑Signalgebung begrenzt, hilft RNF213 B‑Zellen, sich korrekt zu entwickeln und kraftvoll auf Infektionen zu reagieren. Da RNF213 auch ein wichtiger genetischer Risikofaktor für die Moyamoya‑Krankheit ist, deuten diese Befunde darauf hin, dass Störungen dieses Pfads Gefäßanomalien mit subtilen immunologischen und metabolischen Ungleichgewichten verbinden könnten.
Zitation: Zhang, Z., Xiang, N., Liu, Q. et al. Ring finger protein 213 regulates B-cell receptor signaling, metabolism, and development in B lymphocytes. Sig Transduct Target Ther 11, 59 (2026). https://doi.org/10.1038/s41392-026-02575-x
Schlüsselwörter: B‑Zellen, RNF213, Antikörperantworten, Immunstoffwechsel, AKT‑mTOR‑Signalgebung