Clear Sky Science · de
Molekularer Mechanismus der cholesterinabhängigen Membranfusion beim Eindringen von SARS-CoV-2
Warum Cholesterin für ein Atemwegsvirus wichtig ist
Das Virus, das COVID-19 verursacht, SARS-CoV-2, gelangt in unsere Zellen, indem es seine Außenhülle mit den Zellmembranen verschmelzen lässt. Dieses Paper stellt eine auf den ersten Blick einfache, aber weitreichende Frage: Wie stark beeinflusst Cholesterin — eine fettartige Substanz, die man eher von Herzerkrankungen kennt — diesen Fusionsschritt? Die Autoren zeigen, dass Cholesterin in der viralen Membran die Infektion nicht nur leicht moduliert; es organisiert die Spike-Proteine des Virus tatsächlich zu leistungsfähigen Andockplattformen, die das Eindringen erleichtern und verlässlicher machen.
Aufbau eines minimalen Modells des Virus-Eintritts
Um diesen Prozess zu zerlegen, rekonstruierten die Forschenden die Begegnung zwischen Virus und Zelle im Reagenzglas mit winzigen Fettbläschen, so genannten Liposomen. Eine Gruppe von Liposomen trug das SARS-CoV-2-Spike-Protein und stand für die virale Membran; die andere trug den ACE2-Rezeptor und ahmte die Wirtszelloberfläche nach. Beim Mischen und Aktivieren durch spezifische Enzyme, die das Spike in seine fusionsbereite Form „aufschneiden“, verschmolzen diese künstlichen Membranen und ermöglichten, dass ein fluoreszierender Farbstoff von einer Blase zur anderen überging. Dieses reduzierte System erlaubte es dem Team, die Lipidzusammensetzung — einschließlich der Cholesterinwerte — auf beiden Seiten präzise einzustellen und die Fusionsabläufe Schritt für Schritt zu beobachten. 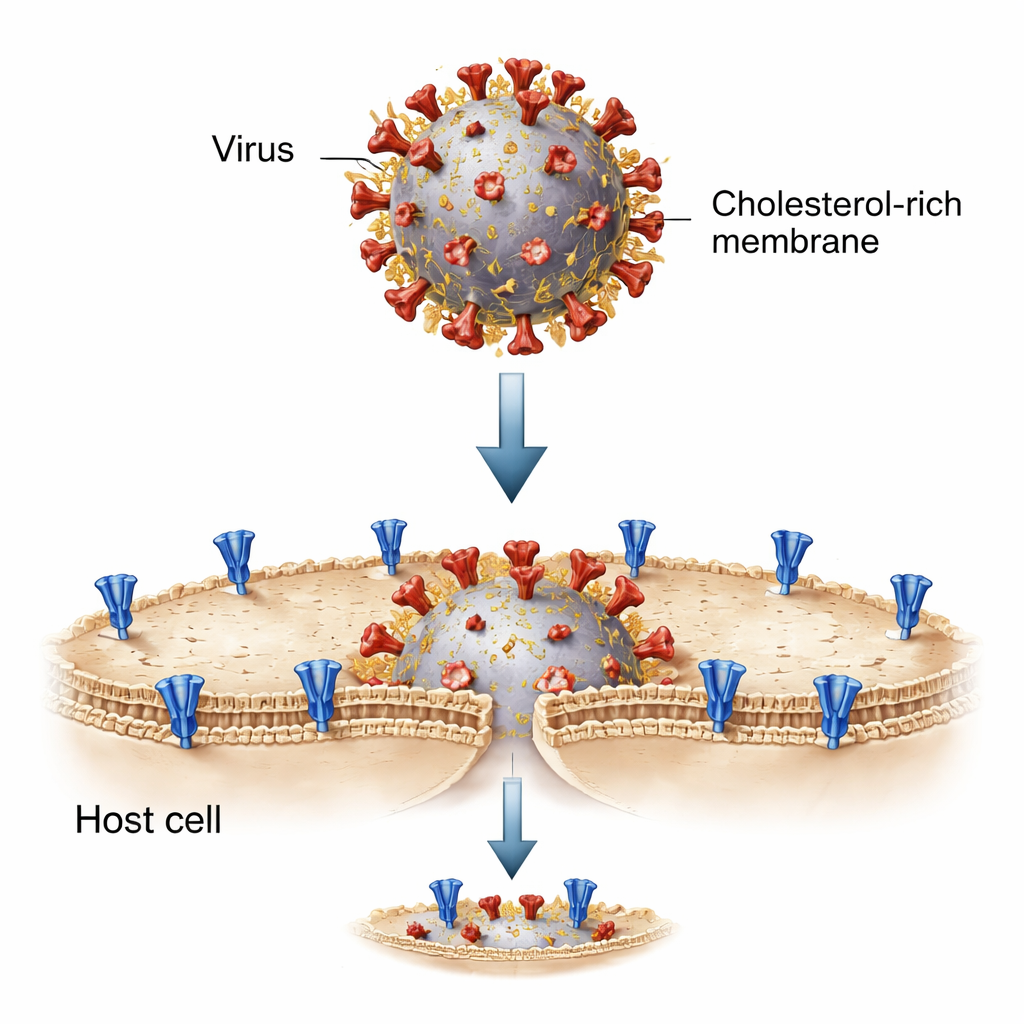
Cholesterin fördert Andocken stärker als Fusion
Durch Variieren des Cholesterins stellten die Forschenden fest, dass das Hinzufügen von Cholesterin zur Spike-tragenden Membran die Fusion häufiger machte, aber nicht auf die erwartete Weise. Hoher Cholesterinspiegel veränderte nicht dramatisch die Wahrscheinlichkeit, dass zwei bereits aneinanderhaftende Membranen tatsächlich verschmelzen. Stattdessen erhöhte es deutlich, wie oft Spike-belegte Vesikel zunächst an ACE2-belegte Vesikel andockten. Einzelpartikel-Imaging zeigte deutlich mehr erfolgreiche Andockereignisse, wenn Spike in cholesterinreichen Membranen saß, während die Wahrscheinlichkeit, dass ein angedocktes Paar anschließend vollständig verschmilzt, ungefähr konstant blieb. Interessanterweise brachte Cholesterin auf der ACE2-Seite kaum Vorteile und hemmte bei sehr hohen Konzentrationen die Fusion sogar, was darauf hindeutet, dass das virale — und nicht das Wirts‑ — Cholesterin der Haupttreiber ist.
Vom Modell zur lebenden Zelle
Die Forschenden prüften dann, ob dasselbe Muster auch in lebenden Zellen gilt. Sie konstruierten menschliche Zellen so, dass sie entweder Spike oder ACE2 exprimierten, und beobachteten, wie sich nach dem Mischen große verschmolzene Strukturen, sogenannte Synzytien, bildeten. Die Entfernung von Cholesterin aus Spike-exprimierenden Zellen beseitigte nahezu die Bildung von Synzytien, während die Wiederherstellung von Cholesterin die Fusion rettete. In parallelen Experimenten mit SARS-CoV-2‑„Pseudoviren“ (harmlosen Partikeln, die das Coronavirus‑Spike zum Eintritt in Zellen verwenden) reduzierte das Entfernen von Cholesterin aus der viralen Membran die Infektion stark, und das Wiederauffüllen steigerte die Infektion dosisabhängig. Im Gegensatz dazu verursachten Veränderungen des Cholesterins allein auf ACE2-exprimierenden Zellen kaum Änderungen. Über alle Tests hinweg war die Botschaft klar: Cholesterin in der Spike-haltigen Membran ist wesentlich für einen effizienten Eintritt.
Spike‑Cluster: Cholesterins Geheimwaffe
Warum sollte Cholesterin auf der viralen Seite so wichtig sein? Hochauflösende Bildgebung von Zellmembranen zeigte, dass Spike-Proteine bei reichlich Cholesterin dazu neigen, dichte Cluster zu bilden, während sie bei Cholesterinmangel stärker verteilt bleiben. Einzelmolekülmessungen zeigten weiter, dass diese Cluster unter cholesterinreichen Bedingungen mehr Spike-Kopien enthalten. Die Autoren führten diesen Effekt auf eine cysteïnreiche Region (CRR) am Schwanzende des Spike zurück, innerhalb der viralen Membran. Dieses Segment wird durch Palmitoylierung modifiziert — eine Art fettiger „Anker“, der cholesterolreiche Bereiche bevorzugt. Wenn das Team den Spike-Schwanz kürzte oder alle zehn Cysteine mutierte, um die Palmitoylierung zu verhindern, clusterte Spike nicht mehr mit Cholesterin, und der cholesterinabhängige Zuwachs an Andocken und Fusion verschwand. 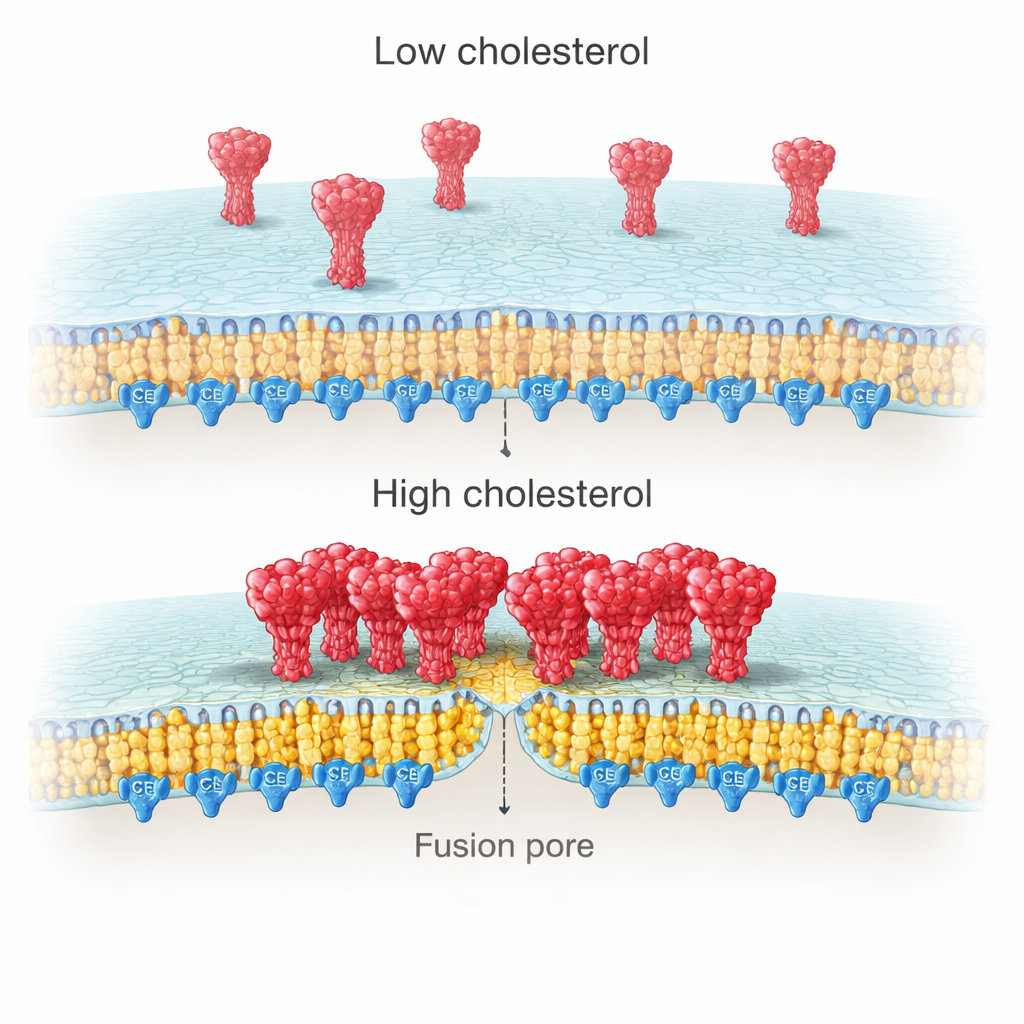
Wie dies künftigen Behandlungen nützen könnte
Kurz gesagt kommt die Studie zu dem Schluss, dass Cholesterin die virale Membran in eine Fusionsplattform verwandelt, indem es viele Spike-Proteine durch ihre palmitoylierte Schwanzregion zu engen Clustern zusammenführt. Diese Cluster docken effizienter an ACE2 auf Wirtszellen an und erhöhen die Wahrscheinlichkeit, dass eine Begegnung zu erfolgreicher Fusion und Infektion führt. Für Nicht‑Spezialisten lautet die wesentliche Erkenntnis: Cholesterin ist kein passiver Bestandteil der viralen Hülle, sondern ein aktiver Organisator der Spike‑Maschinerie. Das macht die cysteïnreiche, cholesterinsensible Schwanzregion des Spike — und die Enzyme, die sie palmitoylieren — zu vielversprechenden Targets für breit wirkende antivirale Strategien, die gegen verschiedene Coronavirus‑Varianten wirksam sein könnten.
Zitation: Li, W., Wu, M., Feng, S. et al. Molecular mechanism of cholesterol-dependent membrane fusion in SARS-CoV-2 entry. Sig Transduct Target Ther 11, 57 (2026). https://doi.org/10.1038/s41392-026-02573-z
Schlüsselwörter: Cholesterin, SARS-CoV-2-Spike, Membranfusion, Virus-Eintritt, Palmitoylierung