Clear Sky Science · de
PKC-eta fördert die Metastasierung von Brustkrebs durch Regulation des Hippo–YAP-Signalwegs
Warum diese Forschung wichtig ist
Triple-negativer Brustkrebs (TNBC) gehört zu den gefährlichsten Formen von Brustkrebs, weil er früh metastasiert und es kaum zielgerichtete Therapien gibt. Diese Studie legt offen, wie ein bestimmtes Enzym in Krebszellen, PKC-eta (PKCη), wie ein Hauptschalter wirkt, der Tumoren dabei hilft, sich zu lösen, durch den Körper zu wandern und neue Tumoren zu begründen. Indem man diesen Schalter versteht, identifizieren die Forschenden außerdem ein kleines, natürliches Peptid, das ihn ausschalten kann — ein Hinweis auf einen potenziell neuen Behandlungsansatz für diese aggressive Erkrankung. 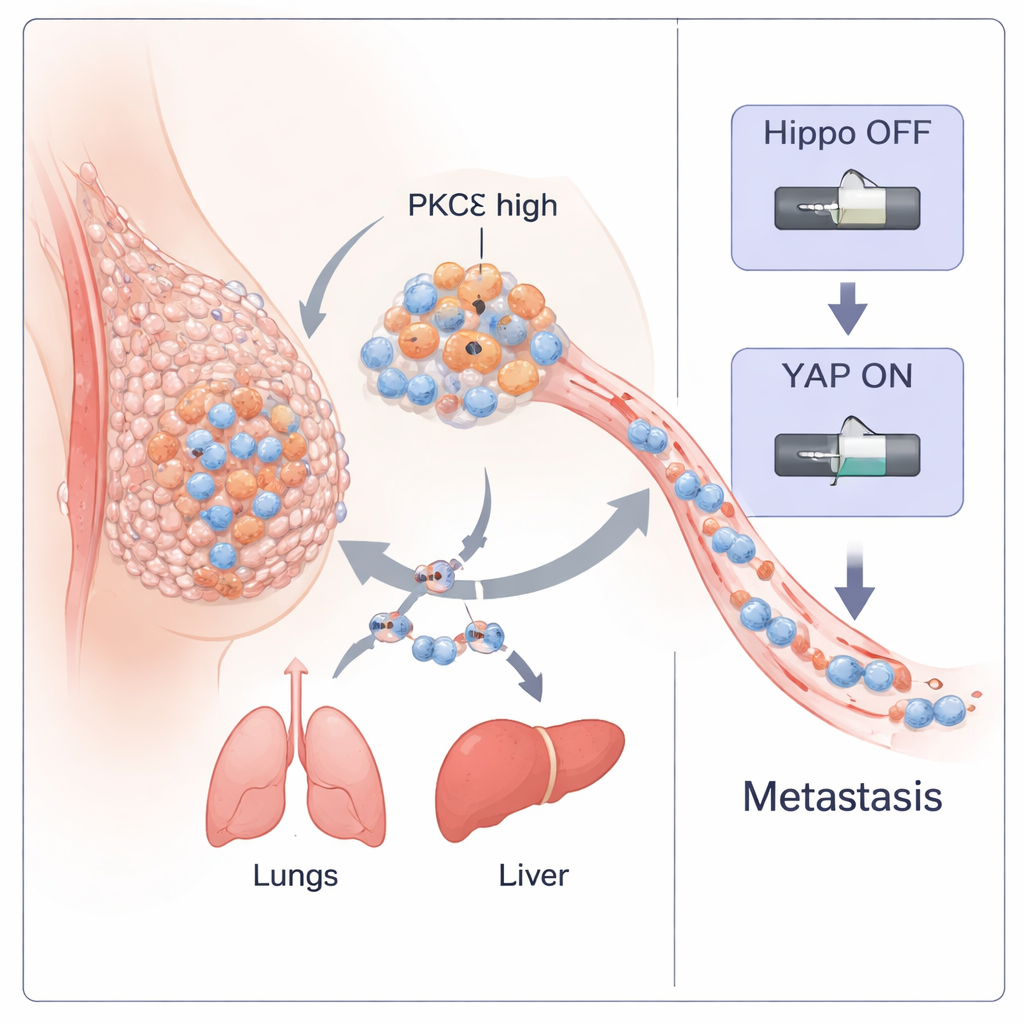
Ein verborgener Treiber in aggressiven Brusttumoren
Das Team begann mit der Analyse großer Datensätze von Brustkrebspatientinnen. Sie fanden heraus, dass das Gen, das PKCη kodiert (PRKCH), besonders hoch in einem Subtyp von Tumoren ist, der als „claudin‑low“ bezeichnet wird — dieser Subtyp überschneidet sich stark mit TNBC und enthält viele stammzellähnliche, hoch mobile Zellen. In mehreren Patientenkohorten zeigten Tumoren mit hohem PRKCH starke Signaturen der epithelial‑mesenchymalen Transition (EMT) — ein Prozess, bei dem vormals geordnete Zellen ihre Verbindungen lockern, ihre Form ändern und invasiver werden. PRKCH-Werte waren auch in metastatischen Proben höher als in den ursprünglichen Primärtumoren, und die Proteinfärbung menschlicher TNBC-Gewebe zeigte mehr aktives, perinukleäres PKCη in höhergradigen, fortgeschrittenen Tumoren. Zusammen deuten diese Befunde darauf hin, dass PKCη eng mit Tumoraggressivität und Ausbreitung verbunden ist.
Von der Zellkultur zur Maus: PKCη treibt die Ausbreitung an
Um Ursache und Wirkung zu prüfen, setzten die Forschenden CRISPR-Geneditierung ein, um PKCη in zwei hoch metastatischen TNBC-Zelllinien zu entfernen — einer Mauslinie (4T1) und einer humanen Linie (MDA‑MB‑231). Ohne PKCη rückten die Zellen in einen näher am Epithel liegenden Zustand: Sie erhöhten Zelladhäsionsproteine wie E‑Cadherin und EpCAM und verringerten klassische mesenchymale Marker wie Vimentin und N‑Cadherin. Diese PKCη-defizienten Zellen bildeten weniger und kleinere Kolonien, migrierten und invasierten weniger effizient, waren beim Verlust von Anhaftung anfälliger für Zelltod und zeigten einen starken Rückgang von Stammzellmerkmalen, darunter weniger CD44high/CD24low- und ALDH-positive Zellen sowie reduzierte sphäroidbildende Kapazität. Nach Injektion in Mäuse bildeten Zellen ohne PKCη kleinere Primärtumoren und deutlich weniger Metastasen in Lunge, Leber, Gehirn und anderen Organen; die Mäuse überlebten zudem länger. Die Wiederherstellung von PKCη kehrte diese Veränderungen um und bestätigte, dass das Enzym aktiv das Fortschreiten und die Ausbreitung von TNBC fördert.
Wie PKCη einen Wachstumsregulationsweg kapert
Die Studie vertiefte sich anschließend in die Mechanismen, durch die PKCη diese prometastatische Wirkung ausübt. Patientendaten zeigten, dass PKCη-Level parallel zu YAP schwanken, einem starken Transkriptionsregulator, der vom Hippo-Weg gesteuert wird — einer zellulären „Sicherheitsbremse“, die normalerweise Wachstum begrenzt. Hohe Werte von PRKCH oder YAP1 sagten schlechtere Patientenergebnisse voraus, und hohe Werte beider Gene zusammen waren mit besonders schlechter fernmetastasierungsfreier Überlebenszeit verbunden. In TNBC-Zellen führte der Verlust von PKCη zu niedrigeren Gesamt-YAP-Leveln und verschob YAP aus dem Zellkern ins Zytoplasma, wo es inaktiv ist. Biochemische Experimente zeigten, dass PKCη physisch an YAP bindet und spezifisch eine Phosphatgruppe an der Ser128-Stelle anfügt. Diese Modifikation stabilisiert YAP und fördert dessen Kernlokalisierung, wo es Gene aktiviert, die EMT, Stammzellmerkmale und Metastasierung antreiben. Fehlt PKCη, wird YAP stattdessen an anderen Stellen (Ser127 und Ser397) phosphoryliert, was die Bindung an 14‑3‑3-Proteine fördert, YAP im Zytoplasma festhält und schließlich dessen Abbau nach sich zieht. PKCη erhöht außerdem PTEN — eine natürliche Bremse auf das AKT-Enzym — und hält dadurch die AKT-Aktivität niedrig, wodurch die upstream liegenden Hippo‑Kinasen unterdrückt werden, die sonst YAP inaktivieren würden. Auf diese Weise aktiviert PKCη YAP sowohl direkt als auch indirekt, indem es die Hippo‑„Bremse“ ausgeschaltet lässt. 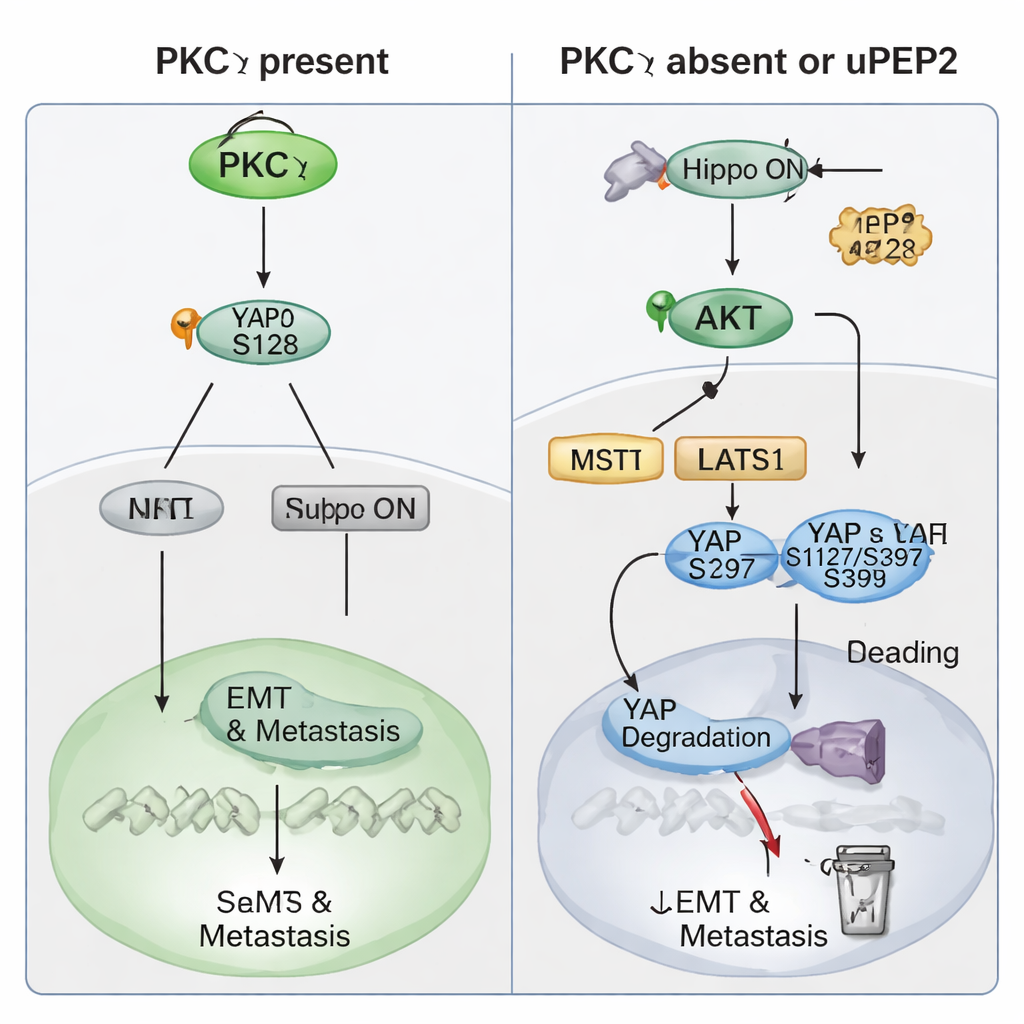
Ein winziges Peptid, das den Krebs-Schalter entschärft
Interessanterweise enthält das PKCη-Gen eine kurze upstream open reading frame (uORF), die ein Mikropeptid namens uPEP2 kodiert. Frühere Arbeiten zeigten, dass uPEP2 an PKCη und verwandte Enzyme binden und diese hemmen kann. Hier ahmte die Behandlung von TNBC-Zellen mit synthetischem uPEP2 die Effekte eines PKCη-Knocks aus: Migration, Invasion und stammzellähnliches Verhalten nahmen ab, EMT-Marker verschoben sich zu einem weniger aggressiven Profil, und YAP-Level fielen, während seine „aus“-Phosphorylierungsmarken zunahmen. In Mausmodellen reduzierten uPEP2 die PKCη- und YAP-Spiegel in Primärtumoren, verstärkten die YAP-Inaktivierung und gingen mit weniger Mikrometastasen in Leber und Lunge einher. Mechanistisch fördert uPEP2 den Abbau von PKCη, schaltet den Hippo-Weg wieder ein und treibt YAP in Richtung zytoplasmatischer Retention und Abbau.
Was das für künftige Therapien bedeutet
Für nichtwissenschaftliche Leser ist die Kernbotschaft: Die Forschenden haben PKCη als Schlüsselfaktor identifiziert, der den aggressivsten Brustkrebsformen ermöglicht, sich zu lösen, zu wandern und ferne Organe zu besiedeln, indem er ein natürliches Wachstums-Kontrollsystem deaktiviert und den YAP‑„Gashebel“ aktiviert. Durch das Entfernen von PKCη oder die Verwendung des kleinen natürlichen Peptids uPEP2, das PKCη abbaut, konnten sie die Hippo-Sicherheitsbremse wiederherstellen, YAP dämpfen und in präklinischen Modellen die Metastasierung deutlich reduzieren. Obwohl diese Arbeit noch experimentell ist und in Zelllinien sowie in immunsupprimierten Mäusen durchgeführt wurde, hebt sie PKCη und seine Wechselwirkung mit YAP als vielversprechende Ziele für neue TNBC-Therapien hervor und legt nahe, dass uPEP2-ähnliche Wirkstoffe eines Tages helfen könnten, die Ausbreitung dieses schwer zu behandelnden Krebses zu verhindern oder zu begrenzen.
Zitation: Liju, V.B., Waidha, K., Muraleedharan, A. et al. PKC-eta promotes breast cancer metastasis by regulating the Hippo–YAP signaling pathway. Sig Transduct Target Ther 11, 58 (2026). https://doi.org/10.1038/s41392-026-02572-0
Schlüsselwörter: triple-negativer Brustkrebs, PKC-eta, Hippo-YAP-Signalweg, epithelial-mesenchymale Transition, Krebsmetastasen