Clear Sky Science · de
Serpina3c schützt vor stoffwechselbedingt-assoziierter steatotischer Lebererkrankung bei Nachkommen, ausgelöst durch pränatale Prednison‑Exposition
Warum diese Forschung für künftige Kinder wichtig ist
Viele Frauen benötigen während der Schwangerschaft Prednison, um schwere Autoimmun‑ und Entzündungserkrankungen zu kontrollieren. Ärztinnen und Ärzte wissen, dass es für die Mütter lebensrettend sein kann, doch weitaus weniger ist darüber bekannt, wie es die langfristige Gesundheit ihrer Kinder beeinflusst. Diese Studie stellt eine drängende Frage: Kann die Einnahme von Prednison in der Schwangerschaft leise die Leber eines Kindes so prädisponieren, dass später im Leben eine Fettlebererkrankung entsteht, besonders in Kombination mit einer ungesunden Ernährung? Und falls ja, gibt es Wege, dieses Risiko umzukehren?
Ein weltweit wachsendes Leberproblem
Die metabolic dysfunction-associated steatotic liver disease (MASLD) ist inzwischen eine der häufigsten chronischen Lebererkrankungen, von der etwa ein Drittel der Weltbevölkerung betroffen ist und deren Häufigkeit weiter steigen dürfte. Sie umfasst einfache Fetteinlagerung in der Leber, entzündliche „fettleberbedingte Hepatitis“, Vernarbung, Zirrhose und sogar Leberkrebs. MASLD steht in engem Zusammenhang mit Adipositas, Bluthochdruck und Typ‑2‑Diabetes. Zunehmend erkennen Wissenschaftler, dass die Grundlagen dieser Krankheit schon vor der Geburt gelegt werden können, wenn der sich entwickelnde Fötus Stressfaktoren wie mangelhafte Ernährung, Umweltverschmutzung oder Medikamente ausgesetzt ist. Diese Idee — dass frühe Lebensumstände das lebenslange Krankheitsrisiko prägen — ist als «developmental origins of health and disease» bekannt. 
Prednison vor der Geburt als erster Schlag
Um zu untersuchen, wie pränatales Prednison die Leber beeinflusst, behandelten die Forschenden schwangere Ratten und Mäuse mit Dosen, die so gewählt waren, dass sie niedrigen klinischen Dosen beim Menschen ähneln. Die Nachkommen wurden dann vor der Geburt und bis ins junge Erwachsenenalter verfolgt. Alleinstehend waren die im Uterus Prednison‑ausgesetzten Jungtiere kleiner und zeigten bereits Anzeichen einer gestörten Fettverarbeitung in der Leber: mehr Fetttröpfchen, höhere Lebertriglyzeride und eine schwächere Nutzung von Fetten zur Energiegewinnung. Während die Nachkommen wuchsen, speicherten ihre Lebern selbst bei normaler Ernährung weiterhin mehr Fett als üblich. Wurden die Tiere später mit einer fettreichen Diät konfrontiert — dem Äquivalent zu einem westlichen Fast‑Food‑Muster —, wurden die Unterschiede dramatisch. Prednison‑exponierte Nachkommen entwickelten schwerere Fettleber, Entzündungen und bei Männchen deutliche Anzeichen von Vernarbung. Auch ihre Blutzuckerregulation verschlechterte sich, was auf breitere metabolische Probleme hindeutet.
Ein schützendes Leberprotein verschwindet
Tiefere Analysen mittels großangelegter Genprofilierung suchten nach gemeinsamen molekularen Veränderungen in den Lebern männlicher und weiblicher Nachkommen. Ein Gen stach hervor: Serpina3c, das ein sezerniertes Protein aus einer Familie natürlicher Enzymhemmer produziert. In beiden Geschlechtern senkte pränatales Prednison Serpina3c in der Leber und im Blut deutlich und anhaltend, von der späten Fetalzeit bis ins Erwachsenenalter. Als die Forschenden Serpina3c gezielt nur in der Leber gesunder Mäuse reduzierten, wurden auch diese Tiere anfällig für Fettleber und gestörte Zuckerregulation, insbesondere bei fettreicher Ernährung. Umgekehrt führte eine Erhöhung von Serpina3c in den Lebern der prednison‑exponierten Nachkommen nach der Geburt weitgehend zur Erholung: Ihre Lebern speicherten weniger Fett, der Glukosestoffwechsel verbesserte sich und Entzündung sowie Vernarbung nahmen ab.
Wie Prednison die Schaltkreise der Leber umprogrammiert
Die Forschenden fragten als Nächstes, wie pränatales Prednison Serpina3c herunterreguliert. Sie fanden heraus, dass die aktive Form von Prednison, Prednisolon, den Glukokortikoidrezeptor — ein drugsensitives Protein in Leberzellen — übermäßig aktiviert. Dieser Rezeptor arbeitet dann mit einem anderen Protein, HDAC3, zusammen, das die DNA‑Verpackung verschärft, indem es kleine „Acetyl“‑Marken von Histonproteinen entfernt. Sowohl in Tierlebern als auch in kultivierten Leberzellen erhöhte Prednisolon die Aktivität von Glukokortikoidrezeptor und HDAC3 direkt am Serpina3c‑Gen und entfernte Acetylmarken an einer Schlüsselstelle, genannt H3K27. Mit dem Verlust dieser Markierungen fiel die Genaktivität und die Serpina3c‑Proteinspiegel sanken. Das Blockieren des Rezeptors oder von HDAC3 bzw. die Hemmung der Deacetylierung stellte diese Acetylmarken wieder her, hob Serpina3c an und verbesserte Fett‑ und Zuckerstoffwechsel in Leberzellen.
Eine schädliche Kettenreaktion in der Leber
Niedrige Serpina3c‑Werte lösten eine zweite schädliche Kaskade aus. Unter normalen Bedingungen hilft Serpina3c, Enzyme wie Chymase zu dämpfen, die das Hormon Angiotensin II direkt im Gewebe erzeugen. Bei Serpina3c‑Mangel stiegen Chymase‑Spiegel und -Aktivität, wodurch mehr Angiotensin II in der Leber produziert wurde und dessen Rezeptor AT1R auf Leberzellen überaktiviert wurde. Dieser lokale Hormonanstieg treibt bekanntermaßen oxidativen Stress, Insulinresistenz, Fettspeicherung, Entzündung und Narbenbildung voran. Sowohl bei prednison‑exponierten Tieren als auch bei Mäusen mit leberspezifischem Serpina3c‑Downregulation war der Chymase–Angiotensin‑II–AT1R‑Weg aktiviert, und Schlüsselgene, die normalerweise Fettverbrennung und Glukoseaufnahme unterstützen, wurden unterdrückt. Die Wiederherstellung von Serpina3c nach der Geburt dämpfte diesen Pfad und belebte einen gesünderen Stoffwechsel. 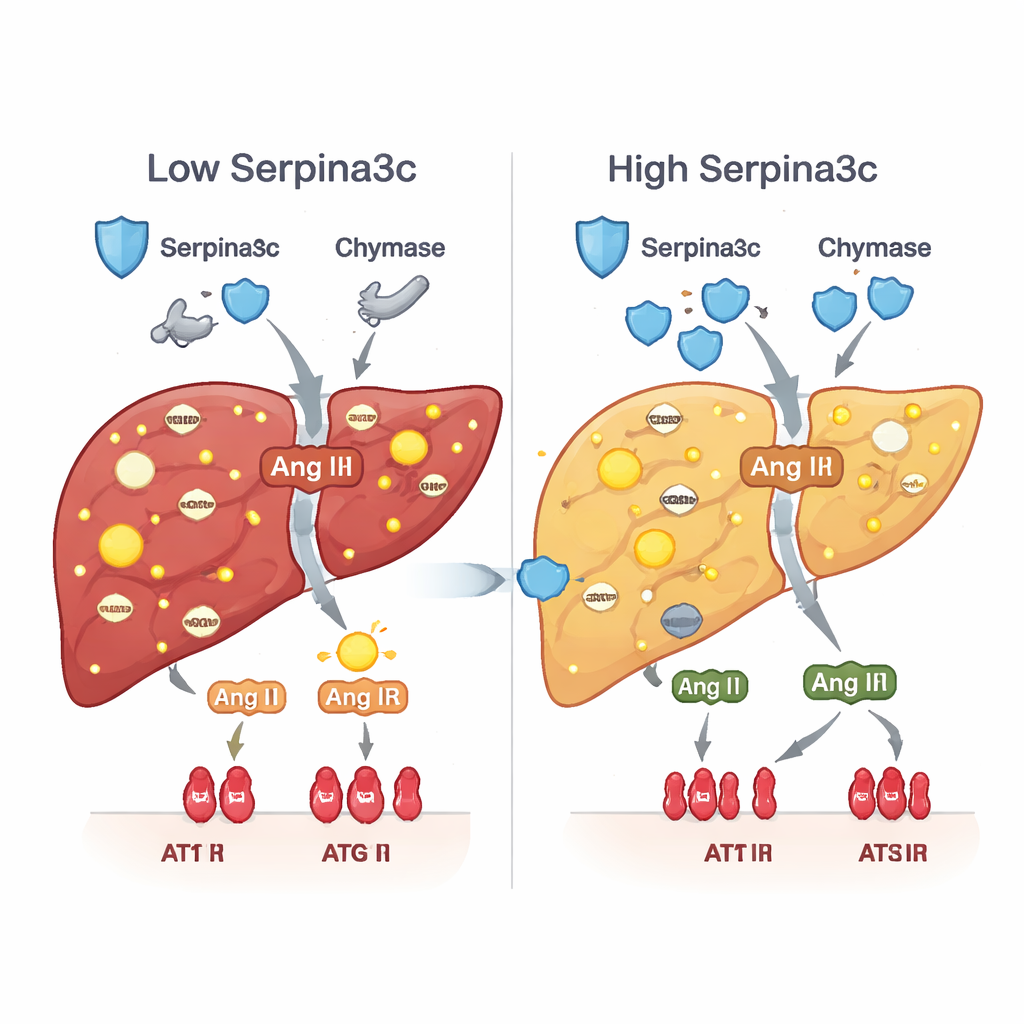
Was das für Patienten und Familien bedeutet
Für Nicht‑Fachleute lautet die Kernbotschaft, dass während der Schwangerschaft eingenommene Medikamente einen molekularen Fingerabdruck in der sich entwickelnden Leber hinterlassen können, der bis ins Erwachsenenalter anhält. In dieser Studie fungierte Prednison als „erster Schlag“, indem es ein schützendes Protein (Serpina3c) durch epigenetische Veränderungen — chemische Markierungen an DNA‑verpackenden Proteinen — senkte, sodass ein späterer „zweiter Schlag“ wie eine fettreiche Ernährung leichter eine Fettlebererkrankung auslösen konnte. Die ermutigende Kehrseite ist, dass dieses Risiko nicht unumkehrbar schien: Eine nachgeburtliche Wiederanhebung von Serpina3c in der Leber verringerte die Leberschädigung deutlich. Auch wenn diese Ergebnisse aus Nagetiermodellen stammen, werfen sie wichtige Fragen dafür auf, wie wir Kinder überwachen und unterstützen sollten, deren Mütter während der Schwangerschaft Prednison benötigten, und sie machen Serpina3c sowie das Chymase–Angiotensin‑II‑System zu vielversprechenden Zielstrukturen, um eine vorgeburtlich beginnende Fettlebererkrankung künftig zu verhindern oder zu behandeln.
Zitation: Dai, Y., Lu, Z., Peng, Y. et al. Serpina3c protects against metabolic dysfunction-associated steatotic liver disease in offspring induced by prenatal prednisone exposure. Sig Transduct Target Ther 11, 71 (2026). https://doi.org/10.1038/s41392-025-02569-1
Schlüsselwörter: pränatales Prednison, Fettlebererkrankung, Epigenetik, Serpina3c, Entwicklungsursprünge