Clear Sky Science · de
Arthrose: molekulare Pathogenese und mögliche Therapieoptionen
Wenn Alltägliche Gelenkschmerzen Zur Ganzkörpergeschichte Werden
Schmerzende Knie oder steife Finger werden oft als unvermeidbarer Teil des Alterns abgetan. Doch Arthrose – die weltweit häufigste Gelenkerkrankung – ist nicht nur „Verschleiß“. Dieser Übersichtsartikel zieht den Vorhang zurück und zeigt, was in schmerzenden Gelenken wirklich passiert, von fehlgeleiteten Schmerznerven bis zu überlasteten Zellmaschinen, und beleuchtet eine neue Generation von Therapien, die weit über einfache Schmerzmittel hinausgehen.
Eine Häufige Krankheit mit Hohem Persönlichem Preis
Arthrose betrifft fast 8 % der Weltbevölkerung; Hundertmillionen Menschen leben mit chronischen Schmerzen und eingeschränkter Mobilität. Die Erkrankung trifft häufiger Frauen, Menschen über 55 sowie Personen mit Übergewicht oder solche, deren Arbeit oder Sportarten wiederholt starke Belastungen auf die Gelenke ausüben. Die heutige Standardversorgung – Bewegung, Gewichtsreduktion, Orthesen, entzündungshemmende Tabletten, Gelenkinjektionen und in schweren Fällen Gelenkprothesen – kann die Symptome lindern, stoppt die Erkrankung jedoch nur selten. Diese Lücke zwischen Bedarf und verfügbaren Therapien hat Forscher dazu veranlasst, viel tiefer zu untersuchen, wie Arthrose beginnt und warum sie so schmerzhaft ist.
Warum Das Gelenk Schmerzt: Leitungen, Chemie und Signale
Schmerzen bei Arthrose lassen sich nicht allein durch Röntgenbilder erklären: Manche Menschen mit moderaten Schäden haben starke Schmerzen, während andere mit schweren Veränderungen kaum Beschwerden berichten. Der Artikel verfolgt den Schmerz vom Kniegelenk über das Rückenmark bis ins Gehirn. Nervenendigungen im Gelenk – insbesondere dünne Aδ- und C-Fasern – liegen in einem Gemisch aus entzündlichen Botenstoffen wie Interleukinen und Tumornekrosefaktor sowie Nervenwachstumsfaktor. Diese Substanzen schalten spezielle Kanäle in den Nervenendigungen ein, die Natrium und Calcium passieren lassen, wodurch die Nerven leichter und häufiger feuern. Mit der Zeit können Schmerzbahnen im Rückenmark und im Gehirn überempfindlich werden, sodass normale Bewegung oder leichte Kälte als scharf und brennend empfunden wird.
Die Verborgene Arbeitslast in Gelenkzellen
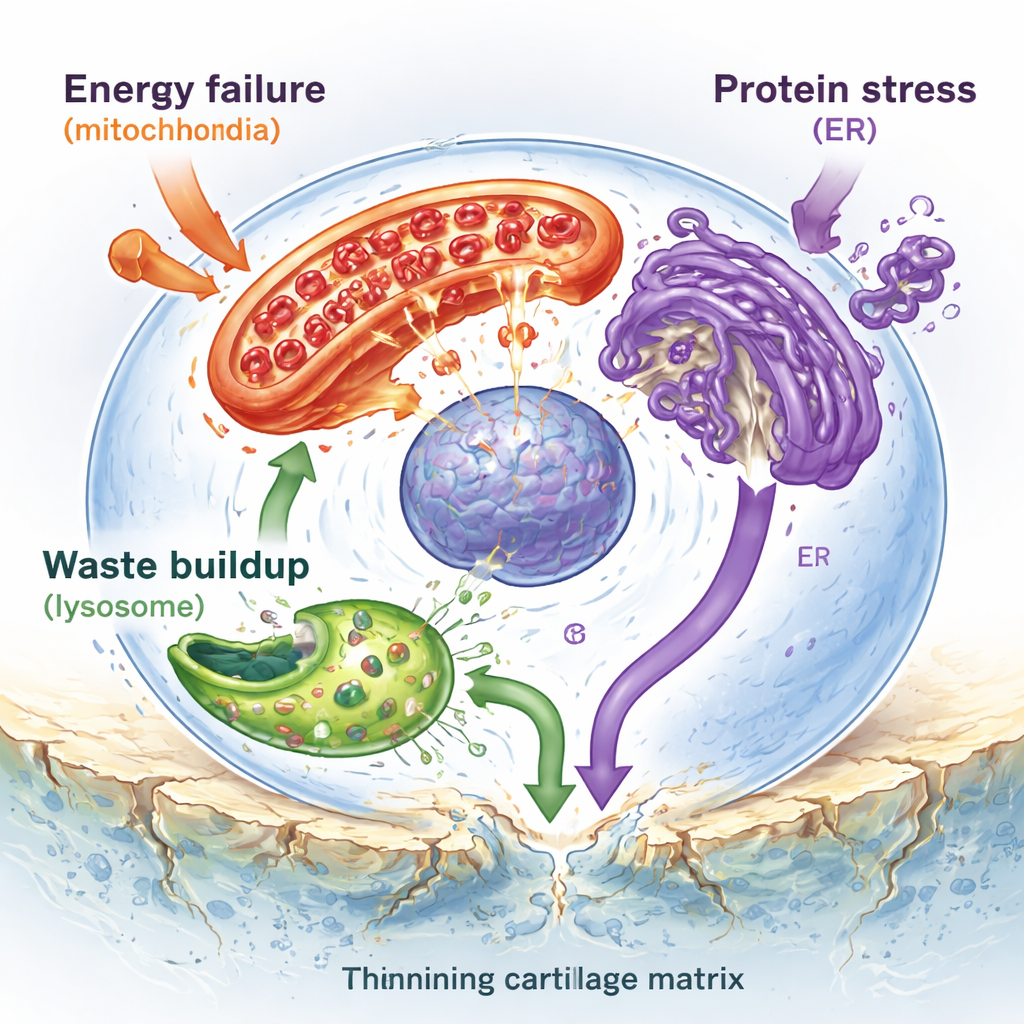
Tief im Knorpel versuchen die einzigen dort ansässigen Zellen – die Chondrozyten – eine glatte, elastische Matrix zu erhalten, die das Gleiten der Knochen ermöglicht. Die Autoren zeigen, dass diese Zellen von mehreren Seiten unter Beschuss stehen. Mitochondrien, die kleinen Kraftwerke der Zelle, werden beschädigt und ineffizient, produzieren zu wenig Energie und gleichzeitig zu viele reaktive Sauerstoffspezies, die DNA und Proteine schädigen. Lysosomen, die Recyclingzentren der Zelle, werden durch harte Mineralsalze überlastet, wodurch ihre Membranen geschwächt werden und zerstörerische Enzyme in die Zelle gelangen, was Zelltod auslösen kann. Das endoplasmatische Retikulum, ein Membrannetzwerk, in dem neue Proteine gefaltet werden, verstopft mit fehlgefalteten Molekülen und löst eine chronische Stressantwort aus, die Zellen schließlich in den Selbstzerstörungsmodus drängt. Gemeinsam treiben diese belasteten Organellen Entzündung an und beschleunigen den Verlust und die Verkalkung des Knorpels.
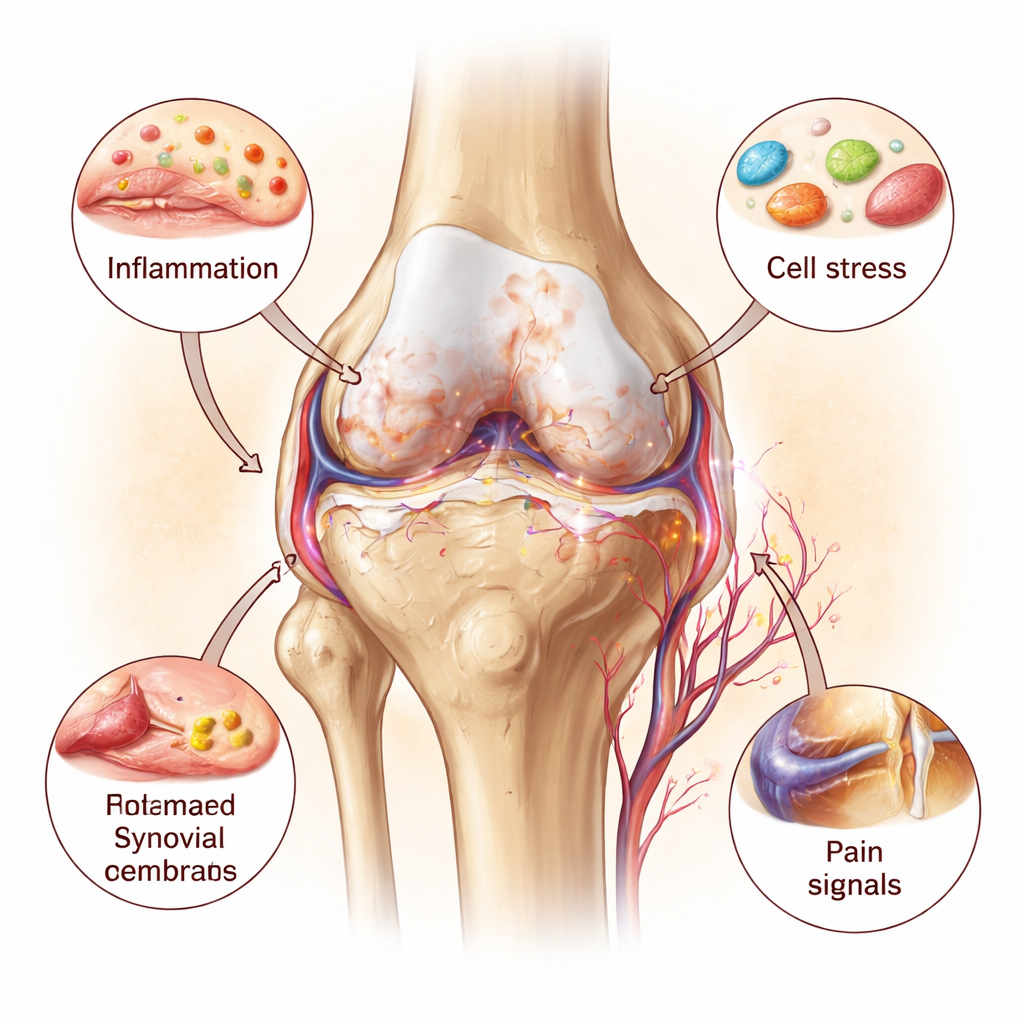
Entzündung: Brennstoff für das Feuer
Entzündliche Botenmoleküle sind die Lautsprecher dieses Prozesses. Drei davon – Interleukin‑1, Interleukin‑6 und Tumornekrosefaktor‑alpha – bilden einen Teufelskreis mit Organellschäden. Sie veranlassen Chondrozyten dazu, Enzyme zu produzieren, die Knorpel abbauen, und fördern abnormales Knochenwachstum unter der Gelenkfläche. Gleichzeitig setzen verletzte Mitochondrien und undichte Lysosomen eigene Warnsignale frei, die weitere Immunsensoren im Gelenk aktivieren. Blutgefäße und Schmerzfasern wachsen in Bereiche des Knorpels ein, die normalerweise still und nervenfrei sind, was die Schmerzempfindlichkeit erhöht. Diese Betrachtung des gesamten Gelenks zeichnet Arthrose als langsam voranschreitende, sich selbst verstärkende entzündliche Erkrankung, nicht als passives, mechanisches Ausfransen des Knorpels.
Neue Therapieideen: Von Ionenkanälen bis zu Zellkraftwerken
Ausgestattet mit dieser mechanistischen Landkarte testen Forscher neue Wirkstoffe und Abgabesysteme. Auf der Schmerzbekämpfungsseite blockieren experimentelle Substanzen oder desensibilisieren sanft Nervenkanäle wie TRPV1 (der Capsaicin‑Rezeptor), TRPA1, TRPM3/8 und spezifische Natriumkanäle (Nav1.7 und Nav1.8), oder sie neutralisieren den Nervenwachstumsfaktor, um eine Überempfindlichkeit der Nerven zu verhindern. Auf der krankheitsmodifizierenden Seite zielen gezielte Antikörper darauf ab, zentrale entzündliche Zytokine herunterzuregeln, während kleine Moleküle und „Senolytika“ versuchen, ein gesünderes Zellverhalten wiederherzustellen. Eine besonders spannende Grenze ist die organellgerichtete Therapie: Verbindungen, die die mitochondriale Reinigung (Mitophagie) ankurbeln, die lysosomale Säurestabilität und Membranen stabilisieren oder den Stress des endoplasmatischen Retikulums vermindern. Ausgereifte Nanopartikel, Liposomen und gentechnisch veränderte Exosomen werden entwickelt, um gezielt Knorpelzellen und sogar spezifische Organellen anzusteuern und Wirkstoffe genau dorthin zu liefern, wo sie gebraucht werden.
Was Das Für Menschen mit Arthrose Bedeutet
Der Artikel kommt zu dem Schluss, dass Arthrose als komplexe biologische Störung zu betrachten und zu behandeln ist, die gestörten Zellstoffwechsel, chronische Niedriggradentzündung und fehlangepasste Schmerzwahrnehmung umfasst. Viele der vorgeschlagenen Medikamente und Abgabesysteme befinden sich noch in frühen Labor‑ oder Tierversuchen, doch sie deuten auf eine Zukunft hin, in der die Therapie multimodal und personalisiert sein wird: Schmerzen werden durch Beruhigung überaktiver Nerven gelindert, während gleichzeitig die eigenen Zellen des Gelenks und ihre interne Maschinerie geschützt oder verjüngt werden. Für Patienten könnte dies schließlich Therapien bedeuten, die Bewegung nicht nur weniger schmerzhaft machen, sondern auch die strukturellen Schäden verlangsamen oder möglicherweise rückgängig machen, die heute oft als unvermeidlich gelten.
Zitation: Zhang, Y., Han, Y., Sun, Y. et al. Osteoarthritis: molecular pathogenesis and potential therapeutic options. Sig Transduct Target Ther 11, 81 (2026). https://doi.org/10.1038/s41392-025-02556-6
Schlüsselwörter: Arthrose, Gelenkschmerzen, Knorpel, Entzündung, Mitochondrien