Clear Sky Science · de
Phototherapiesysteme auf Nanopartikelbasis: molekulare Mechanismen und klinische Anwendungen
Licht als sanftes medizinisches Werkzeug
Die meisten von uns sehen Licht vor allem als Mittel zum Sehen, als Wärmequelle für die Haut oder als Energiequelle für Solarmodule. Dieser Übersichtsartikel untersucht eine überraschendere Rolle: die Nutzung sorgfältig abgestimmten Lichts zusammen mit winzigen, konstruierten Partikeln, um Krankheiten von innen heraus zu diagnostizieren und zu behandeln. Die Autorinnen und Autoren beschreiben, wie eine „auf Nanopartikeln basierende Phototherapie“ Schäden gezielt auf Krebszellen konzentrieren, Entzündungen im Herz- und Gelenkbereich dämpfen und sogar dem Gehirn helfen kann, toxische Proteine bei Erkrankungen wie Alzheimer zu entfernen — und dabei größtenteils gesundes Gewebe schont.
Wie winzige Partikel Licht in Medizin verwandeln
Im Zentrum dieses Ansatzes stehen Nanopartikel — Strukturen, die tausendmal kleiner sind als der Durchmesser eines menschlichen Haares —, die Wirkstoffe transportieren, Licht absorbieren und dieses entweder in Wärme oder kurzlebige chemische Reaktionen umwandeln können. Zwei Hauptstrategien dominieren. Bei der photodynamischen Therapie erzeugen lichtaktivierte Moleküle auf oder in den Partikeln reaktive Sauerstoffspezies — energiereiche Formen von Sauerstoff, die nahegelegene Zellbestandteile schädigen. Bei der photothermalen Therapie wandeln andere Partikel, etwa Gold oder schwarzes Phosphor, nahinfrarotes Licht in Wärme um und „garen“ Tumorzellen kurzzeitig von innen. Weil sich das Licht gezielt lenken und die Partikel so gestalten lassen, dass sie sich vorwiegend in krankem Gewebe anreichern, gewinnen Ärztinnen und Ärzte eine räumliche Präzision, die herkömmliche Chemotherapie und Bestrahlung oft vermissen lässt. 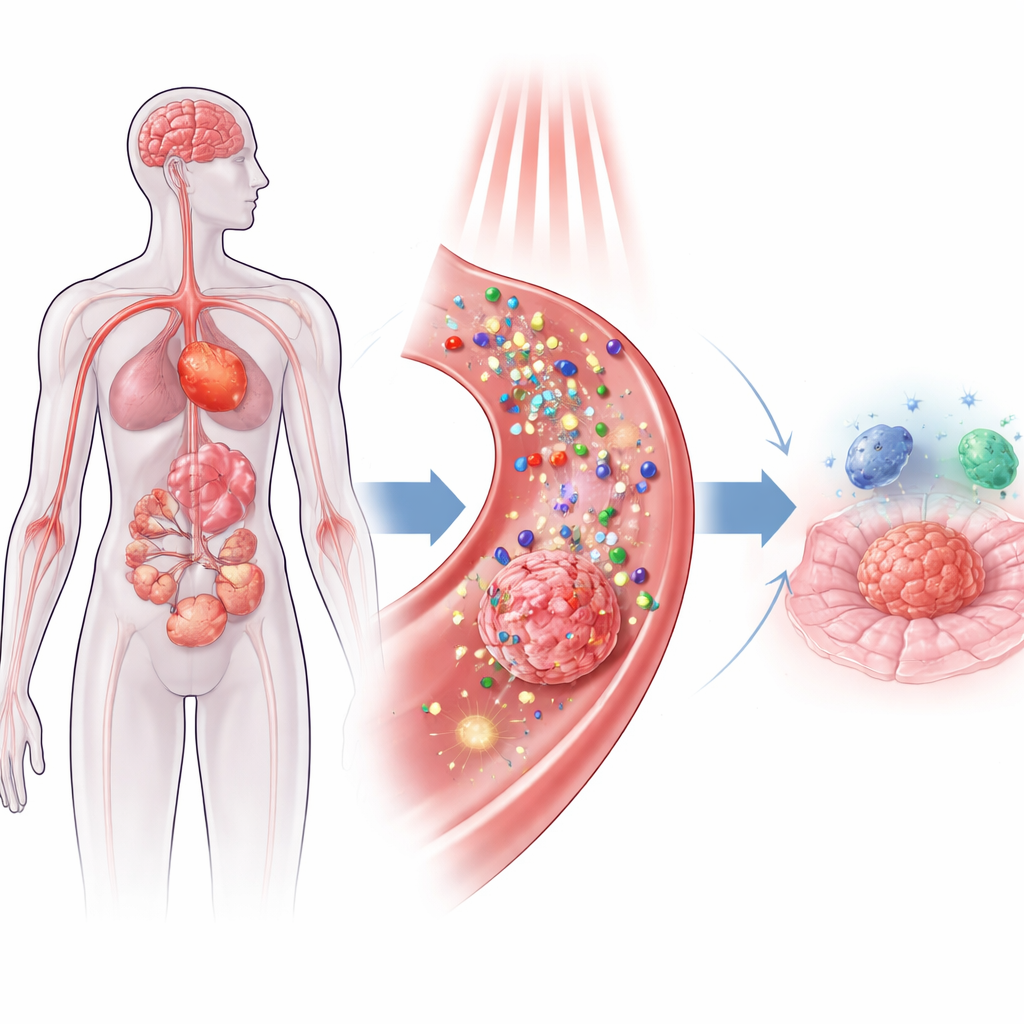
Intelligentere Träger und Lieferwege entwickeln
Einfach Licht auf den Körper zu richten reicht nicht aus; die Herausforderung besteht darin, die richtigen Partikel an den richtigen Ort zu bringen und dort lange genug zu halten, damit sie wirken. Das Review katalogisiert ein Werkzeugset an Liefersystemen, darunter weiche Träger wie Liposomen, feste Lipidpartikel sowie polymerbasierte Kugeln oder Mizellen, ebenso wie starre Gerüste aus Silika, Metallen, Kohlenstoff oder metall-organischen Gerüsten. Ihre Oberflächen können mit Tarnpolymeren beschichtet werden, um die Zirkulationszeit zu verlängern, mit natürlichen Zellmembranen, um Immunabwehr zu entgehen, oder mit „Adressetiketten“, die Marker auf Krebs- oder entzündeten Zellen erkennen. Manche Konstruktionen sind „intelligent“: Sie bleiben im Blut inert, ändern aber Größe, Ladung oder Form als Reaktion auf Azidität, Enzyme oder Redoxbedingungen im Tumor und setzen ihren Inhalt nur dort frei, wo er gebraucht wird.
Was in Zellen passiert, wenn Licht trifft
Sobald das Licht eingeschaltet wird, setzt eine Kaskade molekularer Ereignisse ein. Die Autorinnen und Autoren erklären, wie lichtangeregte Partikel Oxidantien freisetzen, die Membranen, DNA und lebenswichtige Strukturen wie Mitochondrien und Lysosomen angreifen. Dies kann Zellen in einen geordneten Selbstzerstörungsmodus (Apoptose) treiben oder, bei schwerer Schädigung, in chaotischere Formen des Zelltods. Zellen können zudem die Autophagie hochfahren, einen internen Recyclingprozess, der ihnen bei leichtem Stress helfen kann zu überleben oder bei Überforderung ihren Untergang beschleunigt. Entscheidend ist, dass sterbende Tumorzellen „Gefahr“-Signale aussenden können, die das Immunsystem aktivieren: bestimmte Proteine auf ihrer Oberfläche werden exponiert, Faktoren freigesetzt, die dendritische Zellen anziehen, und die tumorassoziierten Immunzellen können von einem unterdrückenden in einen tumorbekämpfenden Zustand umgeformt werden. Effektiv kann eine lokale Lichtbehandlung so zugleich als eine Art personalisierter Krebsimpfstoff wirken. 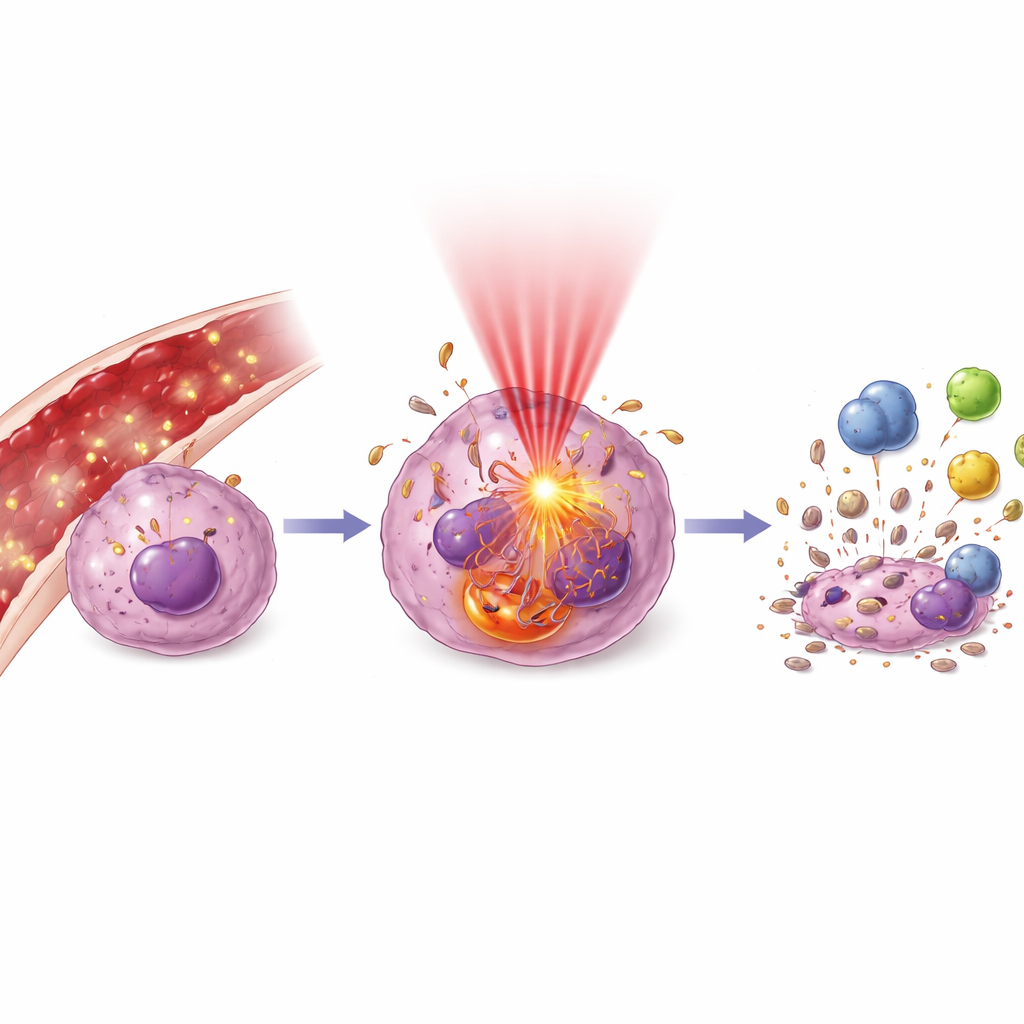
Jenseits von Krebs: Herz, Gehirn und autoimmune Ziele
Während Krebs das am weitesten fortgeschrittene Anwendungsfeld ist, werden dieselben Prinzipien auf chronische Erkrankungen übertragen. In der Kardiologie zielen lichtbasierte Ansätze nicht auf Zellvernichtung, sondern auf die Reduktion von oxidativem Stress, die Stabilisierung von Gefäßwandzellen und sogar auf das Verkleinern oder Verhärten gefährlicher Plaques. Im Gehirn, wo Neurone sehr empfindlich sind, versuchen schonendere Lichtprotokolle — oft als Photobiomodulation bezeichnet — die mitochondriale Energieproduktion zu steigern, toxische Proteinklumpen zu reduzieren und mikroglia- sowie astrozytengetriebene Entzündungen abzuschwächen. Das Review hebt zudem frühe Arbeiten zu metabolischen und autoimmunen Erkrankungen hervor, bei denen dosiertes Licht und Nanopartikel Immunzellen von aggressivem, gewebeschädigendem Verhalten zu regulatorischeren, beruhigenden Rollen umschwenken können, während gleichzeitig die Insulinsensitivität und die Signalgebung im Fettgewebe moderat verbessert werden.
Vom Labor in die Klinik: Versprechen und Hindernisse
Trotz Jahrzehnten der Forschung sind nur wenige lichtaktivierte Arzneimittel vollständig zugelassen, überwiegend für Augenkrankheiten und bestimmte Tumoren. Die Autorinnen und Autoren argumentieren, dass die Nanotechnologie begonnen hat, die nächste Welle zu eröffnen, indem sie tiefere Lichtpenetration, bessere Zielsteuerung und integrierte Bildgebung für die Echtzeitüberwachung der Behandlung ermöglicht. Dennoch bleiben große Hürden: die großtechnische Produktion von Nanopartikeln bei konstanter Qualität, der Nachweis langfristiger Sicherheit und Ausscheidung aus dem Körper, die effektive Lichtzufuhr zu tiefen Organen sowie die Erfüllung strenger regulatorischer Anforderungen. Das Review schließt mit der Feststellung, dass durch die Verbindung von Materialwissenschaft, Optik, Biologie und KI-gestütztem Design die auf Nanopartikeln basierende Phototherapie das Potenzial hat, sich von Nischenverfahren zu einer breiteren, nichtinvasiven Säule der Präzisionsmedizin zu entwickeln.
Zitation: Chauhan, D.S., Prasad, R., Dhanka, M. et al. Nanoparticles-based phototherapy systems: molecular mechanisms and clinical applications. Sig Transduct Target Ther 11, 95 (2026). https://doi.org/10.1038/s41392-025-02536-w
Schlüsselwörter: Nanopartikel-Phototherapie, photothermale Therapie, photodynamische Therapie, Krebsnanomedizin, Photobiomodulation