Clear Sky Science · de
Zytotoxische CD4+-T-Zellen: Ursprung, biologische Funktionen, Krankheiten und therapeutische Zielstrukturen
Wenn Helferzellen zu Killern werden
Das Immunsystem wird oft in einfachen Rollen dargestellt: Einige Zellen erkennen Probleme, andere führen den eigentlichen Kampf. Dieser Artikel konzentriert sich auf eine überraschende Gruppe, die diese Grenze verwischt — zytotoxische CD4-T-Zellen. Lange hauptsächlich als „Helferzellen“ bekannt, die die Abwehr koordinieren, können bestimmte CD4-T-Zellen selbst zu bewaffneten Killern werden. Zu verstehen, wie diese formwandelnden Zellen entstehen, was sie tun und wie sie zu Krankheiten wie Krebs, Virusinfektionen, Autoimmunerkrankungen und Herzerkrankungen beitragen, könnte neue Wege eröffnen, die Immunantwort zu verstärken oder schädliche Entzündungen zu dämpfen. 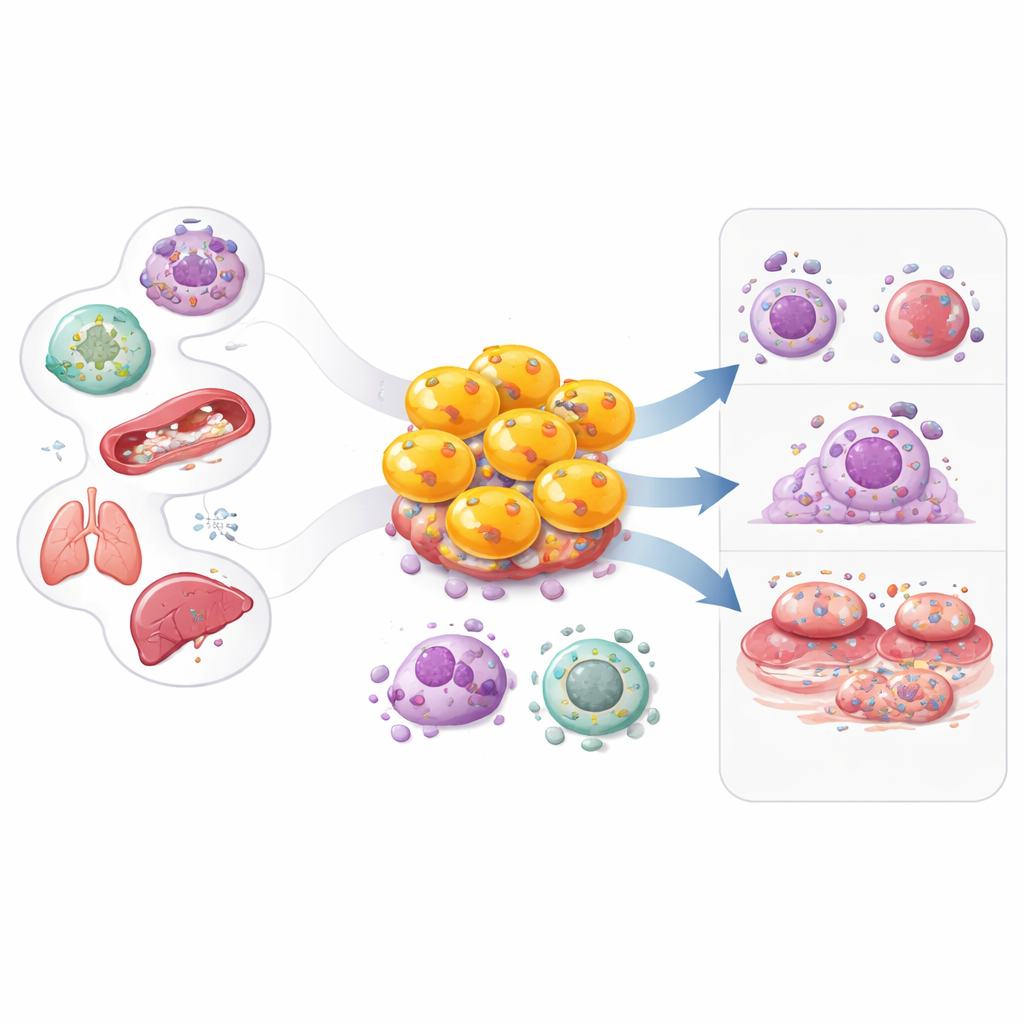
Wie ein flexibler Verteidiger entstand
Frühe Arbeiten in den späten 1970er- und 1980er-Jahren zeigten, dass ein Anteil der CD4-T-Zellen andere Zellen direkt töten kann, wenn diese die richtigen immunologischen Marker zeigen — ähnlich wie klassische zytotoxische CD8-T-Zellen. Zunächst schrieben viele Forschende diese Befunde Laborartefakten zu. In den folgenden Jahrzehnten bestätigten Tiermodelle von Influenza sowie Studien bei Menschen mit Rheumatoider Arthritis, Herzerkrankungen, chronischen Virusinfektionen und Krebs, dass zytotoxische CD4-T-Zellen real und klinisch relevant sind. Moderne Werkzeuge wie Durchflusszytometrie und Einzelzell-RNA-Sequenzierung haben seitdem ihre Vielfalt kartiert und gezeigt, dass diese Zellen bei chronischen Infektionen, Tumoren, im Alter und bei mehreren entzündlichen Erkrankungen expandieren und dort über lange Zeiträume persistieren können.
Woher diese Killer-Helfer kommen
Die Übersichtsarbeit erklärt, dass zytotoxische CD4-T-Zellen wahrscheinlich auf zwei Hauptwegen entstehen. Eine Idee ist, dass sie teilweise natürliche Killerzellen ähneln, weil sie viele gleiche Oberflächenrezeptoren und zytotoxische Moleküle teilen, was auf einen verwandten Entwicklungsweg hindeutet. Zunehmende Belege stützen jedoch eine andere Sicht: Die meisten dieser Zellen beginnen als gewöhnliche Helfer-CD4-T-Zellen — besonders Th1-ähnliche Zellen — die unter chronischer Antigenexposition und starken entzündlichen Signalen in einen terminal differenzierten, zytotoxischen Zustand „umgeschult“ werden. Dieser Wechsel wird von einem Netzwerk äußerer Signale (wie Interleukinen 2, 7 und 15) und innerer Schalter (einschließlich Runx3, T-bet, Eomes, Blimp-1 und Hobit) gesteuert, die gemeinsam Gene für Perforin, Granzyme und todauslösende Liganden einschalten.
Wie sie töten und Entzündungen formen
Funktionell operieren zytotoxische CD4-T-Zellen über zwei Haupangriffswege. Beim Granularweg bilden sie einen engen Kontakt mit einer Zielzelle und setzen Granula frei, die Perforin und Granzym enthalten — diese machen Löcher und lösen programmierte Zellsterblichkeit von innen aus. Beim Weg über Todesliganden präsentieren sie Moleküle wie Fas-Ligand und TRAIL an ihrer Oberfläche und binden passende Rezeptoren auf Zielzellen, um ein internes Selbstmordprogramm zu starten. Über die direkte Tötung hinaus schütten diese Zellen entzündliche Botenstoffe wie Interferon-Gamma, Tumornekrosefaktor und Wachstumsfaktoren aus, die andere Immunzellen anlocken und aktivieren, Blutgefäße umgestalten und das Verhalten des umliegenden Gewebes verändern. Anders als klassische Helferzellen sind sie häufig resistent gegenüber normalen „Bremsen“ wie regulatorischen T-Zellen und sind weniger anfällig für Apoptose, sodass sie sich bei chronischen Erkrankungen ansammeln können. 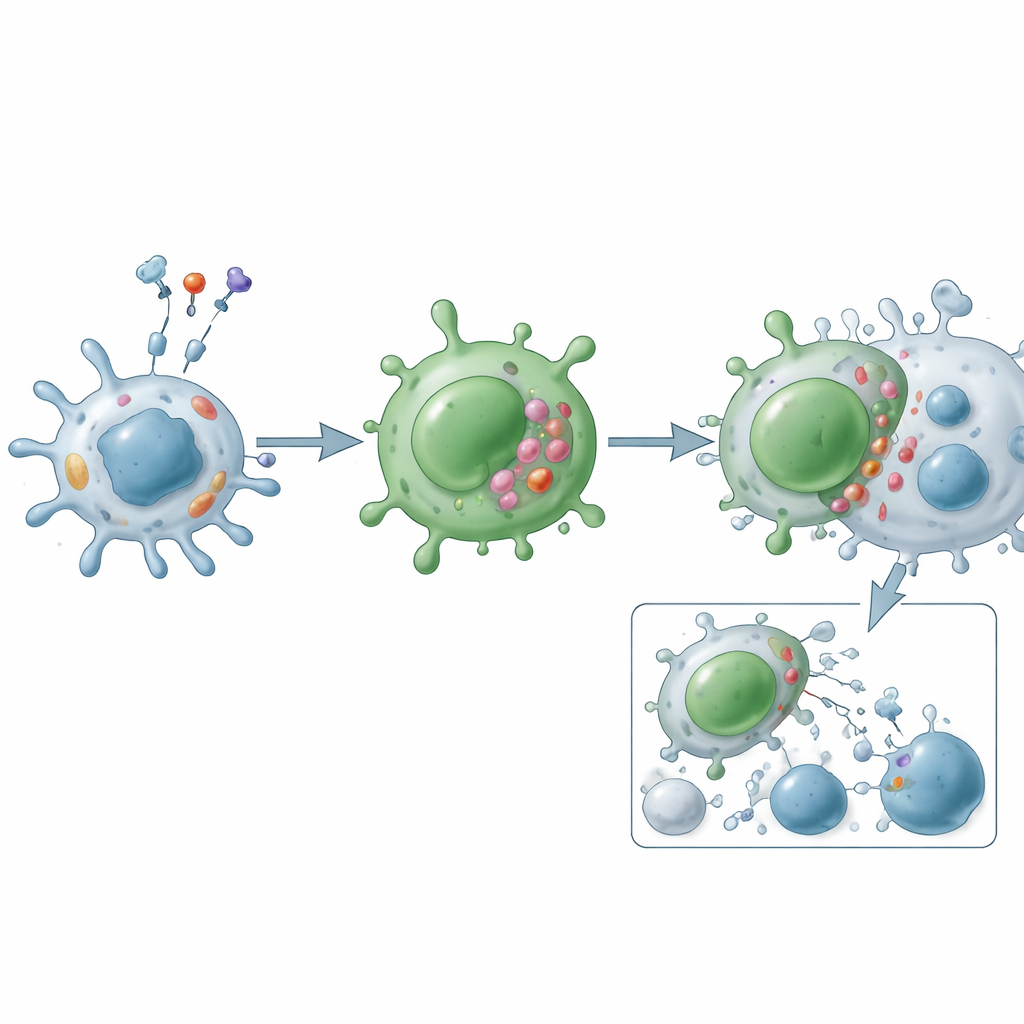
Freunde bei Infektionen und Krebs, Gegner bei Autoimmunität und Herzerkrankungen
Dieses zweischneidige Verhalten zeigt sich in vielen Krankheitsbildern. Bei chronischer Hepatitis B, HIV und COVID-19 helfen zytotoxische CD4-T-Zellen, Viren zu kontrollieren, wenn CD8-Killer erschöpft sind, und ihr Vorhandensein kann mit besserer Kontrolle oder Erholung korrelieren. In soliden Tumoren und Bluttumoren können sie Tumorzellen direkt erkennen, die die passenden immunologischen Marker oder Stresssignale zeigen, und die Reaktionen auf Immuntherapien wie Checkpoint-Inhibitoren und CAR-T-Zell-Behandlungen verbessern. Zugleich können dieselben Mechanismen schaden: Bei Lupus, Rheumatoider Arthritis, entzlicher Darmerkrankung, koronarer Herzkrankheit, Vorhofflimmern, Riesenzellarteriitis und Transplantatabstoßung infiltrieren expandierte zytotoxische CD4-T-Zellen Gewebe, schädigen Blutgefäße oder Organe und verstärken anhaltende Entzündungen, was oft mit einer schlechteren Prognose einhergeht.
Ein riskantes Werkzeug zur Therapie machen
Da zytotoxische CD4-T-Zellen entweder schützend oder zerstörerisch wirken können, hebt die Arbeit aufkommende therapeutische Strategien hervor, die darauf abzielen, diese Population fein zu justieren, statt sie einfach zu eliminieren. Ein Ansatz ist, ihre schädliche Aktivität mit selektiven Inhibitoren zu dämpfen, die kostimulatorische Rezeptoren (wie OX40 oder 4-1BB), entzündliche Zytokine, Ionenkanäle oder Überlebenswege gezielt ansprechen. Ein anderer besteht darin, ihre Tötungskraft in adoptiven Zelltherapien zu nutzen, einschließlich genetisch modifizierter T-Zellen und CAR-T-Zellen, wobei zytotoxische CD4-Zellen oft eine bessere Persistenz zeigen als rein CD8-basierte Produkte. Eine dritte Strategie schlägt vor, langlebige, virus-spezifische CD4-Killer durch Impfstoffe oder pathogenderivierte Peptide, die von Krebszellen präsentiert werden, auf Tumoren umzulenken. Zusammen positionieren diese Forschungsrichtungen zytotoxische CD4-T-Zellen nicht nur als biologische Kuriosität, sondern als zentrales Element für künftige Behandlungen, die gezielter Abwehr gegen Infektionen und Krebs stärken und zugleich gewebeschädigende Entzündungen reduzieren könnten.
Ein neuer Hebel für zukünftige Immuntherapien
Für Nicht-Spezialisten lautet die Kernbotschaft, dass „helfende“ CD4-T-Zellen weit vielseitiger sind, als früher angenommen: Einige können in vollständig bewaffnete Killer umschalten, die uns vor persistierenden Infektionen und Krebs schützen, gleichzeitig aber Autoimmunität, Gefäßschäden und Transplantatabstoßung antreiben. Die Übersicht argumentiert, dass das Erlernen von Methoden zur Verfolgung dieser Zellen, zur Vorhersage, wann sie nützlich oder schädlich sind, und zur Steuerung ihres Verhaltens mit Medikamenten oder konstruierten Therapien, die Behandlung zahlreicher chronischer Krankheiten — von Hepatitis und HIV bis zu Arthritis, Kolitis, Herzerkrankungen und Leukämie — neu gestalten könnte. Anstatt das Immunsystem einfach hoch- oder runterzufahren, könnten zukünftige Therapien vermehrt dadurch wirken, mächtige Zelltypen wie zytotoxische CD4-T-Zellen auf nützliche Ziele zu lenken und von eigenem Gewebe fernzuhalten.
Zitation: Lai, L., Ran, S., Li, Y. et al. Cytotoxic CD4+ T cells: origin, biological functions, diseases and therapeutic targets. Sig Transduct Target Ther 11, 85 (2026). https://doi.org/10.1038/s41392-025-02533-z
Schlüsselwörter: zytotoxische CD4 T-Zellen, Plastizität von Immunzellen, chronische Entzündung, Krebsimmuntherapie, Autoimmunerkrankung