Clear Sky Science · de
Die onkogene Steuerung der Nukleotidsynthese
Warum Krebszellen sich für Bausteine interessieren
Krebs wird oft als unkontrolliertes Zellwachstum beschrieben. Um sich jedoch zu kopieren, brauchen diese Zellen eine konstante Versorgung mit winzigen Bausteinen, den Nukleotiden, die DNA und RNA bilden und viele zelluläre Prozesse mit Energie unterstützen. Diese Übersicht erklärt, wie krebsverursachende Gene die Zellchemie umprogrammieren, um die Nukleotidproduktion hochzuhalten, wie Tumoren zwischen verschiedenen Wegen zur Beschaffung dieser Moleküle wechseln und wie Ärzte diese Strategien mit alten und neuen Medikamenten ausnutzen können.
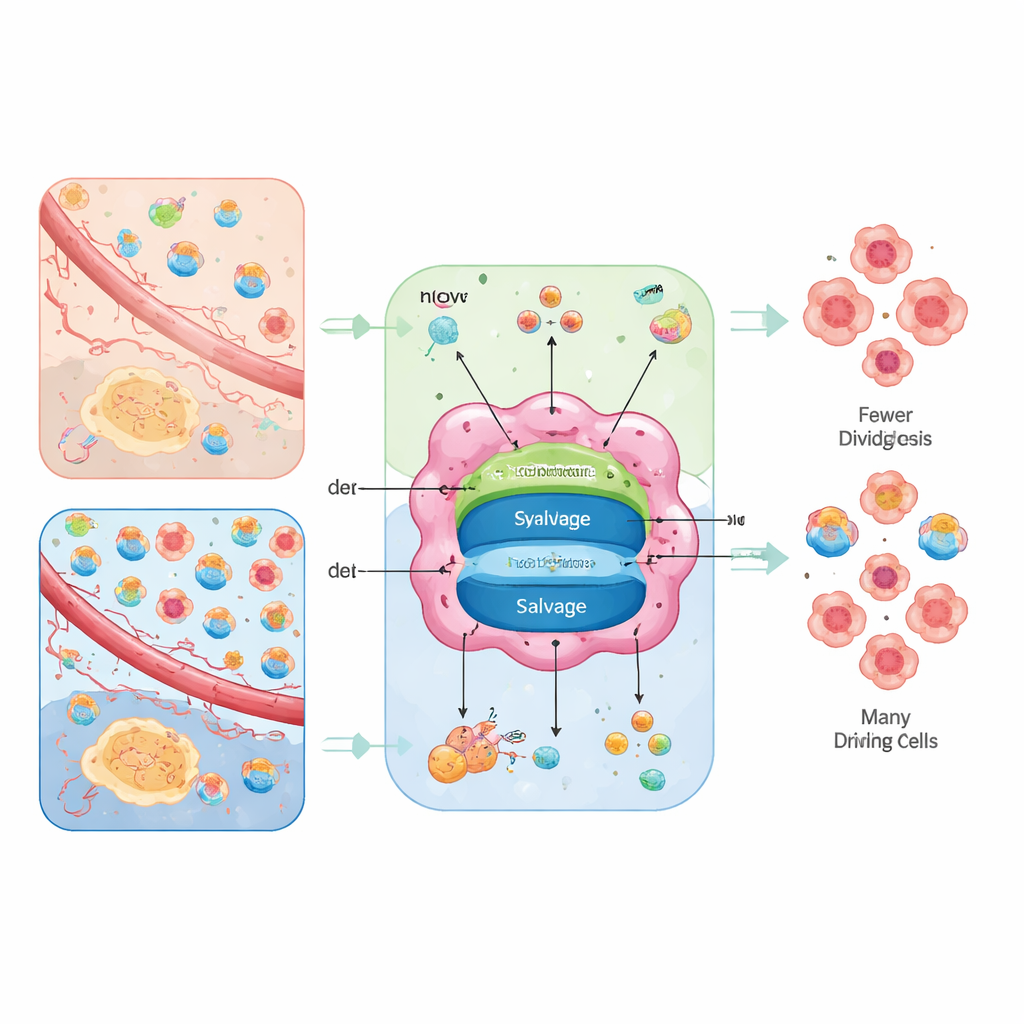
Zwei Wege zu denselben Bausteinen
Zellen können Nukleotide entweder von Grund auf neu synthetisieren oder recyceln. Der „von Grund auf“-Weg, die de-novo-Synthese, baut Ringe aus einfachen Nährstoffen wie Glukose, Aminosäuren, Kohlendioxid und Bikarbonat auf und verwendet energieaufwendige, mehrstufige Reaktionen. Der Recyclingweg, Salvage genannt, nimmt abgebauten Basen und Nukleoside von außen oder aus dem zellulären Abfall auf und fügt sie mit deutlich geringerem Energieaufwand wieder in nutzbare Nukleotide ein. Tumoren nutzen beide Optionen, aber das Gleichgewicht hängt von ihrer inneren Energieversorgung und dem Angebot des umliegenden Gewebes ab.
Wie das Tumorumfeld die Wahl lenkt
Die Autoren stellen die Nukleotidversorgung als ein „umfeldgesteuertes Routing“ dar. In schlecht versorgten Regionen, in denen Aminosäuren vorhanden sind, freie Nukleoside aber knapp sind, stützen sich Krebszellen stark auf de-novo-Wege und werden anfällig für Wirkstoffe, die diese Schritte blockieren. In besser durchbluteten Bereichen, in denen das Blut viele Nukleoside liefert oder die Mitochondrien schwach sind, können Tumoren stärker auf Salvage setzen und reagieren stattdessen auf Blocker von Transportern, die die Nukleosidaufnahme verhindern. Wenn beide Optionen offenstehen, zeigen Tumoren metabolische Flexibilität und können einzelnen Medikamenten ausweichen; sind beide Wege versperrt, stockt die DNA-Replikation, Schäden häufen sich und Zellen sterben oder differenzieren in reifere, weniger aggressive Zustände.
Versteckte Unterstützungsleitungen für die Nukleotidversorgung
Um die Nukleotidfabriken am Laufen zu halten, braucht es mehrere unterstützende Kreisläufe. Der Pentosephosphatweg liefert das Zuckergerüst und Reduktionskraft; Glutamin und der energieproduzierende Zyklus in den Mitochondrien liefern Stickstoff und Aspartat; Serin-, Glycin- und Folatchemie spenden Ein-Kohlenstoff-Einheiten, die die Ringe vervollständigen; Bikarbonat bringt essentielle Kohlenstoffatome ein. Krebs-Treiber wie PI3K–AKT–mTORC1, RAS–MAPK und MYC drehen gemeinsam an diesen Pfaden, erhöhen Schlüsselenzymspiegel und bilden teils sogar Multi-Enzym-Komplexe, die instabile Zwischenprodukte effizient weiterreichen. Im Gegensatz dazu wirken Stresssensoren wie LKB1–AMPK und p53 normalerweise wie Bremsen, die die Nukleotidproduktion drosseln, wenn Energie oder DNA-Integrität bedroht sind — Bremsen, die viele Tumoren außer Kraft setzen.
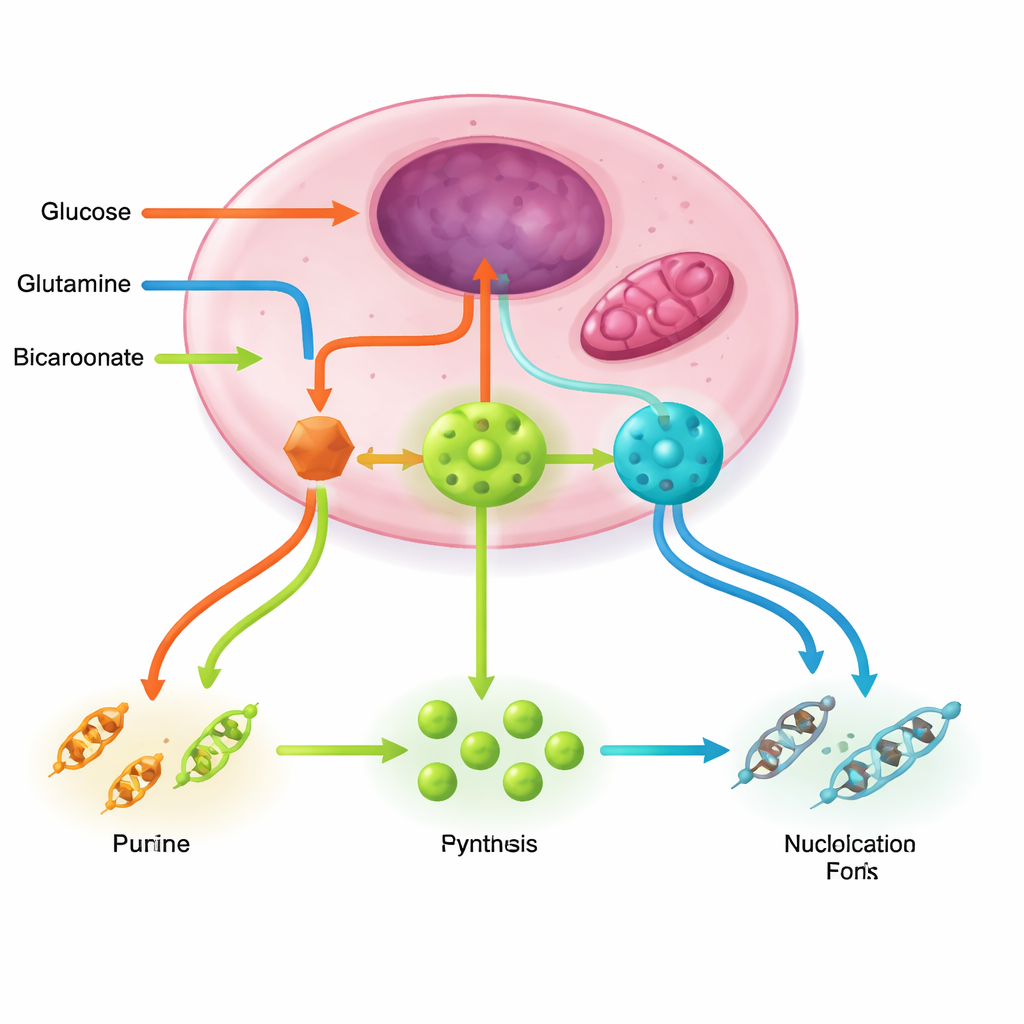
Alte Chemotherapie, neue metabolische Logik
Weil schnell wachsende Zellen stark von Nukleotiden abhängen, zielten einige der frühesten Chemotherapien auf diese Schwäche ab. Klassische Medikamente wie Methotrexat, 5‑Fluorouracil, Cytarabin, Gemcitabin und verschiedene Purinanaloga blockieren entweder die Folsäurenutzung, hemmen spezifische Enzyme oder täuschen fehlerhafte Bausteine vor, die DNA und RNA vergiften. Die Übersicht beleuchtet diese Mittel durch das Routing-Modell und erklärt, warum Nebenwirkungen und Resistenz häufig sind: Nichtkrebshaltige Gewebe brauchen ebenfalls Nukleotide, und Tumoren können oft den Fluss über Salvage- oder parallele Wege umleiten, wenn ein Knoten blockiert ist.
Strategien der nächsten Generation und offene Fragen
Neuere Ansätze zielen darauf ab, selektiver zu sein, indem sie die am stärksten krebs-biasierten Teile des Netzwerks angreifen. Experimentelle Wirkstoffe werden gegen mitochondriale Ein-Kohlenstoff-Enzyme wie MTHFD2, das Pyrimidin-Enzym DHODH und Purin-Enzyme wie IMPDH und PAICS entwickelt, oft in Kombinationen, die auch Salvage-Transporter blockieren. Die Autoren schlagen praktische Marker vor — etwa Transporterlevel, Dichte von Blutgefäßen, mitochondriale Fitness und die Expression bestimmter Stoffwechselenzyme — um zu entscheiden, welche Tumoren stärker auf de-novo oder Salvage angewiesen sind und um Patienten passenden, Pfad-gezielten Therapien zuzuordnen. Blickt man nach vorn, heben sie zentrale Fragen hervor: wie sich diese Wege räumlich und zeitlich in realen Tumoren verschieben, wie umliegende Immun- und Stromazellen die Nukleotidverfügbarkeit formen und wie man verträgliche Medikationspläne gestaltet, die Replikationsstress ausnutzen, ohne normales Gewebe zu überlasten. Zusammen argumentiert diese Arbeit, dass das Verständnis und die gezielte Beeinflussung des Nukleotidstoffwechsels eine grundlegende Voraussetzung der Zellteilung in ein kraftvolles, personalisiertes Hebelwerk gegen Krebs verwandeln könnte.
Zitation: Vidal-Cruchez, O., Ben-Sahra, I. The oncogenic control of nucleotide synthesis. Oncogenesis 15, 17 (2026). https://doi.org/10.1038/s41389-026-00608-2
Schlüsselwörter: Nukleotidstoffwechsel, Krebsstoffwechsel, de-novo-Synthese, Salvage-Wege, metabolische Therapien