Clear Sky Science · de
Teriflunomid moduliert die PD-1/PD-L1-Achse und stärkt die Antitumor-Immunität bei Darmkrebs
Ein Multiple-Sklerose-Medikament gegen Darmkrebs
Viele moderne Krebstherapien zielen darauf ab, das Immunsystem zu reaktivieren, damit es Tumoren besser erkennen und angreifen kann. Für die meisten Menschen mit kolorektalem (Darm-)Krebs bringen die derzeitigen immunbasierten Therapien jedoch nur begrenzten Nutzen. Diese Studie untersucht einen unerwarteten Verbündeten: Teriflunomid, eine seit Langem zugelassene Tablette gegen Multiple Sklerose, und zeigt, wie es eine wichtige Immun‑„Bremse“ umstellen kann, sodass die körpereigenen Killer‑T‑Zellen in Versuchsmodellen Darmtumoren verkleinern. 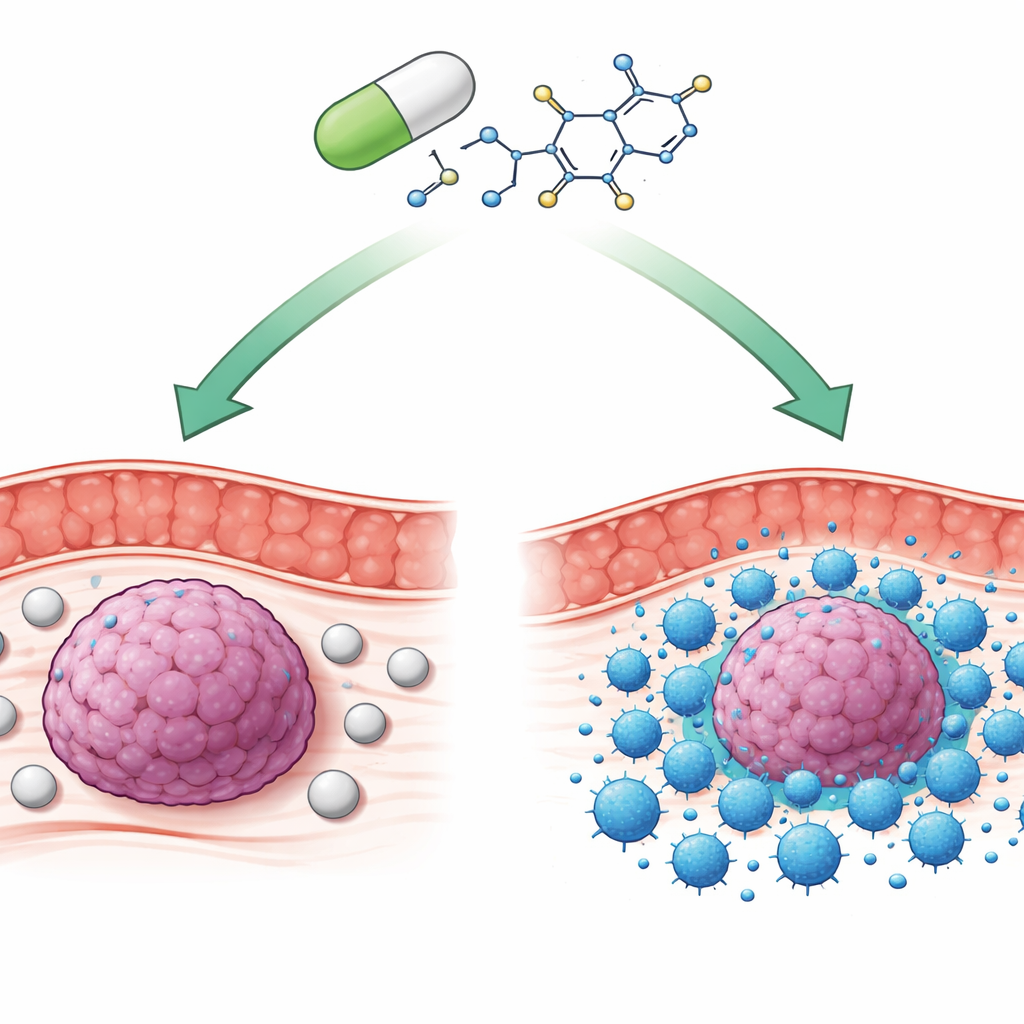
Die Bremsen des Körpers gegen Immunangriffe
Unser Immunsystem beruht auf einem Gleichgewicht aus Gas und Bremse. Eine wichtige Bremse ist das molekulare Händeschütteln zwischen zwei Proteinen, PD-1 auf T‑Zellen und PD‑L1, das häufig auf Tumorzellen präsentiert wird. Wenn sie sich verbinden, werden T‑Zellen erschöpft und hören auf anzugreifen, wodurch Krebs unentdeckt wachsen kann. Bestehende Medikamente, die dieses Händeschütteln blockieren — überwiegend Antikörperinfusionen, die klinisch verabreicht werden — haben die Behandlung mancher Krebsarten revolutioniert. Bei den meisten Darmkrebsen, besonders dem häufigen „mikrosatellitenstabilen“ Typ, wirken diese Medikamente jedoch schlecht, und viele Patientinnen und Patienten sprechen entweder gar nicht an oder entwickeln später eine Resistenz.
Ein altes Medikament mit neuer Aufgabe
Teriflunomid ist ein oral verabreichtes Medikament, das seit Jahren zur Behandlung der Multiplen Sklerose eingesetzt wird, indem es überaktive Immunzellen dämpft. Wegen seiner bekannten Sicherheit beim Menschen ist es ein attraktiver Kandidat zur Wiederverwendung, falls sich zeigt, dass es das Immunsystem bei Krebs eher unterstützt als unterdrückt. Die Forschenden untersuchten, ob Teriflunomid direkt auf das PD‑1/PD‑L1‑System in Darmkrebszellen und T‑Zellen wirken kann. An mehreren im Labor gezüchteten menschlichen Darmkrebszelllinien stellten sie fest, dass Teriflunomid die Menge an PD‑L1‑Protein auf Tumorzellen verringerte, ohne die Zellen bei den getesteten Dosen direkt abzutöten. Interessanterweise resultierte dieser Effekt nicht aus einer Abschaltung des PD‑L1‑Gens; stattdessen beschleunigte das Medikament den Abbau des PD‑L1‑Proteins in zellulären „Recyclingzentren“, den Lysosomen.
Die Immun‑Handshake blockieren und T‑Zellen stärken
Um zu untersuchen, wie Teriflunomid die Immunbremse direkt beeinflusst, prüfte das Team dessen Einfluss auf die Bindung zwischen PD‑1 und PD‑L1. Biochemische Tests und Computer‑Modelle zeigten, dass Teriflunomid an PD‑1 selbst binden kann und sich in die Region einlagert, an die PD‑L1 normalerweise andockt. Dieser direkte Kontakt blockierte die PD‑1/PD‑L1‑Interaktion bereits bei sehr niedrigen Medikamentenkonzentrationen. In konstruierten Zellssystemen, die den Immuncheckpoint nachahmen, stellte Teriflunomid die Signalgebung in T‑Zellen wieder her — ein Zeichen dafür, dass die Bremse gelöst wurde. Wenn Tumorzellen und T‑Zellen gemeinsam kultiviert wurden, senkte Teriflunomid sowohl die PD‑L1‑Werte auf Krebszellen als auch erhöhte Marker für T‑Zell‑Aktivierung und -Killerfunktion.
Vom Reagenzglas zu tumorbefallenen Mäusen
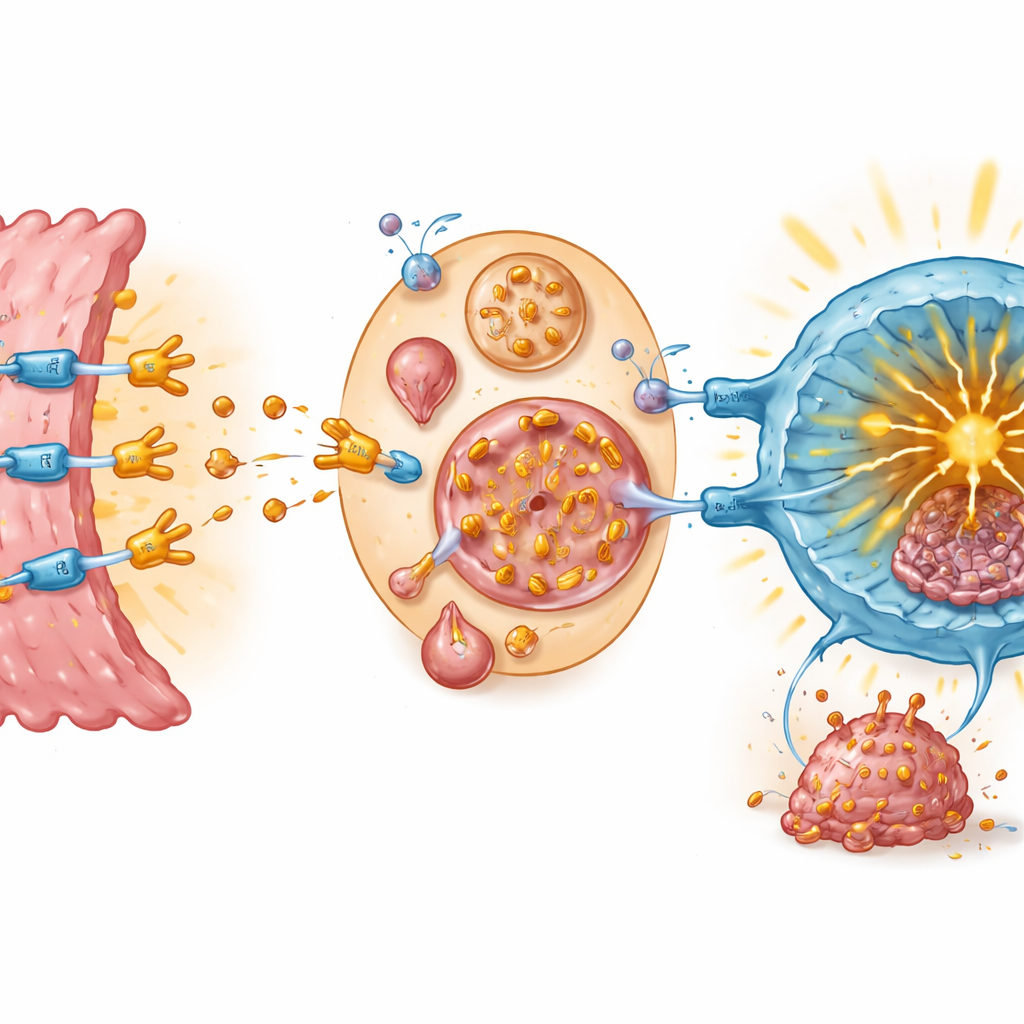
Was das für die zukünftige Krebsversorgung bedeuten könnte
Für Laien ist die Kernaussage, dass Teriflunomid offenbar als doppelt wirkender Checkpoint‑Blocker fungiert: Es bindet an PD‑1 auf T‑Zellen, um ein lähmendes Händeschütteln zu verhindern, und zugleich treibt es Tumorzellen dazu, ihren PD‑L1‑Schutz zu entsorgen. Zusammengenommen erlauben diese Wirkungen, dass Killer‑T‑Zellen in Tumoren eindringen und sie effektiver angreifen in Modellen des Darmkrebses. Da Teriflunomid bereits zugelassen ist und sein Sicherheitsprofil gut dokumentiert ist, könnte es schneller in Krebsstudien überführt werden als ein völlig neues Medikament. Obwohl Studien am Menschen noch erforderlich sind, legt diese Arbeit nahe, dass eine bekannte Multiple‑Sklerose‑Tablette eines Tages Teil kombinierter Strategien für Menschen mit Darmkrebs werden könnte, die von den aktuellen Immuntherapien nicht profitieren.
Zitation: Han, J.H., Lee, EJ., Park, YH. et al. Teriflunomide modulates the PD-1/PD-L1 axis and enhances antitumor immunity in colorectal cancer. Oncogenesis 15, 15 (2026). https://doi.org/10.1038/s41389-026-00607-3
Schlüsselwörter: Immuntherapie bei Darmkrebs, PD-1 PD-L1 Kontrollpunkt, Teriflunomid, CD8-T-Zellen, Wirkstoff-Repositionierung