Clear Sky Science · de
Transkriptomische Profilierung von Krebszellen und Wirtszellen in Ko-Kultur identifiziert Hypoxie als Treiber des antiproliferativen Effekts von Skelettmuskelzellen auf Krebszellen
Warum einige Gewebe der Krebsausbreitung widerstehen
Krebs wird meist dann lebensbedrohlich, wenn Tumorzellen ihren Ursprungsort verlassen und sich in entfernten Organen niederlassen. Auffällig ist, dass einige Gewebe, etwa die Lunge, häufig Zielorte sind, während andere, wie der Skelettmuskel, trotz ihres großen Anteils am Körpergewicht so gut wie nie kolonisiert werden. Die Studie stellt eine einfache, aber wichtige Frage für Patienten und Ärzte: Was ist es am Muskel, das ihn zu einem so ungünstigen „Boden“ für Krebszellen macht, und könnte das Verständnis dieser natürlichen Abwehr unser Denken über die Behandlung von Metastasen verändern?
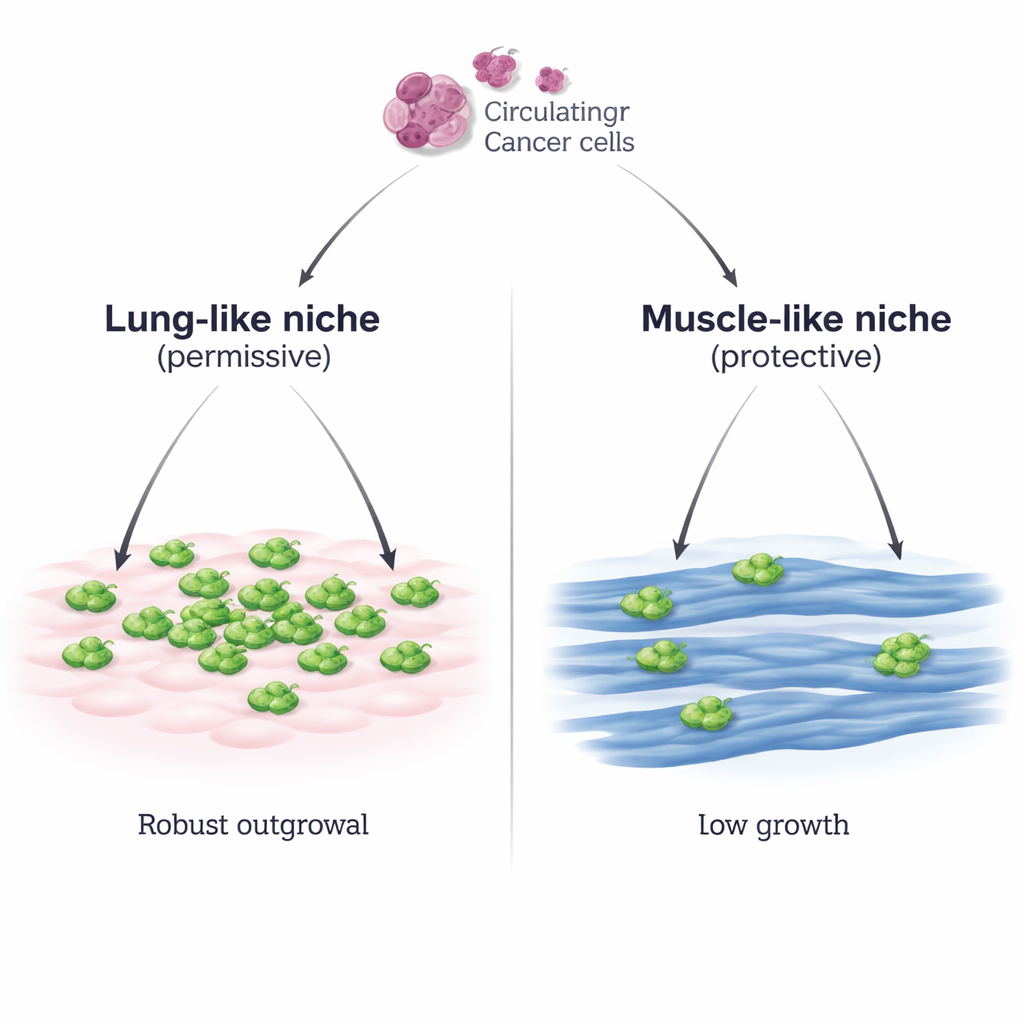
Zwei Nachbarschaften für reisende Tumorzellen
Die Forschenden entwickelten ein kontrolliertes Laborsystem, das zwei verschiedene Nachbarschaften nachbildet, denen eine Brustkrebszelle begegnen könnte: eine lungenähnliche Umgebung aus Lungen-Bindegewebszellen (MLg) und eine muskelähnliche Umgebung aus ausgereiften Skelettmuskelfasern (C2C12-Myotuben). Sie setzten Maus-Brustkrebszellen auf jede Schicht und beobachteten, was geschah. Auf den lungenähnlichen Zellen hefteten sich die Krebszellen gut an und vermehrten sich schnell, sodass dichte Zellverbände entstanden. Auf den Muskelzellen hefteten sie sich ebenso gut an, ihr Wachstum blieb jedoch spärlich und langsam, selbst wenn die Ausgangszahl der Krebszellen stark erhöht wurde oder eine zweite Brustkrebszelllinie verwendet wurde. Eine weitere Skelettmuskellinie (Sol8) zeigte dieselbe Fähigkeit, das Krebswachstum zu bremsen, was unterstreicht, dass dies eine allgemeine Eigenschaft von Muskelzellen und kein Zufall einer einzelnen Zelllinie ist.
Wie Krebs- und Wirtszellen ihre Aktivität umprogrammieren
Um zu verstehen, was in den Zellen vor sich ging, isolierte das Team Krebs- und Wirtszellen aus diesen Mischkulturen und sequenzierte deren RNA – ein Maß dafür, welche Gene an- oder abgeschaltet sind. Krebszellen, die auf Muskelfasern saßen, zeigten weitaus umfangreichere Veränderungen der Genaktivität als solche, die auf Lungenzellen wuchsen, was darauf hindeutet, dass die Muskelumgebung sie zu starken Anpassungen zwingt. Im Muskelumfeld schalteten Krebszellen Programme ein, die mit muskelähnlichen Merkmalen, Energiestoffwechsel und überraschenderweise mit Reaktionen auf niedrigen Sauerstoff (Hypoxie) verbunden sind. Gleichzeitig wurden die üblichen Genprogramme, die schnelles Zellwachstum antreiben, heruntergefahren. Im Gegensatz dazu behielten Krebszellen auf Lungenzellen ein stark wachstumsorientiertes Profil bei und benötigten deutlich weniger Umprogrammierung, was mit der Vorstellung übereinstimmt, dass die lungenähnliche Nische permissiv und leicht auszunutzen ist.
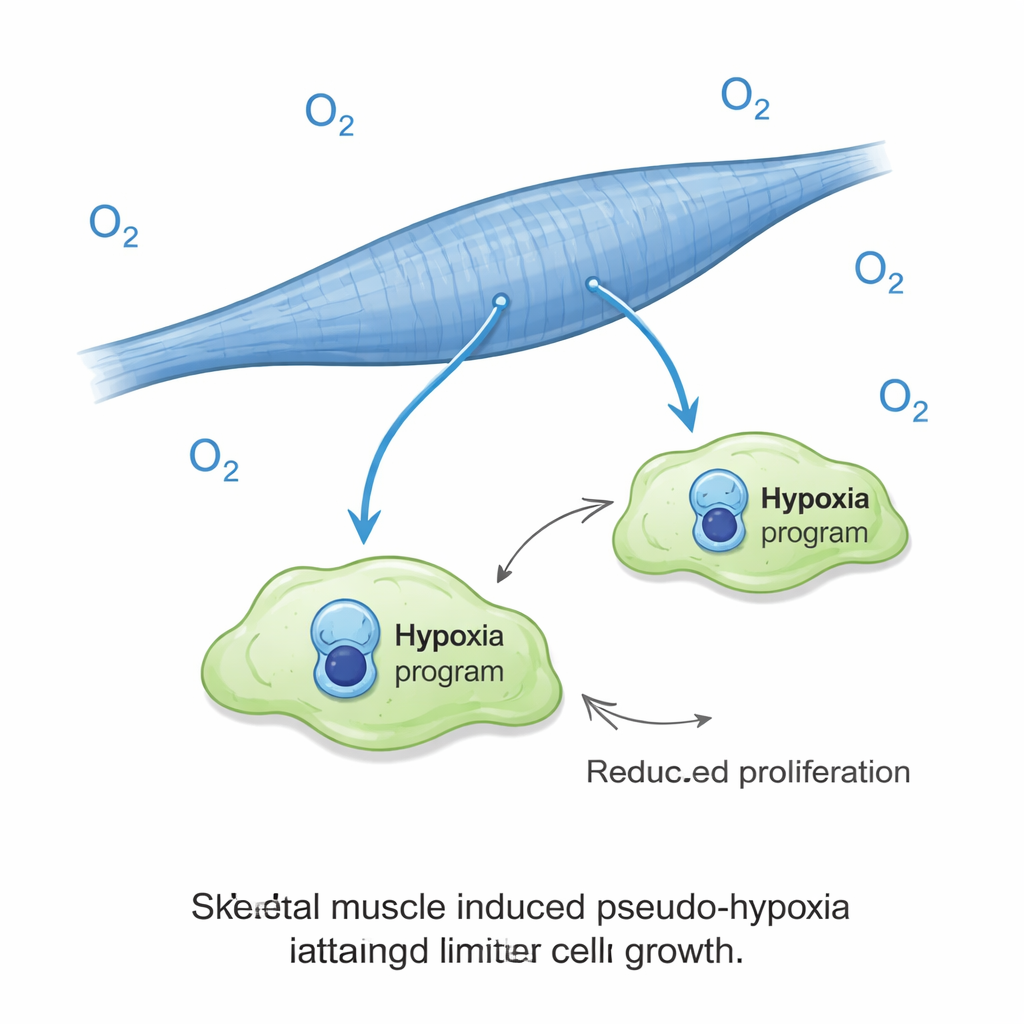
Eine überraschende Rolle für Niedrigsauerstoffsignale
Eines der auffälligsten Ergebnisse war, dass Krebszellen auf Muskelfasern eine hypoxieähnliche Gen-Signatur aktivierten, obwohl sie unter normalen Sauerstoffbedingungen kultiviert wurden. In den meisten Tumoren gilt Hypoxie als schlechtes Zeichen, meist verbunden mit aggressivem Verhalten und schlechter Prognose. Hier war sie mit dem Gegenteil verbunden: schlechtem Wachstum. Die Wissenschaftler setzten die Kulturen daraufhin tatsächlich niedrigen Sauerstoffwerten aus und stellten fest, dass dies die Ausdehnung der Krebszellen auf Muskel fast völlig unterdrückte, während es das Krebswachstum in den lungenähnlichen Kulturen tatsächlich förderte. Mit anderen Worten: Dasselbe Signal, das Tumoren normalerweise zum Gedeihen verhilft, wurde zur Bremse, wenn sich die Krebszellen in einer Muskelumgebung befanden. Dieser Sauerstoffeffekt ließ sich offenbar nicht durch einfache Veränderungen von Lactat, Azidität oder Zuckerverfügbarkeit im Kulturmedium erklären.
Mehr als nur sekretierte Faktoren
Das Team prüfte außerdem, ob einfache lösliche Stoffe, die von Muskelzellen freigesetzt werden, ihren Schutzeffekt erklären könnten. Die Zugabe von zusätzlichem Lactat, das Verändern des pH-Werts, das Ändern des Glukosespiegels oder das Kultivieren von Krebszellen in Medium, das zuvor Muskelzellen ausgesetzt war, reproduzierte nicht die starke Unterdrückung, die in direkten Kontakt-Ko-Kulturen beobachtet wurde. Das deutet darauf hin, dass enger physischer Kontakt oder sehr kurzreichweitige Signale an der Zelloberfläche entscheidend dafür sind, wie Muskelzellen Krebszellen in einen niedrigwachsenden, möglicherweise ruhenden Zustand drängen. Interessanterweise blieben Muskelzellen selbst relativ stabil in ihrer Genaktivität gegenüber Krebs, während Lungenzellen leichter umprogrammiert wurden, was den Muskel als robustes, „metastaseresistentes“ Gewebe hervorhebt.
Was das für Patienten und Therapien bedeutet
Insgesamt zeigt die Studie, dass Skelettmuskel als feindliches Habitat wirkt und Krebszellen in einen hypoxieähnlichen, niedrigproliferativen Modus zwingt, selbst wenn ausreichend Sauerstoff vorhanden ist. Das hilft zu erklären, warum Muskel so seltenes Metastasierungsziel ist. Es enthält auch eine mahnende Botschaft für die Wirkstoffentwicklung: Therapien, die darauf abzielen, Hypoxie-Signale im gesamten Körper zu blockieren, könnten unbeabsichtigt diese natürliche muskelbasierte Abwehr schwächen und es Krebszellen erleichtern, dort zu wachsen, wo sie es normalerweise nicht tun. Das Verständnis und der Erhalt oder sogar die Nachahmung der schützenden Eigenschaften von Muskelgewebe könnten neue Wege zur Prävention oder Kontrolle metastasierter Erkrankungen eröffnen.
Zitation: Aunan, A., Claeyssen, C., Abdelhalim, M. et al. Transcriptomic profiling of co-cultured cancer-host cells identifies hypoxia as a driver of the skeletal muscle cell’s anti-proliferative effect on cancer cells. Oncogenesis 15, 7 (2026). https://doi.org/10.1038/s41389-026-00601-9
Schlüsselwörter: Krebsmetastasen, Skelettmuskel, Hypoxie, tumoröses Mikromilieu, Krebsdormanz