Clear Sky Science · de
Die Aufnahme von Fettsäuren durch FABP4 fördert die Seneszenz von CD8+-T-Zellen durch Lipidperoxidation in der adipocytreichen Mikroumgebung des Ovarialkarzinoms
Warum Fett- und Immunzellen beim Ovarialkarzinom wichtig sind
Ovarialkarzinome breiten sich häufig in die Bauchhöhle aus, wo sie auf große Fettdepots treffen. Diese fettreiche Umgebung ist nicht nur eine passive Kulisse – sie beeinflusst aktiv das Verhalten von Immunzellen. Insbesondere kann sie die CD8‑„Killer“‑T‑Zellen schwächen, die Tumore angreifen sollen. Diese Studie untersucht, wie fettbedingte Substanzen diese T‑Zellen in einen gealterten, erschöpften Zustand treiben und wie die Blockade eines zentralen Fetttransportproteins ihre krebsbekämpfenden Funktionen wiederherstellen könnte.
Fettreiche Umgebungen, die Immunverteidiger altern lassen
Ärztinnen und Ärzte haben lange beobachtet, dass viele Frauen mit fortgeschrittenem Ovarialkarzinom Flüssigkeit im Bauch ansammeln und Tumoren in fettreichen Geweben, dem Omentum, lokalisiert sind. Durch Analyse von Einzelzell‑RNA‑Daten von Patientinnen und mikroskopische Untersuchung von Tumorproben fanden die Forschenden heraus, dass CD8‑T‑Zellen in der Nähe dieser Fettdepots eher Merkmale zellulärer Alterung, also Seneszenz, zeigten. Diese „gealterten“ T‑Zellen bauen Abfallpigmente an, teilen sich nicht mehr und produzieren entzündliche Signale statt Krebszellen zu töten. In menschlichen Proben und Mausmodellen waren CD8‑T‑Zellen aus fett‑ und flüssigkeitsreichen Tumorregionen deutlich seneszenter als solche aus Lymphknoten oder Milz, was die Verbindung zwischen der adipocytreichen Tumormikroumgebung und T‑Zell‑Alterung belegt.
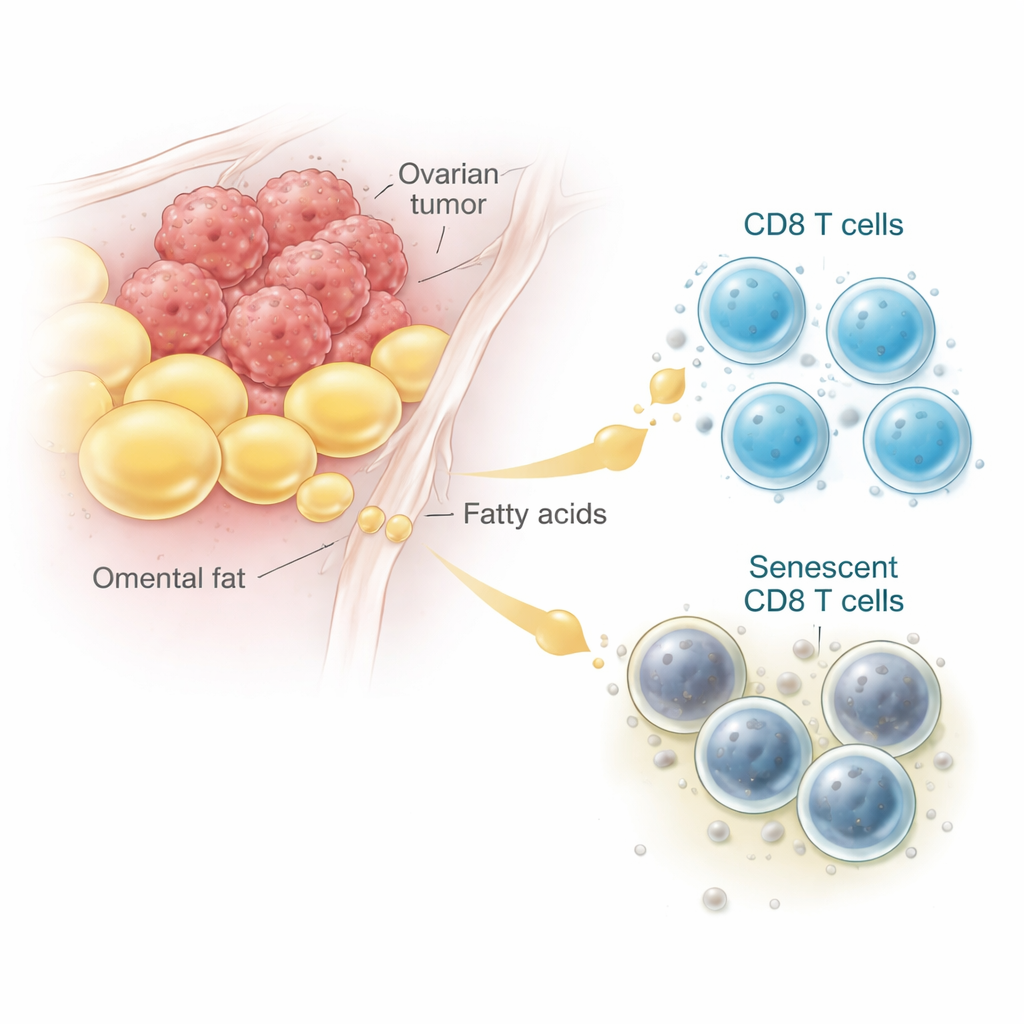
Wie eine häufige Fettsäure hilfreichen Brennstoff in Schaden verwandelt
Um zu verstehen, was das Fett mit T‑Zellen macht, rekonstruierten die Forschenden die Tumorumgebung im Labor. Sie kultivierten Ovarialkarzinomzellen zusammen mit Maus‑CD8‑T‑Zellen und fügten entweder Extrakte aus Fettgewebe oder eine bestimmte Fettsäure, Oleinsäure, hinzu, die in der Flüssigkeit von Ovarialkarzinomen reichlich vorkommt. Bei mittleren bis hohen Dosen förderte Oleinsäure die Seneszenz von CD8‑T‑Zellen – jedoch nur in Anwesenheit von Tumorzellen. Anstatt die eingehenden Fette zur Energiegewinnung zu verbrennen, akkumulierten die T‑Zellen Lipide, die chemisch geschädigt wurden, ein Prozess, der als Lipidperoxidation bekannt ist. Gen‑ und Lipidanalysen zeigten erhöhte Marker für oxidierte Fette und Stress, während die Energiegewinnung aus Fett unverändert blieb. Kurz gesagt: In Anwesenheit von Tumorzellen wurde Fett, das eigentlich Brennstoff sein sollte, in schädigende Reaktionen umgeleitet, die T‑Zellen altern und funktionsunfähig machen.
Der Fetttransporter FABP4 als wichtiger Torwächter
Bei tiefergehenden Untersuchungen fragten die Forschenden, welche Moleküle diesen schädlichen Fettzufluss steuern. Sie stellten fest, dass ein Transportprotein namens FABP4 in CD8‑T‑Zellen, die Fett‑Extrakten oder Oleinsäure ausgesetzt waren, stark hochreguliert wurde. FABP4 wirkt wie ein Shuttle und transportiert langkettige Fettsäuren in die Zellen. Als sie FABP4 entweder mit einem kleinen Molekülinhibitor (BMS309403) oder durch genetische Abschaltung blockierten, nahmen die T‑Zellen weniger Fett auf, zeigten weniger Lipidperoxidation und wurden seltener seneszent. Diese geschützten T‑Zellen teilten sich besser, produzierten mehr krebsabtötende Moleküle wie Interferon‑gamma und Granzyme B und setzten weniger unterdrückende und entzündliche Signale frei. Die Wiederherstellung von FABP4 hob diese Vorteile wieder auf, was bestätigt, dass dieses Transportprotein ein zentraler Schalter ist, der Fettaufnahme mit T‑Zell‑Alterung verknüpft.
Von Mausversuchen zu einer möglichen Behandlungsstrategie
Das Team testete dann die Blockade von FABP4 in lebenden Mäusen mit Ovarialkarzinom, das sich in der Bauchhöhle ausgebreitet hatte. Die Behandlung mit dem FABP4‑Inhibitor reduzierte die Fettaufnahme und Lipidschäden in CD8‑T‑Zellen aus der Bauchaußenflüssigkeit, verringerte den Anteil seneszenter T‑Zellen und erhöhte die Konzentration wichtiger Effektormoleküle. In Kombination mit Standard‑Chemotherapie hatten die Mäuse weniger sichtbare Tumorknoten, stärkere T‑Zell‑Antworten in Milz, Lymphknoten und Aszites und überlebten länger als diejenigen, die nur Chemotherapie erhielten. Diese Ergebnisse legen nahe, dass das Anvisieren des Fettstoffwechsels die Wirksamkeit bestehender Therapien verbessern kann, indem es die vordersten Soldaten des Immunsystems wiederbelebt.
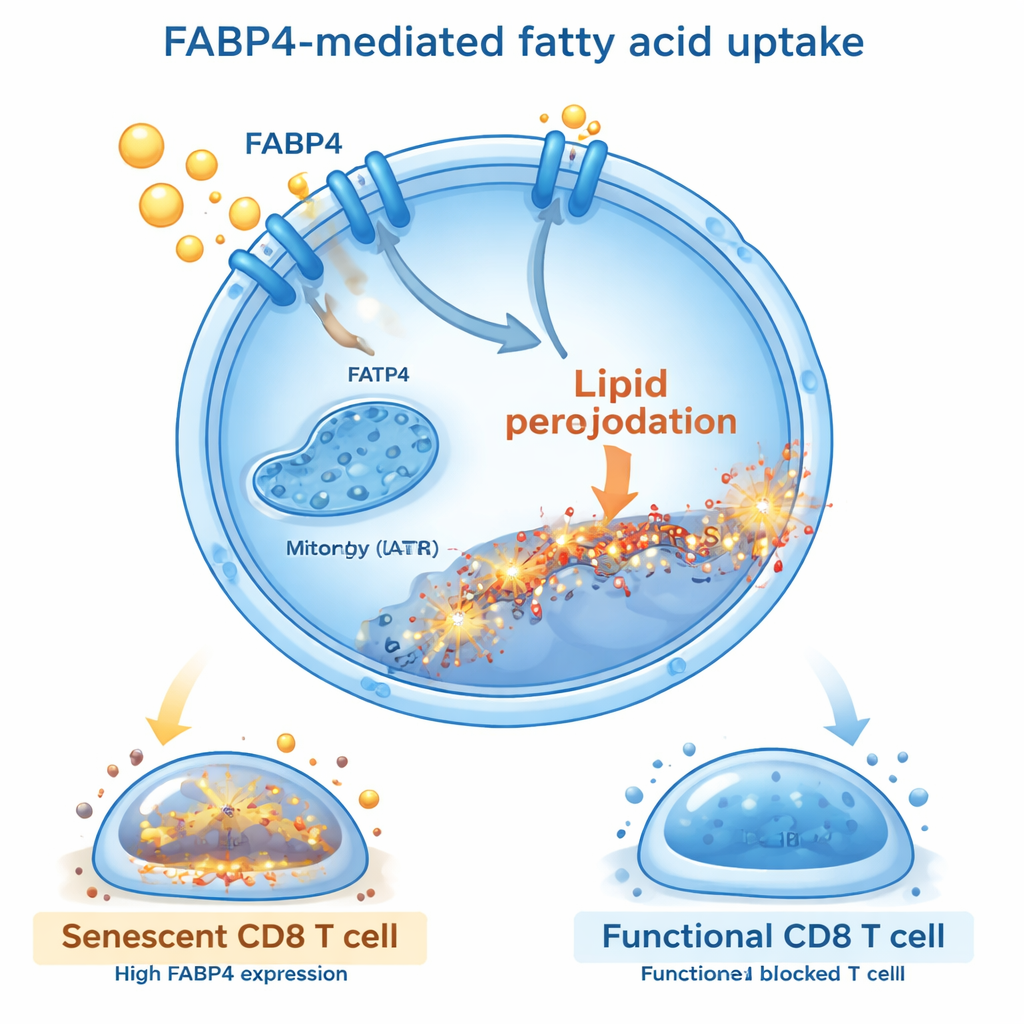
Was das für Patientinnen bedeutet
Für allgemeine Leserinnen und Leser lautet die Kernaussage: Beim Ovarialkarzinom zählt nicht nur der Tumor selbst, sondern auch die fettreiche Nachbarschaft, in der er lebt. Fettabgeleitete Moleküle, insbesondere bestimmte Fettsäuren, können Killer‑T‑Zellen vorzeitig altern lassen und ihnen ihre Angriffsfähigkeit rauben. Diese Arbeit identifiziert den Fetttransporter FABP4 als wichtigen Schuldigen in diesem Prozess. Durch die Blockade von FABP4 können Forschende zumindest bei Mäusen die T‑Zell‑Seneszenz reduzieren, deren Tötungsfunktion wiederherstellen und die Wirkung der Chemotherapie verbessern. Zwar ist weitere Forschung nötig, bis dies eine Patientenbehandlung wird, doch die Studie öffnet einen neuen Weg: nicht nur den Krebs selbst zu behandeln, sondern auch die metabolischen Fallen in seiner Umgebung, die das Immunsystem entwaffnen.
Zitation: Yu, C., Li, X., Qian, X. et al. Fatty acid uptake mediated by FABP4 promotes the formation of CD8+T cell senescence through lipid peroxidation in the adipocyte-rich microenvironment of Ovarian Cancer. Oncogenesis 15, 9 (2026). https://doi.org/10.1038/s41389-026-00600-w
Schlüsselwörter: Ovarialkarzinom, T‑Zell‑Seneszenz, Fettsäurestoffwechsel, Tumormikroumgebung, FABP4